��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��T��ʱ����1 L�̶�������ܱ�����M�м���2 mol X��1 mol Y���������·�Ӧ��2X(g)��Y(g)  aZ(g)��W(g) ��H����Q kJ/mol(Q��0)���÷�Ӧ�ﵽƽ��ų�������ΪQ1 kJ������X��ת����Ϊ������ƽ����������¶ȣ���������ƽ����Է���������С��
aZ(g)��W(g) ��H����Q kJ/mol(Q��0)���÷�Ӧ�ﵽƽ��ų�������ΪQ1 kJ������X��ת����Ϊ������ƽ����������¶ȣ���������ƽ����Է���������С��
��ش��������⣺
(1)��ѧ������a��ֵΪ________��
(2)������˵���÷�Ӧ�ﵽ�˻�ѧƽ��״̬����________(�����)��
a��������ѹǿһ��
b��������������ܶ�һ��
c��������Z�ķ�����һ��
d�����������������һ��
(3)ά��T���¶Ȳ��䣬����ʼʱ������M�м���2 mol X��1 mol Y��1 mol Ar(ϡ�����岻���뷴Ӧ)����Ӧ�ﵽƽ���ų���������________kJ��
(4)ά��T���¶Ȳ��䣬����һ����ԭ���������ȵĺ�ѹ����N�м���2 mol X��1 mol Y�����������Ӧ���ﵽƽ�⣬��________(�M����N��)�����еķ�Ӧ�ȴﵽƽ��״̬��������X����������M________N(�����������������)��
(5)��֪���÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��������ʾ��
�¶�/��
| 200
| 250
| 300
| 350
|
ƽ�ⳣ��K
| 9.94
| 5.2
| 1
| 0.5
|
?
����ij�¶��£�2 mol X��1 mol Y������M�з�Ӧ���ﵽƽ�⣬X��ƽ��ת����Ϊ50%������¶�Ϊ________�档
(6)ά��T���¶Ȳ��䣬����ʼʱ������M�м���4 mol X��6 mol Y����Ӧ�ﵽƽ��ʱ�����ڵķ�����Ŀ����10%����Ӧ�зų�������Ϊ________kJ��
�ο��𰸣���14�֣�(1)1?(2)ac?(3)Q1? (4) N ?> ?(5)? 350 ?(6) Q
�����������1���÷�Ӧ��һ�����ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ�����������ƽ����Է���������С�����ڻ������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ��������������䣬�����巴Ӧ�������֮�ʹ������������������֮�ͣ�����aֻ�ܵ���1��
��2����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬���ݴ˿����жϡ�a�����ڷ�Ӧǰ������Ļ�ѧ������֮�Ͳ���ȣ�����ڷ�Ӧ������ѹǿ�DZ仯�ģ���ƽ��ʱѹǿ���ٷ����仯�����Ե�ѹǿ���ٷ����仯ʱ������˵���ﵽƽ��״̬����a��ȷ��b���ܶ��ǻ�����������������ݻ��ı�ֵ���������ڹ̶�����������з�Ӧ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ��������Ƿ�ﵽƽ��״̬���ܶȶ����䣬��b����c����Ӧ�ﵽƽ��״̬ʱ�����ʵ�Ũ�ȡ������������Ȳ��ٷ����仯����ƽ��ʱ������Z������һ������c��ȷ��d����Ӧ��������ﶼ�����壬�����Ƿ�ﵽƽ��״̬�������������������һ������d����ѡac��
��3������ʼʱ������M�м���2molX��1molY��1molAr��ϡ�����岻���뷴Ӧ����X��Y��Ũ�Ȳ��䣬������ת���ʲ��䣬�÷�Ӧ�ﵽƽ��״̬ʱ���ų�����������ΪQ1kJ��
��4����������Ӧ�������С�Ŀ��淴Ӧ�����ں��º��������£������������ѹǿ�Ǽ�С�ġ����Ը������£���ѹ�������ȣ��൱������ѹǿ��ѹǿԽ��Ӧ����Խ��Ӧ����ƽ���ʱ��Խ�̣���N�������ȴﵽƽ��״̬������ѹǿƽ��������Ӧ�����ƶ�����X������������С����M>N��
��5��2molX��1molY������M�з�Ӧ���ﵽƽ�⣬x��ƽ��ת����Ϊ50%����ƽ��ʱ��c(X)��(1?50%)��2moL��1L��1mol/L�����ݷ���ʽ��֪ƽ��ʱc(Y)��1mol/L��1mol/L��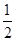 ��0.5mol/L������Z��W��Ũ��c(Z)��c(W)��2mol/L��50%��
��0.5mol/L������Z��W��Ũ��c(Z)��c(W)��2mol/L��50%��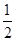 ��0.5mol/L������ݻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ��֪��ƽ�ⳣ��K��
��0.5mol/L������ݻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ��֪��ƽ�ⳣ��K�� ��
��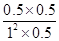 ��0.5�����Ը��ݱ������ݿ�֪���¶���350�档
��0.5�����Ը��ݱ������ݿ�֪���¶���350�档
��6��ͬһ�����У����ʵķ�����֮�ȵ������ʵ���֮�ȣ�����Ӧ�ﵽƽ��ʱ�����ڵķ�����Ŀ����10%ʱ����������ʵ�������10%������������ʵ������٣�4+6��mol��10%��1mol������2X(g)��Y(g)  Z(g)��W(g) ��H����Q kJ/mol��֪������������ʵ�������1molʱ�μӷ�Ӧ��X�����ʵ�����2mol�����Է�Ӧ�зų�������ΪQkJ��
Z(g)��W(g) ��H����Q kJ/mol��֪������������ʵ�������1molʱ�μӷ�Ӧ��X�����ʵ�����2mol�����Է�Ӧ�зų�������ΪQkJ��
�����Ѷȣ�����
2��ѡ���� ��һ�������£���A2��B2����ͨ��1 L�ܱ������У���Ӧ����ʽ���У�mA2��nB2 2C,2 s�ڷ�Ӧ�������£�v(A2)��0.5 mol/(L��s)��v(B2)��1.5 mol/(L��s)��v(C)��1mol/(L��s)����m��n ��ֵ�ֱ�Ϊ
2C,2 s�ڷ�Ӧ�������£�v(A2)��0.5 mol/(L��s)��v(B2)��1.5 mol/(L��s)��v(C)��1mol/(L��s)����m��n ��ֵ�ֱ�Ϊ
[? ]
A��2��3
B��3��2
C��3��1
D��1��3
�ο��𰸣�D
���������
�����Ѷȣ���
3��ѡ���� ��2.0 mol SO �����2.0 mol SO
�����2.0 mol SO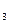 �������ڹ̶�������ܱ������У���һ�������·�����Ӧ��2SO2(g)+O2(g)
�������ڹ̶�������ܱ������У���һ�������·�����Ӧ��2SO2(g)+O2(g) ?2
?2 SO3(g)���ﵽƽ��ʱSO3Ϊn mol ������ͬ�¶��£��ֱ������������ͬ�ܱ������з�����ʼ���ʣ�ƽ��ʱSO3����n mol����?��?��
SO3(g)���ﵽƽ��ʱSO3Ϊn mol ������ͬ�¶��£��ֱ������������ͬ�ܱ������з�����ʼ���ʣ�ƽ��ʱSO3����n mol����?��?��
A��1.6 mol SO2+0.3 mol O2+0.4 mol SO3
B��3.0 mol SO2+1.0 mol O2+1.0 mol SO3
C��2.0 mol SO2+1.0 mol O2+2.0 mol SO3
D��4.0 mol SO2+1.0 mol O2
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4������� (14��)��2011��11��28����12��9�գ����Ϲ�����仯��ܹ�Լ��17�ε�Լ���������Ϸǵ°��ٿ����������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽���÷�Ӧԭ������������ʵ�飬�����Ϊ1L���ܱ������У�����1mol CO2��3.25 mol H2����һ�������·�����Ӧ���ⶨCO2��CH3OH(g)��H2O (g)��Ũ����ʱ��仯��ͼ��ʾ��
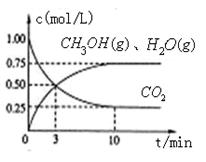
��д���ù�ҵ������ȡ�״��Ļ�ѧ��Ӧ����ʽ������������������
�ڴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v (H2)����?? ��
��
�۸�������CO2��ת����Ϊ��?�����¶Ƚ���ʱCO2��ת���ʱ����÷�Ӧ?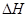 ?�����������������������
?�����������������������
�����д�ʩ����ʹn(CH3OH)/n(CO2)�����������������������
A�������¶�
B�����뵪��
C����ˮ��������ϵ�з���
D���ø���Ч�Ĵ���
 2SO3(g)? ��H=" ��196.6" kJ��mol�D1
2SO3(g)? ��H=" ��196.6" kJ��mol�D1 2NO2(g)? ��H= ��113.0 kJ��mol�D1
2NO2(g)? ��H= ��113.0 kJ��mol�D1 SO3(g) + NO(g) �Ħ�H= ??��
SO3(g) + NO(g) �Ħ�H= ??�� ?CH3OH + H2O��2�֣��� 0.225 ��1�֣�? �� 75%?��1�֣�? < ��1�֣�? �� C��1�֣�
?CH3OH + H2O��2�֣��� 0.225 ��1�֣�? �� 75%?��1�֣�? < ��1�֣�? �� C��1�֣�