��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ������ͼ��ʾ��ת����ϵ��ͼ�и����ʾ�Ϊ�������ʣ�ת�����в���������ʡ�ԡ�
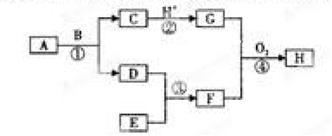
����������C��һ�ֺ�ɫ���Թ��壬F�Ǽ�������ˮ��ˮ��Һ�ʼ��Ե����壬H�Ǻ��ɫ������A��D��E��Ϊ���ʣ���ش��������⣺
��1��д���������ʵĻ�ѧʽ��A�� ��E
��2��д����������H�ķ�������ԭ��Ӧ�����ӷ���ʽ��
��3����120�桢1����ѹ�½�168gA��90gB����1L���ܷ���ƿ�з�����Ӧ�٣�����10min�ﵽƽ�⣬ƽ���D������Ϊ4g������������Բ��ƣ�������D��ʾ10min�ڵ�ƽ����Ӧ����Ϊ �����¶��´˷�Ӧ��ƽ�ⳣ��K= ��B��ת������ ��
�ο��𰸣���1��Fe��1�֣� N2��1�֣�
��2��Fe3++3NH3+H2O==Fe��OH��3��+3NH4+��2�֣�
��3��V(H2)=0.2mol��L-1��min-1��2�֣� K=��2/3��4��2/3��3�֣� 40����3�֣�
���������������֪��AΪFe��BΪH2O��CΪFe3O4��DΪH2��EΪN2��FΪNH3��HΪFe��OH��3��
��2��CΪFe3O4��H+��Ӧ����G�м�����Fe3+�ֺ���Fe2+��������H�ķ�������ԭ��Ӧֻ����Fe3+����Fe��OH��3��
��3����Ӧд���٣�3Fe + 4H2O��g�� = Fe3O4 + 4H2
��ʼ 166g 90g
10min�� 3mol 4g
ת�� 2mol 2mol
��V(H2)=" 2mol/1L/10min" = 0.2mol��L-1��min-1��
ƽ�ⳣ��K=c4(H2)/ c4(H2O) = ��2/3��4��
B��ת����=2mol/5mol=40����
���㣺������ƶϣ���ѧ��Ӧ���ʡ���ѧƽ�ⳣ����ת���ʵļ���
�����Ѷȣ�һ��
2������� ij�¶�ʱ����2L�ܱ���������̬����X��Y��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯�����ʾ��

��1����ϵ�з�����Ӧ�Ļ�ѧ����ʽ��___________________________
��2����ʽ����÷�Ӧ��0-3minʱ���ڲ���Z��ƽ����Ӧ���ʣ�_______________
��3���÷�Ӧ�ﵽƽ��ʱ��Ӧ��X��ת���ʵ���___________________________
��4������÷�Ӧ�Ƿ��ȷ�Ӧ���ı�ʵ���������¶ȣ�ѹǿ���������õ�Z��ʱ��仯�����ߢ٣��ڣ��ۣ���ͼ��ʾ�������ߢ٣��ڣ������ı��ʵ���������ж�������

�� __________________________
�� __________________________
�� __________________________
�ο��𰸣���1��X+2Y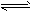 2Z
2Z
��2��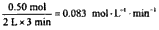
��3��45%
��4���������¶ȣ��÷�ӦΪ���ȷ�Ӧ �ﵽƽ���ʱ�����̣�ƽ��ʱZ��Ũ�ȼ�С
�ڼ���������ﵽƽ���ʱ�����̣�ƽ��ʱZ��Ũ�ȼ�С
������ѹǿ���ﵽƽ���ʱ�����̣�ƽ��ʱZ��Ũ������
���������
�����Ѷȣ�����
3������� ��1���о����仯������������Ҫ���壮
���Ṥҵ�������漰���·�Ӧ��2SO2��g��+O2��g���T2SO3��g������2L�������г���2mol SO2��1mol O2��SO2��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ��T1�¶�ʱ��Ӧ���е�״̬Dʱ��v������______v���棩�����������������=�������¶�ΪT1ʱ����Ӧ��ƽ�ⳣ��K=______������λ����д��������T3�¶�ʱ����ƽ��ʱ��÷�Ӧ�ų�������ΪQ1����ʱ���������м���2mol SO2��1mol O2��ʹ֮���´ﵽƽ�⣬����ַų�����Q2��������˵����ȷ����______��������ĸ��ţ�
a��������ѹǿ����ԭ��������b��Q2һ������Q1
c����ƽ��ʱSO2��ת����һ������80% d��T3ʱ��ƽ�ⳣ������T1ʱ��ƽ�ⳣ��
��2����֪��25��ʱ��Ksp[Mg��OH��2]=5.6��10-12��Ksp��MgF2��=7.4��10-11��25��ʱ����Mg��OH��2������Һ�м���������NH4Cl���壬c��Mg2+��______��������С�䣩���ڵ�Ũ�ȵ�KOH��KF�����Һ�м���ϡMgCl2��Һ���������ɵij�����______��д��ѧʽ����
��3��Al2��SO4��3��Һ��ʾ���ԣ���ԭ����______��д���ӷ���ʽ������ij�ữ��Al2��SO4��3��Һ�м���NaHCO3���壬���ֵ������ǣ��д������������ͬʱ�а�ɫ����������ƽ���ƶ�ԭ������ԭ��______��
��4����������������Һ���������õ�ԭ���ʵ���______��
a��KNO3��Һb��AlCl3��Һc��Al2��SO4��3��Һd������
��5��25��ʱ��pHΪ4���Ȼ����Һ��pHΪ4������Һ�У���ˮ�������H+Ũ��֮��Ϊ______��
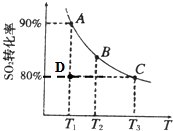
�ο��𰸣���1���¶�T1ʱ��ƽ���ΪA��D���������ת����С��A����Ӧ����������У�V����V�棬
ת���Ķ�����������ʵ�����2mol��90%=1.8mol
2SO2��g��+O2��g�� �T2SO3��g��
��ʼŨ�� 1mol/L 0.5mol/L 0
ת��Ũ�� 0.9mol/L 0.45mol/L 0.9mol/L
ƽ��Ũ�� 0.1mol/L 0.05mol/L 0.9mol/L K=[SO3]2[SO2]2[O2]=1620L/mol���ʴ�Ϊ��1620L/mol��
T3ʱ�������������м���2mol SO2��1mol O2����ƽ�ⲻ�ƶ�ѹǿ��Ϊԭ����2�������Ǹ÷�Ӧǰ������ϵ����ͬ������2mol SO2��1mol O2���൱����ѹǿƽ�����������ƶ�����a����ƽ��ʱ��÷�Ӧ�ų�������ΪQ1����ʱ���������м���2mol SO2��1mol O2���൱��ԭ������ѹ��ƽ��������Ӧ�����ƶ������Էų�����������Q2��Q1����b����ƽ��������Ӧ�����ƶ�����Ӧ���ת��������c��ȷ������ӦΪ���ȷ�Ӧ�������¶�K��С����d����ѡc��
�ʴ�Ϊ������1620L/mol��c��
��2������Mg��OH��2�����ܽ�ƽ��Mg��OH��2 ��s��Mg2+��aq��+2OH- ��aq���������Ȼ�泥�NH4+����������ʹƽ�����ƣ�þ����Ũ�����ʴ�Ϊ������
������þ�����þ���ṹ��ͬ��Ksp[Mg��OH��2]=5.6��10-12��Ksp��MgF2��=7.4��10-11������������þ�ܽ�ȸ�С���ȳ������ʴ�Ϊ��Mg��OH��2��
�ʴ�Ϊ������Mg��OH��2��������Һ�����ԣ�
��3��Al2��SO4��3��ǿ�������Σ�������ˮAl3++3H2O Al��OH��3+3H+������Һ�����ԣ�����̼�����ƺ�̼��������ӷ���ˮHCO3-+H2O H2CO3+OH-��ˮ�����ɵ�������������������ˮ�����ɵ������ӷ�Ӧ��˫����ٽ�������˫ˮ�⣬�����д������������ͬʱ�а�ɫ������
�ʴ�Ϊ��Al3++3H2O?Al��OH��3+3H+�������Ӻ�̼��������ӷ���˫ˮ�⣬��ٽ���ʹˮ��ƽ������������У�
��4��a���������Һ�в�����ˮ�����ʣ�����ˮ��õ�����ع��壬��a��ȷ��
b��AlCl3ˮ�����������������Ȼ��⣬�����Ȼ����ӷ����ٽ�ˮ��ƽ�������ƶ���������������Һ�õ����������������壬��b����
c��Al2��SO4��3��Ȼˮ����������������ѻӷ����ᣬ������Һ�õ���Ȼ�����������壬��c��ȷ��
d�������ǻӷ����ᣬ���ȴٽ��Ȼ���Ļӷ������ɺ�ò���ԭ���ʣ���d����
��ѡac��
��5��pH=4���Ȼ����Һ�У�ˮ�����������Ũ�ȣ�C��H+��=10-4mol/L��pH=4��������Һ�У�ˮ����������ӵ�Ũ�ȣ�C��H+����=10-10mol/L��C��H+����C��H+����=106���� 106��1�����ʴ�Ϊ��106���� 106��1����
���������
�����Ѷȣ�һ��
4��ѡ���� ��2X��g��?2Y��g��+Z��g����H��0?�Ŀ��淴Ӧ��ϵ�У��ڲ�ͬ�¶ȣ�T1��T2���£�������Z�ڷ�Ӧ������еİٷֺ����뷴Ӧʱ�䣨t���Ĺ�ϵ������ͼʾ��������ȷ���ǣ�������
A��

B��

C��
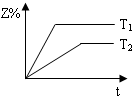
D��

�ο��𰸣�B
���������
�����Ѷȣ���
5������� �״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϣ���ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO��g��+2H2��g��?CH3OH��g����ͼl��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4molH2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯ͼ��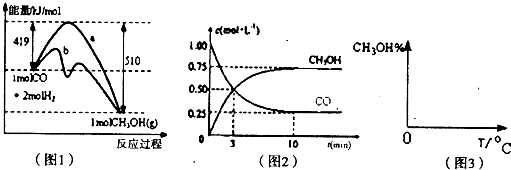
��ش��������⣺
��1���ڡ�ͼ1���У�����______���a����b������ʾʹ���˴������÷�Ӧ����______������ȡ����ȡ�����Ӧ��
��2�����ݡ�ͼ2���жϣ�����˵����ȷ����______
a����ʼ�����COΪ1mol
b������COŨ�ȣ���ʹH2��ת��������
c��������ѹǿ�㶨ʱ����Ӧ�Ѵ�ƽ��״̬
d�������¶Ⱥ��ܱ������ݻ����䣬�ٳ���1molCO��2molH2���ٴδﵽƽ��ʱn��CH3OH��/n��CO��������
��3���ӷ�Ӧ��ʼ������ƽ�⣬v��H2��=______�����¶���CO��g��+2H2��g��?CH3OH��g���Ļ�ѧƽ�ⳣ��Ϊ______�������������������䣬����Ӧ��ϵ���£���÷�Ӧ�Ļ�ѧƽ�ⳣ����______�����������С�����䡱����
��4�����ڡ�ͼ3���л���ƽ��ʱ�״������ٷֺ����������꣩���¶ȣ������꣩�仯�����ߣ�Ҫ��ѹǿ��ͬ��2�����ߣ��������ϱ��P1��P2����P1��P2����
�ο��𰸣���1������������ɽ��ͷ�Ӧ�Ļ�ܣ���ͼ���֪b��ܽϵͣ�Ӧ�����������Ӧ������������������������������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ��b�����ȣ�
��2��A��CO����ʼŨ��Ϊ1moL/L�����Ϊ2L������ʼ�����COΪ2mol����a����
B������COŨ�ȣ�ƽ�����������ƶ���H2��ת��������b��ȷ��
C�����ڷ�Ӧǰ�������������ȣ���������ѹǿ�㶨ʱ����Ӧ�Ѵﵽƽ��״̬����c��ȷ��
D�������¶Ⱥ��ܱ������ݻ����䣬�ٳ���1mol CO��2mol H2���൱����ԭ���Ļ�������С�����ѹǿ����ƽ��������Ӧ�����ƶ�����ƽ��ʱn(CH3OH)n(CO)������d��ȷ��
�ʴ�Ϊ��bcd��
��3���ӷ�Ӧ��ʼ������ƽ�⣬v��CO��=1mol/L-0.25mol/L10min=0.075moL/��L?min����
��v��H2��=2v��CO��=0.15moL/��L?min����
ƽ��ʱ��c��CO��=0.25mol/L��c��CH3OH��=0.75mol/L��
������n��CO��=0.75mol/L��2L=1.5mol�����ĵ�n��H2��=3mol��
ƽ��ʱc��H2��=4mol-3mol2L=0.5mol/L��
k=0.750.25��0��52=12��
�ʴ�Ϊ��0.15moL/��L?min����12��
��4������ѹǿ��ƽ��������Ӧ�����ƶ�����״��İٷֺ��������¶����ߣ�ƽ�����淴Ӧ�����ƶ����״��İٷֺ������ͣ���ͼ���Ϊ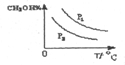 ��
��
�ʴ�Ϊ�� ��
��
���������
�����Ѷȣ�һ��