��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����Ȼ��Ϊԭ�Ͼ��ϳ���(CO��H2)�ƻ�ѧƷ��Ŀǰ��Ȼ��ת�����õ���������·�ߣ��Լ���IJ�������Ϊ�����Ʊ�����(CH3OCH3)�ͼ״��Ĺ�ҵ��������
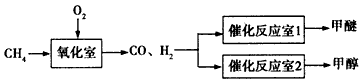
(1)����IJ���������Ӧ���£�2CH4(g) +O2(g)=2CO(g) +4H2(g) ��H=-71.2 kJ/mol
���о���Ϊ���鲿�������Ļ���Ϊ��
��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H1=- 890.3 kJ/mol
��CH4(g)+CO2(g)=2CO(g)+2H2(g) ��H2
��CH4(g)+H2O(g)=CO(g) +3H2(g) ��H3=+250.3 kJ/mol ���H2=____��
(2)����Ӧ��1�кϳɼ��ѵķ�ӦΪ��2CO(g)+4H2(g) CH3OCH3(g)+H2O(g)���÷�ӦΪ�Է���Ӧ����÷�Ӧ�ġ�H___________���<������>����=����0��
CH3OCH3(g)+H2O(g)���÷�ӦΪ�Է���Ӧ����÷�Ӧ�ġ�H___________���<������>����=����0��
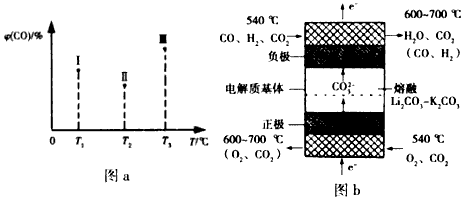
(3)����Ӧ��2�з������·�Ӧ��CO(g) +2H2(g)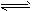 CH3OH(g) ��H<0�����ݻ���ΪVL��I����������ͬ�ܱ������зֱ����amol CO��2a mol H2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�tminʱCO�����������ͼa��ʾ����ʱI��������������һ���ﵽ��ѧƽ��״̬����___�����ﵽ��ѧƽ��״̬ʱ��COת������͵���___��
CH3OH(g) ��H<0�����ݻ���ΪVL��I����������ͬ�ܱ������зֱ����amol CO��2a mol H2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�tminʱCO�����������ͼa��ʾ����ʱI��������������һ���ﵽ��ѧƽ��״̬����___�����ﵽ��ѧƽ��״̬ʱ��COת������͵���___��
(4)��ͼbΪ����̼����ȼ�ϵ�صĹ���ԭ��ʾ��ͼ������̼����ȼ�ϵ�ص�������Ӧʽ�ɱ�ʾΪ��____��
�ο��𰸣�(1)+247.3 kJ/mol
(2)<
(3)��
(4)O2+4e-+2CO2=2CO32-
���������
�����Ѷȣ�һ��
2��ѡ���� ��30%KOH��ҺΪ�������Һ������ȼ�ϵ�أ��缫��Ӧ���£�2H2+4OH--4e-=4H2OO2+2H2O+4e-=4OH-�ݴ��жϣ�����˵���д�����ǣ�������
A��H2�ڸ�������������Ӧ
B������ʱ���ܷ�ӦΪ��2H2+O2=2H2O
C��ȼ�ϵ�ص�����ת���ʿɴ�100%
D����������Ⱦ�����ڻ����Ѻõ��
�ο��𰸣�A���ɵ缫��Ӧʽ��֪��ͨ��������һ��Ϊ��صĸ���������������Ӧ����A��ȷ��
B������ܷ�Ӧ��������������ȼ�յĻ�ѧ����ʽһ�£�����ʱ���ܷ�ӦΪ2H2+O2�T2H2O����B��ȷ��
C������ȼ�ϵ���ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�����������ܵ��������ͷţ�����ת���ʲ����100%����C����
D������ȼ�ϵ�ز�����ˮ���Ի�������Ⱦ��������ת���ʸߣ���D��ȷ��
��ѡC��
���������
�����Ѷȣ���
3������� ��ͼ�ס����ǵ绯ѧʵ��װ�á�
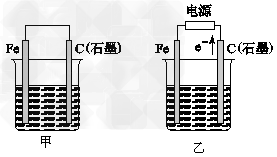
(1)���ס������ձ��о�ʢ��NaCl��Һ��
�ټ���ʯī���ϵĵ缫��ӦʽΪ_______________________________��
�������ܷ�Ӧ�����ӷ���ʽΪ____________________________��
�۽�ʪ��ĵ���KI��ֽ�������ձ��Ϸ���������ֽ�ȱ�������ɫ��������Ϊ������Cl2������I-���ɵ�I2������Ӧ��Cl2��I2�����ʵ���֮��Ϊ5��1�������������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ_________________��
(2)���ס������ձ��о�ʢ��CuSO4��Һ��
�ټ��������ϵĵ缫��ӦʽΪ_____________________________��
�������ʼʱ����ʢ��200?mL?pH��5��CuSO4��Һ(25?��)��һ��ʱ�����Һ��pH��Ϊ1����Ҫʹ��Һ�ָ������ǰ��״̬��������Һ�м���__________(��д���ʵĻ�ѧʽ)________g��
�ο��𰸣�(1)��O2��2H2O��4e��===4OH������2Cl����2H2O 2OH����H2����Cl2������5Cl2��I2��6H2O===10HCl��2HIO3
2OH����H2����Cl2������5Cl2��I2��6H2O===10HCl��2HIO3
(2)��Fe��2e����Fe2������CuO(��CuCO3)��0.8(��1.24)
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����
A����300�桢70MPa���ɶ�����̼�������ϳ��Ҵ��ѳ�Ϊ��ʵ��2CO2(g)+6H2(g)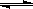 CH3CH2OH(g)+3H2O(g)������Ʋ�÷�Ӧ�����ȷ�Ӧ��
CH3CH2OH(g)+3H2O(g)������Ʋ�÷�Ӧ�����ȷ�Ӧ��
B����¯�г�����CaSO4����Na2CO3��Һ���ݺ��������ܽ�ȥ��
C�������£���Ũ��Ϊ0.1mol.L?1HF��Һ��ˮϡ�ͣ������ƽ�ⳣ����c(H+)/c(HF)������
D����⾫��ͭʱ���������г����н���������п�ȡ�
�ο��𰸣�B
�����������Ӧ�Ƿ��ȷ�Ӧ���������ȷ�Ӧ���뷴Ӧ�����ء�ֻ�뷴Ӧ�������������������Դ�С�й�ϵ��A����ȷ��B��ȷ�����ų���ת�����ص㡣ϡ�������ڵ��룬������ϡ�����У������ӵ����ʵ��������ӵģ�HF���ӵĸ����Ǽ�С�ģ����c(H+)/c(HF)������ģ�C����ȷ��п�Ļ�����ǿ��ͭ�ģ������������в����ܺ���п��D����ȷ����ѡB��
�����Ѷȣ�һ��
5��ʵ���� ��15�֣���������������Ӧ����A��NaOH + HCl =" NaCl" + H2O
��B��2FeCl3 + Cu = 2FeCl2 + CuCl2
��1����������Ӧ���ʣ��ж��ܷ���Ƴ�ԭ���(��ܡ����ܡ�)��A�� ��B�� ��
��2�����(A��B)���ܣ�˵����ԭ�� ��
��3�����(A��B)���ԣ���д�������������ϼ���缫��Ӧʽ���������Һ
������ �� ��
������ �� ��
�������Һ�� ��
�ο��𰸣���1����A�����ܣ�1�֣� ��B���� ��1�֣�
��2��A��Ӧ�Ƿ�������ԭ��Ӧ ��2�֣�
��3��������Cu��2�֣���Cu-2e-=Cu2+��2�֣�
������ʯī��2�֣�������������ɣ���2Fe3++2e-=2Fe2+��3�֣�
�������Һ���Ȼ�����Һ��2�֣�
�����������1�����ڵ��ӵĶ����˶��γɵ���������ֻ��������ԭ��Ӧ������Ƴ�ԭ��أ�A���кͷ�Ӧ����ʾ������ԭ��Ӧ��������Ƴ��е���B��������ԭ��Ӧ�����ԡ�
��3������B���ܷ�Ӧʽ��֪��ͭʧȥ���ӣ�����ԭ����������ԭ��صĸ�������������ֻ�ý���������ͭ���ɡ��Ȼ����õ����ӣ���˵������Һ���Ȼ�����
�����Ѷȣ�һ��