微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组热化学方程式程中,△H的绝对值前者大于后者的是
[? ]
①C(s)+O2(g)=CO2(g);△H1? C(s)+1/2O2(g)=CO(g);△H2
②S(s)+O2(g)=SO2(g);△H3? S(g)+O2(g)=SO2(g);△H4
③H2(g)+1/2O2(g)=H2O(l)△H5? 2 H2(g)+O2(g)=2H2O(l);△H6
A.①
B.②
C.② ③
D.①②③
参考答案:A
本题解析:
本题难度:简单
2、填空题 (16分)以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
C(s)+H2O(g)  CO(g)+H2(g)?ΔH=+131.3 kJ?mol-1,
CO(g)+H2(g)?ΔH=+131.3 kJ?mol-1,
①该反应在常温下??自发进行(填“能”与“不能”);
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有??
Ⅰ混合气体的密度;?Ⅱ容器内气体的压强;
Ⅲ混合气体的总物质的量;?ⅣCO物质的量浓度
A.只有Ⅳ? B.只有Ⅰ和Ⅳ? C.只有Ⅱ和Ⅲ? D.Ⅰ、Ⅲ和Ⅳ?
(2)水煤气再进一步反应可制取氢气。反应为H2O(g)+CO(g) H2(g)+CO2(g),某温度下该反应的平衡常数K= 4/9。该温度下在甲、乙、丙三个恒容密闭容器中,只投入H2(g)和CO2(g),其起始浓度如下表所示。下列判断不正确的是??。
H2(g)+CO2(g),某温度下该反应的平衡常数K= 4/9。该温度下在甲、乙、丙三个恒容密闭容器中,只投入H2(g)和CO2(g),其起始浓度如下表所示。下列判断不正确的是??。
起始浓度
| 甲
| 乙
| 丙
|
c(H2)/mol/L
| 0.010
| 0.020
| 0.020
|
c(CO2)/mol/L
| 0.010
| 0.010
| 0.020
|
?
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.平衡时,乙中CO2的转化率大于60%
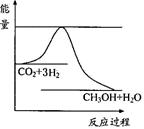
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ,右图表示该反应进行过程中能量(单位为kJ?mol―1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2反应
CH3OH(g)+H2O(g) ,右图表示该反应进行过程中能量(单位为kJ?mol―1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2反应
①下列措施中能使c (CH3OH)增大的是??。
A.升高温度?
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来?
D.再充入1mol CO2和3mol H2
②在温度T1时,当反应达到平衡时,测得n(H2) =" 2.4" mol;其它条件不变,在温度T2时,当反应达到平衡时,测得n(CO2) =" 0.82" mol,则T2 ?T1。(填“>”、“<”或“=”),
(4)在一定条件下科学家从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇。CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol。
①写出工业上以CO2、H2合成CH3OH和液态水的热化学方程式:??;
②该转化的积极意义是??;
③有人提出,可以设计反应CO2=C+O2(△H>0、△S<0)来消除CO2对环境的影响。请你判断是否可行并说出理由:??
参考答案:(1)?①不能?②? D?(2)C? (3) ①?CD?② >
(4)①CO2(g)+3H2(g)→CH3OH(l)+H2O(l)?△H=-131.9kJ/mol
②可降低温室效应和弥补资源短缺
③不可行,该反应是一个焓增、熵减的反应,所以不能自发进行
本题解析:(1)反应是体积增大的,吸热放热可逆反应,所以在常温下不能自发进行。因为恒温,在容积可变的密闭容器中进行,所以I、Ⅱ、Ⅲ均不能说明。只有当CO物质的量浓度不再变化时可以说明。
(2)反应开始时丙中浓度最大,甲中浓度最小,反应速率丙最快,甲最慢。因为反应前后体积不变,而甲和丙中反应物的浓度之比相同,所以其平衡是等效的,所以C不正确。根据方程式可知? H2(g)+CO2(g)  ?H2O(g)+CO(g)
?H2O(g)+CO(g)
起始量(mol)? 0.010? 0.010? 0? 0
转化量(mol)? x? x? x? x
平衡量(mol)? 0.010-x? 0.010-x? x? x
所以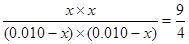 ,解得x=0.006,即转化率是60%。乙中最大氢气的浓度,可以提高二氧化碳的转化率。
,解得x=0.006,即转化率是60%。乙中最大氢气的浓度,可以提高二氧化碳的转化率。
(3)根据图像可知该反应是放热反应,升高温度平衡向逆反应方向移动。充入He(g),使体系压强增大,则原体系的物质的浓度将减小,平衡向逆反应方向移动。降低生成物水的浓度,平衡向正反应方向移动,c (CH3OH)增大。若再充入1mol CO2和3mol H2,相当于增大体系的压强,平衡向正反应方向移动,c (CH3OH)增大。在温度T2时,当反应达到平衡时,测得n(CO2) =" 0.82" mol,则此时n(H2) ="2.46" mol.因为反应放热,温度越高氢气的物质的量越多,所以T2大于T1。
(4)根据盖斯定律和燃烧热的热化学方程式可以得到CO2、H2合成CH3OH和液态水的热化学方程式。在反应中消耗二氧化碳,所以可以降低温室效应,同时生成甲醇可以弥补资源短缺。因为△H>0、△S<0,所以该反应不能自发进行。
本题难度:一般
3、选择题 下列推论正确的是
[? ]
A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g) △H2;则:△H1>△H2
B.C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,则:由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ/mol,则:含20gNaOH的溶液与稀盐酸完全反应,放出的热量为28.7kJ
D.CaCO3(s)=CaO(s)+CO2(g) △H>0,△S>0,则:该反应任何温度下都能自发进行
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列推论正确的是( )
A.S(g)+O2(g)=SO2(g)△H=a;S(s)+O2(g)=SO2(g)△H=b;则a>b
B.C(石墨,s)=C(金刚石,s);△H=+1.9kJ/mol,则可判定金刚石比石墨稳定
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ/mol,则含20gNaOH的稀溶液与稀盐酸完全反应,放出的热量为28.7kJ
D.CaCO3(s)=CaO(s)+CO2(g)△H>0,则该反应任何温度下都能自发进行
参考答案:A.S(s)→S(g)为吸热过程,S的燃烧为放热过程,△H<0,固体硫燃烧放出的热量较少,则a<b,故A错误;
B.由热化学方程式可知,石墨总能量小于金刚石,则石墨较稳定,故B错误;
C.n(NaOH)=0.5mol,放出的热量为0.5mol×57.4kJ/mol=28.7kJ,故C正确;
D.CaCO3(s)=CaO(s)+CO2(g)△H>0,△S>0,由△G=△H-T?△S可知,当在较高温度下反应才能自发进行,故D错误.
故选C.
本题解析:
本题难度:一般
5、填空题 (6分)依据叙述,写出下列反应的热化学方程式。
①在25℃、101 kPa下,32g甲醇(CH3OH)的燃烧放出的热量为725.8kJ,则表示甲醇燃烧热的热化学方程式为(已知常温下甲醇为液态)
______________________________________________________________
②1.00 L 1.00 mol・L-1H2SO4溶液与2.00 L 1.00 mol・L-1 NaOH溶液完全反
应,放出114.6 kJ热量,表示其中和热的热化学方程式为
_________________________________________________________________。
参考答案:①CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(l) ΔH=-725.8 kJ・mol-1
②1/2H2SO4(aq)+NaOH(aq)==="1/2" Na2SO4(aq)+H2O(l)?ΔH=-57.3 kJ・mol-1
本题解析:(1)燃烧热是在一定条件下1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,因此在表示燃烧热的热化学方程式中可燃物前的计量数一定是1。
(2)中和热是在一定条件下的稀溶液中酸和碱反应生成1mol水时所放出的热量,所以在表示中和热的热化学方程式中生成物水前的计量数一定是1。
本题难度:一般