微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 V2O3和V2O5按不同的物质的量之比 混合,可按计量完全反应.今欲制备V8O17,则V2O3和V2O5的物质的量之比应为(?)
混合,可按计量完全反应.今欲制备V8O17,则V2O3和V2O5的物质的量之比应为(?)
A.1∶2
B.2∶1
C.3∶5
D.5∶3
参考答案:C
本题解析:(待定计量法)设化学反应中V2O3和V2O5的化学计量数分别是x和y.则:
x V2O3+y V2O5====V8O17
根据V原子守恒得:2x+2y=8
根据O原子守恒得:3x+5y=17
解得:x∶y=3∶5
本题难度:简单
2、选择题 下列各组物质中,所含分子数相同的是
[? ]
A.10 g H2和10 g O2
B.5.6LN2和11 g CO2
C.9 g H2O和0.5 mol Br2
D.224 mLH2(标准状况)和0.1molN2
参考答案:C
本题解析:
本题难度:简单
3、选择题 NA代表阿伏伽德罗常数,下列叙述正确的是(?)
A.在20℃、1.01×105Pa时,2.8gC2H4和CO的混合气体中含气体分子数小于0.1NA
B.23g金属钠与足量氧气反应,生成Na2O2和Na2O的混合物,钠失去NA个电子
C.7.8Na2S和Na2O2的固体混合物中含有的阴离子数大于0.1NA
D.0.5mol的甲基(―CH3)所含电子数为5NA
参考答案:B
本题解析:A,C2H4和CO的相对分子质量都是28,则混合气体的平均相对分子质量是28,所以2.8gC2H4和CO的混合气体是0.1mol,气体分子数应该等于0.1NA。B,23g金属钠反应,都是生成+1价的钠离子,所以是失去NA个电子。C,Na2S和Na2O2中都是含有一个阴离子,而且两微粒相对分子质量相等,都是78,所以7.8Na2S和Na2O2的固体混合物是0.1mol, 阴离子数等于0.1NA?D,0.5mol的甲基(―CH3)所含电子数为4.5NA
本题难度:一般
4、选择题
A.28 g氮气所含有的原子数目为N
B.4 g金属钙变成钙离子时失去的电子数目为0.1N
C.1 mol甲烷的质量与N个甲烷分子的质量之和相等
D.标准状况下,22.4 L甲烷和乙炔混合物所含的分子数为N
参考答案:CD
本题解析:此题考查的是物质的量、质量和粒子数目三者之间的关系。28 g N2的物质的量为1 mol,含氮原子2N个;4 g钙为0.1 mol,反应中失去0.2N个电子。
本题难度:简单
5、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是(?)。
A.1 mol・L-1 NaCl溶液含有NA个Na+
B.1 mol Cu和足量稀硝酸反应产生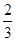 NA个NO分子
NA个NO分子
C.1 L 0.1 mol・L-1氨水含有0.1NA个OH-
D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
参考答案:B
本题解析:由于没有提供1 mol・L-1 NaCl溶液的体积,则溶液所含Na+数目无法确定,A项错误;根据Cu与稀硝酸的反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则反应生成的n(NO)=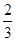 n(Cu),其分子数目为
n(Cu),其分子数目为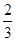 NA,B项正确;C项氨水中的NH3・H2O为弱电解质,不能完全电离,1 L 0.1 mol・L-1氨水中OH-数目小于0.1NA;D项中Fe2+被氧化成Fe3+,1 mol Fe2+转移1 mol电子,即NA个电子。
NA,B项正确;C项氨水中的NH3・H2O为弱电解质,不能完全电离,1 L 0.1 mol・L-1氨水中OH-数目小于0.1NA;D项中Fe2+被氧化成Fe3+,1 mol Fe2+转移1 mol电子,即NA个电子。
本题难度:一般