微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (13分)试根据上表填空:
A
| ?
| ?
|
?
| B
| ?
| ?
| C
| D
| E
| F
| ?
|
G
| H
| I
| J
| ?
| L
| K
| M
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| N
| ?
| ?
| Q
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
| | | | | | | | | | | | | | | | | |
|
(1)请写出元素Q的基态原子电子排布式?;元素N在周期表中的位置?周期?族。
(2)基态D原子核外有?个未成对电子;D2分子中分别有?个,?个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式??。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是?(填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是?(填化学式),它是由_?键(填“极性”或“非极性”,下同)构成的?分子。
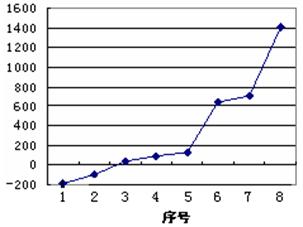
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是?(填元素符号);其中气态氢化物稳定性最强的元素是?(填下图中的序号)。
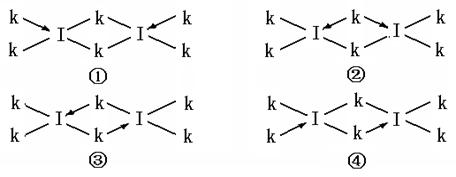
(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。
(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式?;最后生成配离子的结构式为?。
参考答案:(1)(2分)1s22s22p63s23p63d104s1;?(2分)第4周期? VIII族。
(2)(3分) 3;?1?,? 2。(3)(2分)?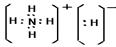 。
。
(4)(4分)? SO2;? SO3?;?极性;?非极性
(5)(2分) Si 、 2 ;(6)(2分) ③ 。
(7)(6分)Cu2++2NH3?H2O= Cu(OH)2↓+2NH4+?
Cu(OH)2 +4NH3 =〔Cu(NH3)4〕2+? + 2OH-。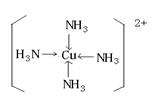
本题解析:(1)Q是铜,根据构造原理可知,电子排布式为1s22s22p63s23p63d104s1。N是铁元素,位于第4周期VIII族。
(2)D是氮元素,最外层有3个未成对电子。氮气是由三键构成的,而三键是由2个π键和1个σ键构成。
(3)化合物DA5是氢化铵,属于离子化合物。电子式为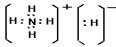 。
。
(4)CE2、CL2、BK2、LE2四种物质分别是CO2、CS2、BeCl2、SO2,其中前三个是直线型化合物,SO2是V形结构。DA3、DF3、DK3、LE3四种物质分别是NH3、NF3、NF3、SO3。其中SO3是平面三角形,是由极性键形成的非极性分子,其余都是三角锥形。
(5)硅是原子晶体,熔点最高。氯元素的非金属性最强,氯化氢最稳定。单质氯的沸点之比Ar的高,是由是2。
(6)氯元素最外层含有孤对电子,能和铝元素形成配位键,所以正确的答案是③。
(7)硫酸铜和氨水发生复分解反应,生成氢氧化铜沉淀。当氨水过量时,由于氨气能和铜离子形成配位键,所以沉淀会溶解,生成配合物。反应式为Cu2++2NH3?H2O= Cu(OH)2↓+2NH4+、Cu(OH)2 +4NH3 =〔Cu(NH3)4〕2+? + 2OH-。
本题难度:一般
2、选择题 短周期元素X,Y,Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y,Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是
[? ]
A、Z的氢化物的水溶液在空气中存放易变质
B、X的氢化物没有还原性
C、Y的氧化物是共价化合物,其水化物显两性
D、X和Z的最高价氧化物对应的水化物都是具有强氧化性的酸
参考答案:A
本题解析:
本题难度:简单
3、选择题 只有在化合物中才能存在的化学键是
[? ]
A.离子键
B.共价键
C.金属键
D.极性键
参考答案:AD
本题解析:
本题难度:简单
4、选择题 在空气中不易变质的是
A.Na2SO3
B.NaHSO4
C.亚硫酸
D.氢硫酸
参考答案:B
本题解析:略
本题难度:简单
5、选择题 下列分子或离子属等电子体的是
A.CH4和NH3
B.NO3-和CO32-
C.H3O+ 和PCl3
D.CS2和SO2
参考答案:B
本题解析:原子总数和价电子总数分别都相同的分子或离子称为等电子体,等电子体间结构和性质相似(等电子原理)。A、甲烷分子中含有5个原子,氨气分子中含有4个原子,所以不是等电子体,故A错误;B、硝酸根离子和碳酸根离子都含有4个原子,其价电子数都是24,所以是等电子体,故B正确;C、H3O+和PCl3都含有4个原子,水合氢离子价电子数是8,PCl3价电子数是26,所以不是等电子体,故C错误;D、CS2和SO2分子中都含有3个原子,CS2中价电子数是16,SO2中价电子数是18,所以不是等电子体,故D错误,答案选B。
本题难度:一般