| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ�ؿ�֪ʶ�㡶����ľ���������������ռ�������ǿ����ϰ��2017�����°棩(��)
��2������ҺC���CuSO4��5H2O����Ҫ��������Ũ����?�����������˵Ȳ��������ձ���©���⣬���˲��������õ���һ�����������������ڴ˲����е���Ҫ������������������ ��3���Ʊ�CaCO3ʱ��������Ӧ�Ļ�ѧ����ʽ��?������������������������������?����ʵ��������а����ݳ�����ѡ������װ���е�?����?������ţ�װ�����հ����� ���ձ��е�Һ�嶼Ϊˮ�� 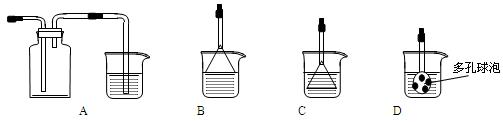 ��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�������100 mL 0.1 mol�MLKMnO4����Һ�����Ƹ���Һʱ�����ձ�������������ͷ�ι��⣬�����һ�ֲ���������?����������?�������ò��������м�����ˮ���ӽ��̶���1��2cmʱ��Ӧ�������������������μ�����ˮ����Һ�İ�Һ��������̶�����ƽ�� �ο��𰸣���ÿ��2�֣���16�֣� ����������� �����Ѷȣ�һ�� 2��ѡ���� ���������У���������ˮ���ռ����ǣ�?�� �ο��𰸣�C �������������ˮ���ռ�����Ҫ�����岻����ˮ��Ӧ��������ˮ��NO2��ˮ��Ӧ���������һ���������ʲ�������ˮ���ռ��� �����Ѷȣ��� 3��ʵ���� ������ʵ��װ����ͼ�� �ο��𰸣�(1)��A�з�������ˮ��ʹˮ��ս�û����©���¶ˣ�������a������ƿB�ײ��Լ��ȣ�����A©������ˮ����������E�е��ܿ��������ݳ�����ʾװ�ò�©���� ��������������ۺϿ�����ʵ��װ�������Եļ�顢�������ȵļ��鼰NH3�ĺϳɵ�֪ʶ�� �����Ѷȣ�һ�� 4������� п������һ�ְ�ɫ���ϡ���ҵ������ZnSO4��BaS��Һ��϶��ɣ�BaS+ZnSO4=ZnS��+BaSO4������������¹�ҵ�������̻ش��й����⡣ |

�ο��𰸣�����16�֣�
��1����4�֣�SiO2��2�֣�? B��2�֣�
��2����3�֣�Fe(OH)3��Cu(OH)2��2�֣�?�٣�1�֣�
��3����4�֣�OH��+CO2= HCO3����2�֣���ZnO22��+ 2CO2 + 2H2O = Zn(OH)2�� + 2HCO3����2�֣�
��4����3�֣�BaSO4(s) + 4C(s) =" BaS(s)" + 4CO(g)?��H =" +571.2" kJ?mol��1
��5����2�֣�����������BaS��Һ��ϻ�����ж���H2S������Ⱦ������1�֣�������п���IJ��ʻή�ͣ�1�֣�
�����������1��ZnCO3��FeCO3��Cu2(OH)2CO3������������5mol/LH2SO4��Һ�����ϸ��ֽⷴӦ����������������ZnSO4��FeSO4��CuSO4��CO2���塢H2O����SiO2���������ᣬ��������֮����������1�Ļ�ѧʽΪSiO2����Һ1����Ҫ�ɷ���ZnSO4��FeSO4��CuSO4��H2O�����������Cl2������Fe2+�����������µ����ʣ�Cl����Cl2�����ҹ����������ж�����A����H2O2������Fe2+����ԭ������H2O���������������ʣ��ҹ���H2O2�����ֽ�Ϊˮ����������B��ȷ��KMnO4������Fe2+�����ǻ������µ����ʣ�K+��Mn2+��KMnO4������C����ŨHNO3������Fe2+����ԭ�������ж���NO2�����������µ����ʣ�NO3����HNO3������D����2�������������������Һ����Ҫ�ɷ���ZnSO4��Fe2(SO4)3��CuSO4�����������NaOH��Һ��Ӧ�����������֪��Һ2����Ҫ�ɷ���Na2ZnO2��NaOH������2����Ҫ�ɷ���Fe(OH)3��Cu(OH)2��������е�CO2�������Բ���������Ӧ�ų������壬���Խ��ܼ��ţ���3��ƫ��������Һͨ�����CO2������������������������ɴ��ƶϲ���ܷ����ķ�ӦΪNa2ZnO2��NaOH��Һ�ֱ���CO2����ķ�Ӧ��NaOH+CO2=NaHCO3��Na2ZnO2+2H2O+2CO2=Zn(OH)2��+2NaHCO3��������3ΪZn(OH)2����Һ3����Ҫ�ɷ�ΪNaHCO3����4�����ݸ�˹���ɣ��ɢڡ�4+�ۣ��ٿ���ԼȥBa(s)��S(s)��2O2(g)���õ����Ȼ�ѧ����ʽΪ��BaSO4(s) + 4C(s) =" BaS(s)" + 4CO(g)?��H =" +571.2" kJ?mol��1����5���������ΪZn(OH)2�����������кͷ�Ӧ��������Һ����Ҫ�ɷ�ΪZnSO4��H2SO4��ZnSO4��H2SO4��Һ��BaS(s)���ʱ����������ȡп���ף����ҹ�����H2SO4������BaS(s)�������ֽⷴӦ�������ж���H2S���壬�ȵ��¿�����Ⱦ���ּ���п���IJ�����
�����Ѷȣ�һ��
5��ʵ���� ��12�֣�NaClO2�����ޡ��顢ճ����ά��֯���Ư�ס�ʵ�����Ʊ�NaClO2��װ������ͼ��ʾ��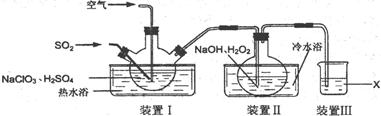
(1)װ��I�����¶���35~55�棬ͨ��SO2��NaClO3��ԭΪClO2���е㣺11�棩����Ӧ������ͨ�������Ŀ�������Ŀ����???��
(2)װ�â��з�Ӧ����NaClO2�Ļ�ѧ����ʽΪ???����Ӧ�����Һ�������ӳ���ClO2����ClO3����Cl����ClO����OH������ܺ��е�һ����������??����������ӵķ�����??
(3)��֪��NaClO2������Һ���¶ȵ���38��ʱ����������NaClO2��3H2O���¶ȸ���38��ʱ����������NaClO2���¶ȸ���60��ʱNaClO2�ֽ�����NaClO3��NaCl���벹���װ�â�Ӧ�����Һ�л��NaClO2����IJ������衣
�ټ�ѹ��55�������ᾧ����??����??����??���õ���Ʒ��
(4)װ�â����Լ�XΪ??��
�ο��𰸣�(1)��ClO2���뵽װ�â���з�Ӧ��2�֣�
(2)2NaOH+2ClO2+H2O2��2NaClO2+2H2O+O2(2��)
SO42����1�֣�?ȡ������Ӧ�����Һ���ȼ����������ᣬ�ټ�BaCl2��Һ����������ɫ��������˵������SO42����2�֣�
(3)�ڳ��ȹ��ˣ�1�֣�����38��~60"����ˮϴ�ӣ�1�֣��ܵ���60"����1�֣�
(4)NaOH��Һ�������𰸾��ɣ���2�֣�
�����������1����Ϊװ��I������ClO2��Ϊ�����ԭ�ϵ������ʣ���Ҫ���ÿ��������ɵ�ClO2���뵽װ�â���з�Ӧ��
��2��ClO2���������ԣ��ɽ�˫��ˮ����������������������ԭ����NaClO2������ʽΪ2NaOH+2ClO2+H2O2��2NaClO2+2H2O+O2�����ڽ���װ�â���������ж����������壬�������������������ᡣ����SO42��һ���������ữ�ļ�BaCl2��Һ��
��3������������Ϣ��֪��Ҫ��õ�NaClO2���壬�ؼ��ǿ����¶ȡ��¶�̫��̫�;���������ʡ�
��4�������ڷ�Ӧ�л����ClO2��SO2�ȴ�����Ⱦ�������Ҫβ��������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ���ܽᡶ�л���ѧ��.. | |
| �����Ŀ |