微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A、B、C、D、E、F是短周期元素,周期表中A与B、B与C相邻;C与E同主族;A与C最外层电子数之比为2:3,B的最外层电子数比C的最外层电子数少1个; F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞溶液变红。
(1)E在周期表中的位置为__________________________;D的最高价氧化物的水化物的电子式___________________________。
(2)B、C的氢化物稳定性顺序为(用分子式表示,由大到小)_________>__________。
(3)B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z的名称为____________________,Z的化学键类型为____________________。
(4)两种均含C、D、E、F四种元素的化合物相互反应放出气体的反应离子方程式为_____________________________________。
(5)一定量的D2C2与AC2反应后的固体物质,恰好与含0.8mol HCl的稀盐酸完全反应,并收集0.35 mol 气体,则固体物质的组成为(写清成分和物质的量)____________________。
参考答案:(15分)(最后一空3分,其余每空2分)
(1)第三周期第ⅥA族?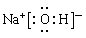 ?
?
(2)H2O >NH3?
(3)硝酸铵?离子键、共价键?
(4)HSO3- +H+?= H2O+SO2 ↑?
(5)0.1mol Na2O2? 0.3mol Na2CO3
本题解析:根据题中信息分析,F元素的原子在周期表中半径最小,F为H元素。常见化合物D2C2与水反应生成C的单质,且溶液使酚酞溶液变红,D2C2为Na2O2,C为O元素,D为Na元素。B与C相邻,B的最外层电子数比C的最外层电子数少1个,B为N元素。C与E同主族,E为S元素。A与B相邻,A与C最外层电子数之比为2:3,A为C元素。
(1)E为S元素,在周期表中的位置为第三周期第ⅥA族。D为Na元素,最高价氧化物的水化物为NaOH,电子式为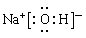 。
。
(2)B为N元素,C为O元素,氢化物分别为NH3、H2O,O元素的非金属性大于N元素,氢化物稳定性为H2O >NH3。
(3)B为N元素,氢化物分别为NH3,最高价氧化物的水化物是HNO3,NH3和HNO3反应生成NH4NO3,Z的名称为硝酸铵,含有离子键和共价键。
(4)C、D、E、F分别为O元素、Na元素、S元素、H元素。四种元素的化合物相互反应放出气体的物质为NaHSO3,H2SO4,反应的离子方程式为HSO3- +H+?= H2O+SO2。
(5)D2C2、AC2分别为Na2O2、CO2,反应生成Na2CO3和O2,根据Na2CO3~2H+~CO2,酸过量,2Na2O2~4H+~O2,酸少量,固体为Na2O2和Na2CO3的混合固体,则2n(Na2CO3)+2n(Na2O2)=0.8mol,n(Na2CO3)+1/2n(Na2O2)=0.35mol,解得n(Na2CO3)= 0.3mol,n(Na2O2)="0.1" mol。
点评:本题考查元素的推断以及元素化合物知识,解答本题时注意把握原子的结构特点,结合元素周期律知识进行推断,本题难度中等。
本题难度:一般
2、填空题 (6分)已知四种短周期元素形成的离子 、
、 、
、 、
、 具有相同的电子层结构。(用推断出的元素符号表示)
具有相同的电子层结构。(用推断出的元素符号表示)
①M、N、R、W的原子序数由大到小的顺序是?。
②M、N、R、W的原子半径由大到小的顺序是?。
③ 、
、 、
、 、
、 的离子半径由大到小的顺序是? ?。
的离子半径由大到小的顺序是? ?。
参考答案::(1)①N>M>R>W
②M>N>W>R
③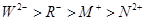 ?
?
(2)①1?②m+n?③8-m-n
本题解析:
四种短周期元素形成的离子 、
、 、
、 、
、 具有相同的电子层结构,则在元素周期表中位置:
具有相同的电子层结构,则在元素周期表中位置: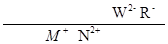
①N>M>R>W
②③比半径大小,先看电子层数,层数越多半径越大;等层数,看核,核电荷数越大,半径越小。M、N、R、W的原子半径由大到小:M>N>W>R; 、
、 、
、 、
、 的离子半径由大到小:
的离子半径由大到小: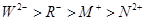 。
。
本题难度:一般
3、选择题 A、B为同主族的两元素,A在B的上一周期,若A的原子序数为n,则B的原子序数不可能为
A.n+8? B.n+18? C.n+32?D.n+20
参考答案:D
本题解析:周期表中各周期含有的元素种类分别是2、8、8、18、18、32、32(全部排满后),所以同主族上下两主族元素的原子序数相差一定不可能是20,答案选D。
点评:该题主要是考查学生对元素周期表结构的熟悉了解程度,旨在培养学生氯化银基础知识解决实际问题的能力。该题的关键是在明确周期表编制原则的基础上,熟练记住元素周期表的结构,并能结合题意灵活运用即可。
本题难度:一般
4、选择题 某实验室仅有如下仪器或用具:烧杯、铁架台、铁圈、三脚架、漏斗、分液漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴.从缺乏仪器的角度来看,不能进行的实验操作是
A.蒸发
B.萃取
C.液体过滤
D.固体溶解
参考答案:C
本题解析:对照每项操作,检查是否缺乏某些或某件必用的仪器.如蒸发所需的仪器有:蒸发皿、酒精灯、火柴、玻璃棒、铁架台、铁圈或三脚架,所给仪器充分;萃取所需的仪器只有分液漏斗、烧杯;固体溶解前述仪器已经足够;只有液体过滤尚缺少滤纸而无法进行.
本题难度:一般
5、填空题 (12分)X、Y、Z、E、F为五种短周期元素,原子序数依次递增。X+中只含有一个质子;Y的正、负化合价绝对值相等,在同族元素中氢化物最稳定;Z的原子核内质子数是Y的最外层电子
数的2倍;F与Z同主族;E与X同主族。试推断:
⑴下列元素分别是:Y ??Z??F??。(用元素符号表示)
⑵X、Z、E形成化合物的电子式为??,所含有的化学键有?
??;它属于??化合物(填离子或共价)
参考答案:(1)C? O? S? (2) 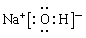 、离子键和极性键、离子
、离子键和极性键、离子
本题解析:(1)X+中只含有一个质子,所以X是氢元素。Y的正、负化合价绝对值相等,则Y是第ⅣA元素。又因为Y在同族元素中氢化物最稳定,所以Y是碳元素。则Z是氧元素,F是硫元素,E是钠。
(2)X、Z、E形成化合物是氢氧化钠,含有离子键和极性键,属于离子化合物,其电子式为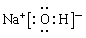 。
。
本题难度:简单