微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.根据反应 可知:用酸性KMnO4溶液可检验绿矾
可知:用酸性KMnO4溶液可检验绿矾 是否变质
是否变质
B.根据反应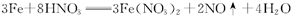 可知:反应中HNO3表现酸性和氧化性
可知:反应中HNO3表现酸性和氧化性
C.根据反应 可知:
可知: 的酸性比
的酸性比 强
强
D.根据反应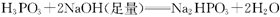 可知:
可知: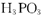 属于三元酸
属于三元酸
参考答案:B
本题解析:A错,酸性高锰酸钾溶液虽会氧化亚铁离子为铁离子,使高锰酸钾溶液褪色,但铁离子溶液为棕黄色溶液,不易判断;B正确,硝酸与铁反应生成了盐起酸性作用,生成NO元素化合价降低,又表现为氧化性;C错,该反应能进行的原因是生成了难溶于稀硫酸的CuS沉淀;D错,该反应只能知道磷酸为二元酸,不知道其是否为三元酸;
本题难度:一般
2、选择题 下列物质的水溶液中,加入Ba(OH)2溶液后原溶液中阴、阳离子都减少的是
A.Na2CO3
B.FeCl3
C.CuSO4
D.Ca(NO3)2
参考答案:C
本题解析:A中生成碳酸钡沉淀,阳离子没有减少;B中生成氢氧化铁沉淀,氯离子没有减少;D中不反应,都没有减少;C中生成硫酸钡和氢氧化铜,都减少,答案选C。
本题难度:一般
3、选择题 某无色溶液中,已知含有H+、Mg2+、Al3+等阳离子,逐滴加入NaOH(aq),则消耗NaOH(aq)的体积(x轴)和生成沉沉量(y轴)之间的函数关系可用下图表示,其中正确的是
[? ]
A.
B.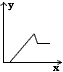
C.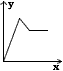
D.
参考答案:B
本题解析:
本题难度:一般
4、选择题  常温下,向0.1mol/L的H2SO4溶液中逐滴加入0.1mol/L的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的
常温下,向0.1mol/L的H2SO4溶液中逐滴加入0.1mol/L的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的
A.b处溶液的c(H+)与d处溶液的c(OH-)相等
B.a~d溶液的导电能力:a<b<c<d
C.a~d溶液的C(H+):a>b>c>d
D.c处溶液和d处溶液均呈碱性
参考答案:C
本题解析:分析:先判断酸的体积,然后根据图象计算abcd四点的体积,根据反应程度判断abcd四点溶液的酸碱性、离子浓度、导电能力.
解答:由题意知,酸碱浓度相等,且酸碱反应时计量数之比为1:1,沉淀最大时消耗碱的体积与酸的体积相等,所以酸的体积是20ml,a点为酸溶液体积为20ml,b点混合液体积为30ml,c点体积为40ml,d点为50ml.
A、b点酸溶液剩余10ml,d点碱液剩余10ml,酸碱浓度相等,所以酸碱的物质的量相等,虽然b、d两点氢离子和氢氧根的物质的量,但混合液的体积不同,所以浓度不等,故A错误;
B、溶液的导电能力与离子的浓度成正比,离子的浓度越大导电能力越强,c处电解质是弱电解质水,离子浓度最小,导电能力最弱,故B错误;
C、a、b都为酸性溶液,a点氢氧根和氢离子没反应,浓度最大,b点氢氧根和部分氢离子反应,c点为中性溶液,d点为碱性溶液,所以氢离子浓度大小为:a>b>c>d,故C正确;
D、c处Ba2+和SO42-?恰好完全反应生成沉淀,H+和OH-恰好完全反应生成H2O,溶液呈中性,d处溶液中Ba(OH)2过量,溶液呈碱性,故D错误;
故选C.
点评:本题是图象解析题,难度较大,分析图象时要注意曲线的“原点”、“交点”、“转折点”等的意义,对“数”、“形”、“义”、“性”进行综合思考,从中发掘隐含信息快速解题.
本题难度:一般
5、选择题 下列离子方程式正确的是
A.氯化亚铁溶液中通入少量氯气? Fe2+ + Cl2 = Fe3+ +2Cl―
B.向溴化亚铁溶液中通入过量氯气:Fe2+ + 2Br― + 2Cl2 ="=" Fe3+ + Br2 + 4Cl―
C .向碳酸氢铵溶液中加入足量的NaOH溶液:NH4+ +OH-= NH3・H2O
.向碳酸氢铵溶液中加入足量的NaOH溶液:NH4+ +OH-= NH3・H2O
D.等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合时发生反应:
HCO3-+Ba2++OH-?BaCO3↓+H2O
参考答案:D
本题解析:略
本题难度:简单