��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б�������ȷ���ǣ�?��
A���κ���ʹ��ֵ��С�Ĺ��̶����Է�����
B����֪��2SO2��g��+O2��g�� 2SO3��g������H=-197kJ��mol��ʵ����4molSO2�μ�������Ӧ�ų�354kJ��������SO2��ת������ӽ���90��
2SO3��g������H=-197kJ��mol��ʵ����4molSO2�μ�������Ӧ�ų�354kJ��������SO2��ת������ӽ���90��
C����Na2SO4��Һ�м��������BaCl2����Һ�в�����SO42-
D��1mol NaOH�ֱ��1mol CH3COOH��1molHNO3��Ӧ�����߱�ǰ�ߡ�H��
�ο��𰸣�B
���������
��ȷ�𰸣�B
A������ȷ���ر���ʱ乲ͬ������Ӧ���Է���
B����ȷ��SO2��ת���ʣ�345�£�197��2����100%=87.6%
C������ȷ����Һ�д���BaSO4���ܽ�ƽ�⣻
D�����ߡ�HС������������ȣ��к�ʱ�����٣���H��
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�����������������ڷ�Ӧ������������
A����������������Ȼ�茶����Ϸ�Ӧ
B�����������þ��Ӧ
C��ʯ��ʯ��������
D��ˮ�ķֽ�
�ο��𰸣�B
���������A �����ȷ�Ӧ�����������������ڷ�Ӧ��������
B �Ƿ��ȷ�Ӧ�����������������ڷ�Ӧ��������
C �����ȷ�Ӧ�����������������ڷ�Ӧ��������
D�����ȷ�Ӧ�����������������ڷ�Ӧ��������
��ѡB
�����Ѷȣ�һ��
3��ѡ���� ��֪��25�桢l0lkPa������
4Al(s)��3O2(g)=2Al2O3(s)?��H=-2834.9kJ/mol
4Al(s)��2O3(g)=2Al2O3(s)?��H=-3119.91kJ/mol:?�ɴ˵ó��Ľ�����ȷ����
A����������O2��O3�����ͣ���O2��O3Ϊ���ȷ�Ӧ
B����������O2��O3�����ͣ���O2��O3Ϊ���ȷ�Ӧ
C��O3��O2�ȶ�����O2��O3Ϊ���ȷ�Ӧ
D��O2��O3�ȶ�����O2��O3Ϊ���ȷ�Ӧ
�ο��𰸣�A
����������ɸ����������Ȼ�ѧ����ʽ��������ͬ�����µõ���ͬ����������������������������Ҫ�ࡣ˵����������O3��O2�����ߡ�����Խ��Խ�ȶ����ɳ���������Ϊ���ȷ�Ӧ����ȷѡ��ΪA��
�����Ѷȣ�һ��
4��ѡ���� �������Է�ĩ״̬���ڣ��Ͱ�������������ͬ�������塣��֪��
�� Sn(s����) + 2HCl(aq) �� SnCl2(aq) + H2(g) + Q1?
�� Sn(s����) + 2HCl(aq) �� SnCl2(aq) + H2(g) + Q2

 �� Sn(s����)
�� Sn(s����)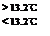 Sn(s����) + Q3��? Q3=" -" 2.1kJ
Sn(s����) + Q3��? Q3=" -" 2.1kJ
����������Ϣ�ƶ���ȷ����
A�������������Ļ���ת���ǿ��淴Ӧ
B�����������Ի���״̬����
C����Ӧ�е������仯��Q1 < Q2
D�����ڴ���13.2�����£�������������лٻ�
�ο��𰸣�D
������������ȣ�Sn�Ҽ��ȵõ�Sn�ף�˵��Sn���е�����Ҫ��������Sn������SnCl2���϶�Ҫ�ų����Ӷ�������Q1>Q2�����淴Ӧ��ָ��ͬ���������淴Ӧ���ڽ���,����ֲ�����ͬ�¶�ת����������25�ȣ�������״̬���ڣ������±��Sn��,�Ƿ�ĩ���Գ��ڴ��ڵ��»��ɷ�ĩ��D�ԡ�
�����Ѷȣ�һ��
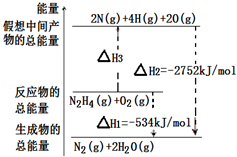
5��ѡ���� ��6�֣���2012?���죩�£�H2N��NH2����һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯��ͼ��ʾ����֪����1mol��ѧ�������������kJ����N��NΪ942��O=OΪ500��N��NΪ154�������1molN��H�������������kJ���ǣ�?��
A��194
B��391
C��516
D��658
�ο��𰸣�B
��������������Ȼ�ѧ����ʽ�ĺ����֪���ɼ����������յ��������¼��������ͷŵ�����֮�Ϊ��ѧ��Ӧ�ʱ����ֵ�����ͼʾ�������شɣ�
�⣺����ͼ�����ݣ����Կ���N2H4��g��+O2��g��=2N��g��+4H��g��+2O��g������H3=2752kJ/mol��534kJ/mol=2218kJ/mol��
�����1molN��H�����������ΪK����154+4K+500=2218�����K=391��
��ѡB��
���������⿼��ѧ����ѧ���Ķ��Ѻ������뷴Ӧ��������֮��Ĺ�ϵ������ѧ��֪ʶ�����Ӧ��������ѶȲ���
�����Ѷȣ�һ��