��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1������˵����ȷ����______
A����ѧ��Ӧ��ʵ�ʾ��Ǿɻ�ѧ���Ķ��ѣ��»�ѧ�����γɣ��ڻ�ѧ��Ӧ�У���Ӧ��ת��Ϊ�������ͬʱ����Ȼ���������ı仯
B��������������ʴ�����ⸯʴ�ĸ�����Ӧ��ΪFe-2e-=Fe2+
C�����ȷ�Ӧ����ʱ��һ��Ҫ���ȣ������ȷ�Ӧ����Ҫ���Ȳ��ܷ���
D�����淴Ӧ��һ����������һ�����ȣ�����Ӧ���е�һ���Ⱥ�Ӧ�ﲻ��ת��Ϊ������
��2��25�桢101kPa�����£�8gCH4������ȫȼ������CO2�����Һ̬ˮ�ų�445kJ������
д��CH4ȼ�յ��Ȼ�ѧ����ʽ______
��3��101kPa�����£�������������Ӧ���ɰ����������仯��ͼʾ�⣺
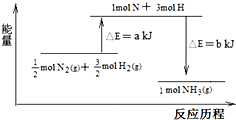
����֪����a=1127����25�桢101kPa��N2��g��+3H2��g��=2NH3��g����H=-92kJ?mol-1��b=______��
�ο��𰸣���1��A����ѧ��Ӧ��ʵ�ʾ��Ǿɻ�ѧ���Ķ��ѣ��»�ѧ�����γɣ��ڻ�ѧ��Ӧ�У���Ӧ��ת��Ϊ�������ͬʱ�����ڷ�Ӧ�����������������ȣ���Ȼ���������ı仯����A��ȷ��
B��������������ʴ�����ⸯʴ�ĸ�����Ӧ���ǽ���ʧȥ���ӣ��缫��ӦΪ��Fe-2e-=Fe2+����B��ȷ��
C�����ȷ�Ӧ����ʱ��һ��Ҫ���ȣ������ȷ�ӦҲ��һ��Ҫ���ȣ���C����
D�����淴Ӧ��һ����������һ�����ȣ�����Ӧ���е�һ���Ⱥ�Ӧ����Ȼת��Ϊ�������D����
��ѡ��AB��
��2��8gCH4������ȫȼ������CO2�����Һ̬ˮ�ų�445kJ������16g��1molCH4��������ȼ������CO2��Һ̬ˮ���ų�889kJ���������Ȼ�ѧ����ʽΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890KJ/mol��
�ʴ�Ϊ��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890KJ/mol��
��3���÷�Ӧ���ȣ���Ӧ��=��Ӧ��ļ���-������ļ��ܣ�������������Ӧ���ɰ������Ȼ�ѧ����ʽΪ��
12N2��g��+32H2��g��=NH3��g����H=a-bkJ?mol-1����N2��g��+3H2��g��=2NH3��g����H=2��a-b��kJ?mol-1=-92kJ?mol-1������a-b=-46������a=1127������a-b=-46��b=1173���ʴ�Ϊ��1173��
���������
�����Ѷȣ���
2������� ��֪A��g��+B��g��?C��g��+D��g��?��Ӧ�����е������仯��ͼ��ʾ���ش��������⣮
��1���÷�Ӧ��______��Ӧ������ȡ��������ȡ���������Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת����______�����������С�����䡱����
��2���ڷ�Ӧ��ϵ�м����������Ӧ��������E�ı仯��______�������������С�����䡱��������______��?E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ������Ӱ�죿______��
��3��һ�������£������Ϊ2L�ĺ����ܱ������г���1mol?A��g��?��3mol?B��g�����жϸ÷�Ӧ�ﵽƽ��״̬�������ǣ�����ţ�______��
��c?��A��=c?��C��?��������ѹǿ����
�ۻ�������ƽ����Է�����������?��v���棩��D��=v?��������B��
��4����ij�¶��£���Ӧ�����ʼŨ�ȷֱ�Ϊ��c��A��=1mol?L-1��c��B��=2.4mol?L-1���ﵽƽ���A��ת����Ϊ60%����ʱB?��ת����Ϊ______��
��5������Ӧ�¶Ȳ��䣬��Ӧ�����ʼŨ�ȷֱ�Ϊ��c��A��=4mol?L-1��c��B��=amol?L-1���ﵽƽ���c��C��=2mol?L-1���г�����ʽ�����aֵ��
�ο��𰸣���1����ͼ����Կ�����Ӧ�����������������������������÷�Ӧ������ӦΪ���ȷ�Ӧ��
�����¶�ƽ�������ȷ�Ӧ�ƶ��������淴Ӧ�ƶ���A��ת���ʼ�С��
�ʴ�Ϊ�����ȣ���С��
��2�������ı��˷�Ӧ�����̽����ͻ�ܣ��ӿ췴Ӧ���ʣ���Ӧ��ȡ���ڷ�Ӧ���������������������������������Ӱ�췴Ӧ�ȣ�
�ʴ�Ϊ����С��?��Ϊ�����ı��˷�Ӧ������ʹ���E���ͣ�?��Ӱ�죮
��3����ƽ��ʱA��CŨ�ȿ�����ȣ���c?A��=c��C������˵����Ӧ����ƽ�⣬�ʢٴ���
?���ɷ���ʽ��֪����Ӧǰ������������䣬������ѹǿ�������仯���ʢڴ���
�ۻ��������������䣬�ܵ����ʵ������䣬��������ƽ����Է�������ʼ�ղ��䣬�ʢ۴���
?��v���棩��D��=v?��������B��������֮�ȵ��ڻ�ѧ������֮�ȣ�˵����Ӧ����ƽ�⣬�ʢ���ȷ��
��ѡ���ܣ�
��4������c��A��=60%��1mol?L-1=0.6mol?L-1��Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȣ����ԡ�c��B��=��c��A��=0.6mol?L-1���ʴ�ʱB��ת����0.6mol/L2.4mol/L��100%=25%��
�ʴ�Ϊ��25%
��5���ɣ�4����֪ƽ��ʱ�������ʵ�Ũ��Ϊc��A��=0.4mol/L��c��B��=2.4mol/L-0.6mol/L=1.8mol/L��c��C��=c��D��=��c��B��=��c��A��=0.6mol/L������ƽ�ⳣ��k=0.6��0.60.4��1.8=12��
��Ӧ�����ʼŨ�ȷֱ�Ϊ��c��A��=4mol?L-1��c��B��=amol?L-1���ﵽƽ���c��C��=2mol?L-1�������ɵ�DΪ2mol?L-1��ƽ��ʱc��A��=2mol?L-1��c��B��=��a-2��mol?L-1��
�¶Ȳ��䣬��ƽ�ⳣ�����䣬��2��22��(a-2)=12��a=6��
�ʴ�Ϊ��6��
���������
�����Ѷȣ�һ��
3������� ͨ�����ǰѲ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ķ�Ӧ�ȵ��ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
��ѧ��
| Si-O
| Si-Cl
| H-H
| H-Cl
| Si-Si
| Si-C
|
����/kJ��mol��1
| 460
| 360
| 436
| 431
| 176
| 347
|
��ش��������⣺
��1����֪Si��SiC��SiO2�ۻ�ʱ�������������ѧ�����Ƚ������������ʵ��۵�ߵͣ��>����<������SiC_____Si��Si _____SiO2
��2����ҵ�ϸߴ����ͨ�����з�Ӧ��ȡ�� ����2 mol H2���ɸߴ�����_____ ������ա��ų���������_____ kJ��
����2 mol H2���ɸߴ�����_____ ������ա��ų���������_____ kJ��
��3����֪��ȼ���ȵ��Ȼ�ѧ����ʽΪSi(s)+O2(g)===SiO2(s) ?��H=-989.2kJ��mol��1����O=O������Ϊ_____________��
�ο��𰸣�(1)>����<����(2)���ա���236?��3��498.8 kJ��mol��1
�����������1����ѧ��Խǿ������Խ�ȶ�������̼������ȶ���ǿ�ڹ衣���ʹ���ȶ������ڶ�������ġ�
��2����Ӧ�Ⱦ��Ƕϼ����յ��������γɻ�ѧ�����ų��������IJ�ֵ�����Ը÷�Ӧ�ķ�Ӧ����360 kJ��mol��1��4+2��436 kJ��mol��1��4��431 kJ��mol��1��176 kJ��mol��1��2��236kJ��mol��1�����������ȷ�Ӧ.
��3����O=O������Ϊx���ɼ��ܿ�֪176 kJ��mol��1��2+x��4��460 kJ��mol��1����989.2kJ��mol��1������x��498.8 kJ��mol��1.
�����Ѷȣ�һ��
4��ѡ���� ����˵��������ǣ�?��
A��ȼ�ϵ�ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ
B��һ������ȼ����ȫȼ�շų��������Ȳ���ȫȼ�շų���������
C�����ȷ�Ӧ���淴Ӧһ�������ȷ�Ӧ
D��ѡ��ȼ��ֻҪ����ȼ����ֵ�Ĵ�С
�ο��𰸣�D
�����������
�����Ѷȣ���
5��ѡ���� ��ӦCO(g)��2H2(g)  CH3OH(g)�����е������仯�������ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ����
CH3OH(g)�����е������仯�������ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ����
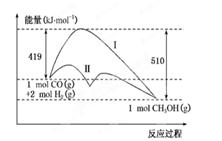
A���÷�Ӧ�Ħ�H����91 kJ/mol
B����������������淴Ӧ�Ļ����ֵ����С
C������������÷�Ӧ�Ħ�H��С
D������÷�Ӧ����Һ̬CH3OH����H���
�ο��𰸣�B
���������A����Ӧ���������������������������÷�Ӧ���ȣ�A����B������������ͷ�Ӧ�Ļ�ܣ������淴Ӧ�Ļ����ֵ����С��B��ȷ��C�������������Ӧ�Ȳ��䣬C����D������÷�Ӧ����Һ̬CH3OH���ų��������������Ӧ��Ϊ���������H��С��D����ѡB��
�����Ѷȣ�һ��