��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1���ƶ��� �������е�A��B��C��D��E 5��Ԫ�أ�ԭ��������������A��Dͬ���壻A��B��ԭ������֮�͵���C��ԭ��������C2-��D+�ĺ����������ȣ�Bԭ����D+�ĺ��������֮�͵���Eԭ�ӵĺ������������D��E��Ԫ�����γ���������Ϊ1��1�����ӻ����
(1)EԪ�ص����ӽṹʾ��ͼΪ____________��
(2)A��BԪ�ء�A��CԪ�ؾ��ɹ���18���ӵķ��ӣ��仯ѧʽ�ֱ�Ϊ___________��____________��
(3)A��CԪ�ؿ����ԭ�Ӹ�����Ϊ1��1�Ĺ��ۻ������ң���E ����ͨ���ҵ�ˮ��Һ�У�����һ��ǿ�ᣬ��������ų�����Ӧ�Ļ�ѧ����ʽΪ__________________��
(4)A��B��C��D��E�е���������Ԫ�ؿ���ɶ��ֻ����X��Y�����е����֡�X��Y���ǼȺ����Ӽ��ֺ����ۼ������ӻ������X��Y�ֱ�����ˮʱ��X�ܴٽ�ˮ�ĵ��룬��Y������ˮ�ĵ��룬Xˮ��Һ��
pH<7��Yˮ��Һ��pH >7����0. 2mol/L��X��Һ��0. 1mol/L��Y��Һ�������Ϻ���Һ�ʼ��ԡ����жϣ���X�Ļ�ѧʽΪ________��Y�Ļ�ѧʽΪ_________���ڻ����Һ�и��ִ����������ʵ���Ũ���ɴ�С��˳��Ϊ_______________��
�ο��𰸣�(1) (2)N2H4��H2O2
(2)N2H4��H2O2
(3)H2O2 +Cl2 =2HCl+O2
(4)��NH4Cl(��NH4NO3)��NaOH����c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)
���������
�����Ѷȣ�����
2��ѡ���� X2+��Y-��벵ĵ��Ӳ�ṹ��ͬ�������ж��в���ȷ����
[? ]
A��ԭ�Ӱ뾶 X>Y
B��ԭ������ X>Y
C������������ X>Y
D�����Ӳ��� X<Y
�ο��𰸣�CD
���������
�����Ѷȣ���
3������� ����Ԫ�����ڱ���һ���֣��ش������й����⣺
��
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0
2
��
��
3
��
��
��
��
��
��
��
4
��
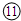
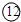
|
��1������ЩԪ�ص�����������Ӧˮ�����У�������ǿ���ǣ��ѧʽ����ͬ��______��������ǿ����______�������Ե�����������______��
��2��д����ҵ��ұ���ݵĻ�ѧ����ʽΪ______������һ�ֺ�ɫ���巴Ӧұ�����Ļ�ѧ����ʽΪ��______��
��3���ڢ�����У��ǽ����Խ�ǿ��Ԫ����______��д��������֤�ý��۵�һ�����ӷ�Ӧ����ʽ______��
�ο��𰸣���Ԫ�������ڱ���λ�ÿ�֪����ΪN����ΪF����ΪNa����ΪMg����ΪAl����ΪSi����ΪS����ΪCl����ΪAr����ΪK��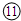 ΪCa��
ΪCa��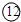 ΪBr��
ΪBr��
��1������������Ӧˮ�����У�Cl������������ˮ����������ǿ������ΪHClO4��K������������ˮ���������ǿ���ü�ΪKOH����������Ϊ�������������������������ΪAl��OH��3���ʴ�Ϊ��HClO4��KOH��Al��OH��3��
��2����ⷨұ��Al���÷�ӦΪ2Al2O3�����ڣ����.����ʯ4Al+3O2����Al��������������Ӧ����Fe���÷�ӦΪ3Fe3O4+8Al����.9Fe+4Al2O3��
�ʴ�Ϊ��2Al2O3�����ڣ����.����ʯ4Al+3O2����3Fe3O4+8Al����.9Fe+4Al2O3��
��3��Cl��Sλ��ͬ���ڣ�ԭ��������ķǽ�����ǿ���ǽ�����Cl��S�������÷ǽ�������֮����û���Ӧ˵������Cl2+S2-=S��+2Cl-���ʴ�Ϊ��Cl��Cl2+S2-=S��+2Cl-��
���������
�����Ѷȣ�һ��
4��ѡ���� ��������������������?
A��ľ̿��������ȼ�շ�����
B����˿��������ȼ�վ��ң��������䣬���ɺ�ɫ����
C������������ȼ�ղ��������İ���
D��þ������ʳ���������
�ο��𰸣�C
���������C�����Ӧ����ȷ�Ļ�ѧʽ���Ǻ����ǰ��ף�P/P4).
4P+5O2=2P2O5(���������ף�
�����������ڴ˷�Ӧ������С������ʽ�ֲ��ڿ����У���������Ӧ�ð�����Ϊ�̡�
������ָСҺ�Σ�������ˮ���ֲ��ڿ����У�����ǰ��Ӧ��û��ˮ��������ɣ����Բ��ܳ�֮Ϊ�����ʴ�����ѡC��
���������⿼����ǻ�ѧ��Ӧ��������֪ʶ����Ŀ�ѶȲ���ּ�ڿ���ѧ���Ի���֪ʶ�����ա�
�����Ѷȣ���
5������� ����֪a��b��c��d��eΪ����������Ԫ�أ�����
��a��b��ͬ����Ԫ�أ��������γɶ�����̬�����
��a��c��ͬ����Ԫ�أ��������γ�������̬�����
��a��d��ͬ����Ԫ�أ��������γ����ֳ��������
��e�ɷֱ��a��b��c��d�γɾ�����ͬ�������Ĺ��ۻ�����ס��ҡ���������
��ش�
��1��aԪ��Ϊ______���ķ���ʽΪ______�����ĵ���ʽΪ______��
��2��������һ�ֻ���Ԫ���γɵ����ʿ���ˮ����������ԭ��Ӧ���������û���Ӧ��д��һ������Ҫ��Ļ�ѧ��Ӧ����ʽ��______��
��̼��̼�Ļ����������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ������ʽ��
��1������ȼ��ʱ�ų��������ȣ�����Ϊ��ԴӦ������������������
��֪��2CH4��g��+3O2��g���T2CO��g��+4H2O��l������H1=-1214.6kJ/mol��
��CO2?��g���TCO?��g��+
O2��g������H2=+283kJ/mol
�����ȼ���ȵ��Ȼ�ѧ����ʽΪ______��
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g�����õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min
H2O
CO
CO2
CO
1
650
2
4
1.6
2.4
5
2
900
1
2
0.4
1.6
3
3
900
a
b
c
d
t
|
��ʵ��1�У���v��H2����ʾ��ƽ����Ӧ����Ϊ��______?mol/L?min��
�ڸ÷�Ӧ������ӦΪ______��������š����ȷ�Ӧ��
����Ҫʹʵ��3�ﵽƽ��״̬ʱ�����ʵ����������ʵ��2�ֱ���ȣ���a��bӦ����Ĺ�ϵ��______���ú�a��b��ʾ����
�ο��𰸣�����֪a��b��c��d��eΪ����������Ԫ�أ���a��b��ͬ����Ԫ�أ��������γɶ�����̬�������a��c��ͬ����Ԫ�أ��������γ�������̬������ݴ˿�֪aΪOԪ�أ�bΪNԪ�أ�cΪCԪ�أ���a��d��ͬ����Ԫ�أ��������γ����ֳ��������dΪSԪ�أ���e�ɷֱ��a��b��c��d�γɾ�����ͬ�������Ĺ��ۻ�����ס��ҡ���������Ϊ18���ӻ����eΪHԪ�أ��ʼ�ΪH2O2����ΪN2H4����ΪC2H6����ΪH2S��
��1��������������֪��aΪ��Ԫ�أ���ΪH2O2����ΪH2S������ʽΪ
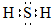
���ʴ�Ϊ������H2O2��
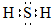
��
��2��������һ�ֻ���Ԫ���γɵ����ʿ���ˮ����������ԭ��Ӧ���������û���Ӧ������Ҫ��Ļ�ѧ��Ӧ����ʽ��3NO2+H2O=NO+2HNO3�ȣ�
�ʴ�Ϊ��3NO2+H2O=NO+2HNO3��
��1����֪��2CH4��g��+3O2��g���T2CO��g��+4H2O��l������H1=-1214.6kJ/mol��
��CO2?��g���TCO?��g��+12O2��g������H2=+283kJ/mol��
���ݸ�˹���ɣ���-�ڡ�2��2CH4��g��+4O2��g���T2CO2��g��+4H2O��l������H=-1780.66kJ/mol��
���Լ���ȼ���ȵ��Ȼ�ѧ����ʽΪCH4��g��+2O2��g���TCO2��g��+2H2O��l���ġ�H=-890.3?kJ/mol��
�ʴ�Ϊ��CH4��g��+2O2��g���TCO2��g��+2H2O��l���ġ�H=-890.3?kJ/mol��
��2�����ɱ������ݿ�֪��ƽ��ʱn��CO2��=1.6mol������v��CO2��=1.6mol2L5min=0.16mol/��L?min������������֮�ȵ��ڻ�ѧ������֮�ȣ�����v��H2��=v��CO2��=0.16mol/��L?min�����ʴ�Ϊ��0.16��
�ڷ�Ӧ����ֵĻ�ѧ������Ϊ1���ʿ��������ʵ�������Ũ�ȼ���ƽ�ⳣ����
650��ʱ����ƽ�⣺H2O��g��+CO��g��?CO2��g��+H2��g����
��ʼ��mol����2? 4? 0? 0
�仯��mol����1.6? 1.6? 1.6?1.6
ƽ�⣨mol����0.4? 2.4? 1.6? 1.6
����650���ƽ�ⳣ��k=1.6��1.60.4��2.4=83
900��ʱ����ƽ�⣺H2O��g��+CO��g��?CO2��g��+H2��g����
��ʼ��mol����1? 2 ? 0? 0
�仯��mol����0.4?0.4?0.4?0.4
ƽ�⣨mol����0.6?1.6?0.4? 0.4
����900���ƽ�ⳣ��k=0.4��0.40.6��1.6=16��
�����¶�ƽ�ⳣ����С���������¶�ƽ�����淴Ӧ�ƶ��������¶������ȷ�Ӧ�ƶ���������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ���ţ�
��ʹʵ��3�ﵽƽ��״̬ʱ�����ʵ����������ʵ��2�ֱ���ȣ�Ϊ��Чƽ�⣬�÷�ӦΪ��Ӧǰ�����������������仯������n��H2O����n��CO��=1��2���ɣ���b=2a��
�ʴ�Ϊ��b=2a��
���������
�����Ѷȣ�һ��