微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验方法合理的是
A.可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液
B.可用分液的方法从溶有溴的四氯化碳溶液中分离出单质溴
C.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量相等
D.可用水鉴别已烷、四氯化碳、乙醇三种无色液体
参考答案:D
本题解析:略
本题难度:一般
2、选择题 海带中含碘元素。从海带中提取碘有如下步骤:①通入适量的Cl2②将海带焙烧成灰后加水溶解③加CCl4振荡④用分液漏斗分液⑤过滤⑥蒸馏,则正确的操作顺序是(?)?
A.①②③④⑤⑥
B.②⑤①③④⑥
C.①③⑤②④
D.②①③⑥⑤④
参考答案:B
本题解析:略
本题难度:简单
3、实验题 下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置
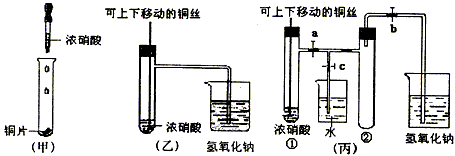
(1)写出铜和浓硝酸反应的离子方程式__________________________。
(2)和甲装置相比,乙装置的优点有____________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹_________,再打开弹簧夹_________,才能使NO2气体充满②试管。
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操作________________________________。
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是_________________(气体体积按标准状况计算)。
参考答案:(1)Cu+4H++2NO3-==Cu2++2NO2↑+2H2O
(2)①可以控制反应,②吸收NO2气体,防止污染环境
(3)c;a、b
(4)先关闭b,再关闭a,然后打开c,用手捂住(热水、热毛巾、加热)试管②
(5)1/22.4mol・L-1或0.045mol・L-1
本题解析:
本题难度:困难
4、实验题 为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下:
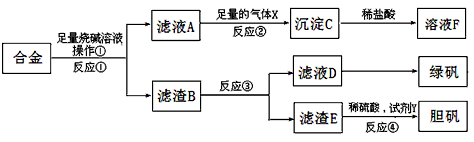
请回答:
(1)操作①用到的玻璃仪器有 ______________。
(2)写出反应①的化学方程式___________ , 反应②的离子反应方程式 _____________。
(3)设计实验方案,检测滤液D中含有的金属离子(试剂自选)_______________。
(4)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,反应④的总化学方程式是__________________ 。
(5)乙同学在甲同学方案的基础上提出用滤渣B来制备 FeCl3・6H2O晶体,在滤渣中滴加盐酸时,发现反应速率比同浓度盐酸与纯铁粉反应要快,其原因是_______________ ,将所得氯化铁溶液用加热浓缩、降温结晶法制得FeCl3・6H2O晶体,而不用直接蒸发结晶的方法来制得晶体的理由是____________ 。
(6)将滤渣B的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见表(设硝酸的还原产物只有NO)。
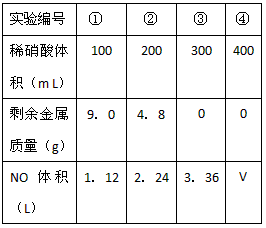
试通过计算填空:
I.硝酸的浓度为 ______________;
II.③中溶解铜的质量为 ________________;
III.④中V=_____________ L。
参考答案:(1)烧杯、漏斗、玻璃棒
(2)2Al + 2NaOH + 2H2O== 2NaAlO2+ 3H2↑?;AlO2- + CO2 + 2H2O==Al(OH)3↓+ HCO3-
(3)取少量滤液D加入NaOH溶液,产生白色沉淀,沉淀变成灰绿色最后变成红褐色。
(4)Cu + H2O2 + H2SO4 + 3H2O == CuSO4・5H2O或Cu+H2O2 + H2SO4 == CuSO4 + 2H2O
(5)铁粉与杂质铜形成原电池反应,加快了反应速率 ;因为氯化铁是强酸弱碱盐水解生成氢氧化铁和盐酸,加热蒸干时使HCl 挥发造成水解平衡右移,因此得不到FeCl3・6H2O晶体
(6)2mol/L; 4.8g; 4.48L
本题解析:
本题难度:困难
5、选择题 通过下列实验方法能达到实验目的是( )
A.用焰色反应证明某物质是否为氯化钠
B.用CaCl2鉴别碳酸钠和碳酸氢钠两种溶液
C.通过颜色鉴别氧化钠和过氧化钠
D.使用润湿有色布条鉴别次氯酸钠和过氧化钠
参考答案:A、焰色反应检验的是金属元素,所以只能检验钠元素不能检验氯离子,故A错误.
B、氯化钙和碳酸氢钠不反应,碳酸钠和氯化钙溶液反应产生白色沉淀,所以能鉴别,故B正确.
C、氧化钠是白色固体,过氧化钠是淡黄色固体,所以能鉴别,故C正确.
D、次氯酸钠和过氧化钠都具有强氧化性,都能使湿润的有色布条褪色,所以不能鉴别,故D错误.
故选BC.
本题解析:
本题难度:一般