微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 常温下,将10.0 g 40%的NaCl溶液跟40.0 g 15%的NaCl溶液混合,得到密度为1.17 g・cm-3的混合液,该混合液NaCl的质量分数为?,物质的量浓度为?。
参考答案:20%? 4 mol・L-1(不带单位不给分)
本题解析:略
本题难度:简单
2、选择题 下列各项中,两种物质间反应均产生1 mol气体时,参加反应的酸的物质的量最少的是
A.碳与浓硝酸
B.铜与浓硫酸
C.锌与稀硫酸
D.二氧化锰与浓盐酸
参考答案:A
本题解析:A、碳与浓硝酸的反应为:C+4HNO3=CO2↑+4NO2↑+2H2O,产生1mol气体需HNO3 0.8mol;B、铜与浓硫酸的反应为:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,产生1mol气体需H2SO4 2mol;C、锌与稀硫酸的反应为:Zn+H2SO4=ZnSO4+H2↑,产生1mol气体需H2SO4 1mol;D、二氧化锰与浓盐酸的反应为:MnO2+4HCl(浓)
CuSO4+SO2↑+2H2O,产生1mol气体需H2SO4 2mol;C、锌与稀硫酸的反应为:Zn+H2SO4=ZnSO4+H2↑,产生1mol气体需H2SO4 1mol;D、二氧化锰与浓盐酸的反应为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,产生1mol气体需HCl 4mol,所以参加反应的酸的物质的量最少的是A项。
MnCl2+Cl2↑+2H2O,产生1mol气体需HCl 4mol,所以参加反应的酸的物质的量最少的是A项。
本题难度:一般
3、选择题 在标准状况下,如果11. 2L氧气含有n个氧原子,则阿伏加德罗常数可表示为
2L氧气含有n个氧原子,则阿伏加德罗常数可表示为
A.n
B.
C.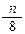
D.4n
参考答案:A
本题解析:略
本题难度:一般
4、计算题 (6分)含CuSO4和H2SO4的混合溶液200mL,其中CuSO4物质的量浓度为1mol.L-1, H2SO4物质的量浓度为0.5mol.L-1,若用此溶液配成0.2mol.L-1 CuSO4和2mol.L-1 H2SO4的混合溶液,试求:
(1)所得溶液的体积是多少毫升?
(2)需加入密度为1.84g.cm-3、98%的浓硫酸多少毫升?
参考答案:(1)1000ml (2)103.3ml
本题解析: (1)稀释前后,硫酸铜的物质的量不变,则所得溶液的体积=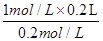 =1000mL,
=1000mL,
答:所得溶液的体积是1000ml;
(2)浓硫酸的物质的量浓度=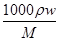 =
=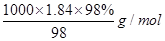 =18.4mol/L,
=18.4mol/L,
增加的硫酸的物质的量=2mol/L×1L-0.5mol/L×0.2L=1.9mol,则需要浓硫酸的体积=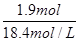 =
=
103.3ml,
考点: 溶液的混合时物质的量浓度的计算。
本题难度:一般
5、选择题 用惰性电极电解VmL某二价金属的硫酸盐溶液一段时间后,阴极有wmg金属析出,溶液的pH从6.5变为2.0(体积变 化可忽略不计)。析出金属的相对原子质量为? (? )
化可忽略不计)。析出金属的相对原子质量为? (? )
A.100w/V
B.20 0w/V
0w/V
C.2×10-5w/V
D.1×10-5w/V
参考答案:B
本题解析:略
本题难度:简单