��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����Ƥ�϶�һ��пʱ��������ͼ��װ�á����������������
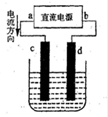
A�����ǰ����Ƥ�����ȼ���Һ�����գ����������
B��cΪ����dΪп
C���ú�Zn2+������ɵ������Һ
D�����ʱ�����������ͻ�ԭ��Ӧ�Ķ���пԪ��
�ο��𰸣�B
���������A�����ǰ�����յijɷ��������ڼ�����������ˮ�⣬ϴ������ڽ���������ȥ��������������⣬��ȷ�� B��c�����������ʱΪ�Ƽ���Ҫ������������C���ú�Zn2+������ɵ������Һ����ȷ��D�����ʱ�����������ͻ�ԭ��Ӧ�Ķ���пԪ�أ���ȷ��
�����Ѷȣ�һ��
2������� ��9�֣��о�������ת��������ȵ�����������������ǻ�ѧ�о�����Ҫ����֮һ��
��1����ͼΪij̫��վ������ת��ʾ��ͼ������ȼ�ϵ����NaOH��ҺΪ���Һ��

�ٹ��ת����������ת����ʽΪ ��
��ˮ���ϵͳ��ͨ����������Na2SO4������Na2SO4��Ŀ���� ��
��ȼ�ϵ�صĸ�����ӦΪ�� ��
��2��������ȼ�ϵ�أ��缫��Ϊʯī�缫��Ϊ�磬����ͼװ�õ��ϡ������Һ��������d�缫�����д������ݲ�����

��d�缫�������� ���������������������
��c�缫�ĵ缫��ӦʽΪ�� ��
��ͨ��������е��ܷ�ӦΪ�� ��
�ο��𰸣���1����̫����ת���ɵ��ܣ�1�֣�����ǿ��Һ�����ԣ�1�֣�
��H2��2OH����2e��===2H2O��2�֣�
��2����������1�֣���Cu ��2e��=== Cu2+��2�֣� ��Cu��H2SO4 CuSO4��H2����2�֣�
CuSO4��H2����2�֣�
�����������1���ٹ��ת������̫����ת��Ϊ��ѧ�ܣ��ڵ����������Һ��ʵ���ǵ��ˮ�����������Ƶ�Ŀ��Ϊ��ǿ��Һ�����ԣ�������ȼ�ϵ�صĸ���ͨ����������������������Ӧ����ӦΪH2��2OH����2e��===2H2O ����2��aΪȼ�ϵ�صĸ���������dΪ���ص�������d�缫��ӦΪ2H++2e-=H2����cΪ���ص�����������c�缫��ӦʽΪCu��2e��=== Cu2+���ҵ��ܷ�ӦΪCu+2H+= Cu2++ H2��
���㣺���⿼����ء�ԭ���ԭ��
�����Ѷȣ�һ��
3��ѡ���� �ö��Ե缫���һ��Ũ�ȵ�CuSO4��Һһ��ʱ�����0.1molCu2��OH��2CO3ǡ��ʹ��Һ�ָ���ԭ����״̬����������������ת�Ƶ�������ʵ���Ϊ��������
A��0.2mol
B��0.4mol
C��0.5mol
D��0.6mol
�ο��𰸣��������ͭʱ�����Σ�2CuSO4+2H2O?ͨ��?.?2Cu��+O2��+2H2SO4����Σ�2H2O?ͨ��?.?2H2��+O2����
���ֻ���յ�һ�εĵ�⣬��Ӧֻ��Ҫ����CuO��CuCO3�Ϳ��ԣ��������ڼ������Cu2��OH��2CO3���൱�ڶ������һ��ˮ��0.1molH2O������0.1mol��ˮ��Ӧ���ǵڶ��εķ�Ӧ���У��ý�ת����0.4mol���ӣ���һ��ת����0.2mol���ӣ������ܹ�ת�Ƶ���0.6mol��
��ѡD��
���������
�����Ѷȣ���
4������� ��14�֣�
����ͼ��ʾ��A��FΪʯī�缫��B��EΪ��Ƭ�缫����Ҫ��ش��������⣮
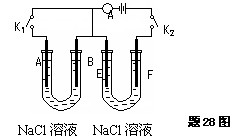
��1����K2���ϲ�K1��BΪ?����A�ĵ缫��ӦΪ?�����տɹ۲쵽��������?��
��2����K1���ϲ�K2��EΪ?����F���ĵ缫��ӦΪ?��
����F����������ķ�����?��
��3������U���еμӷ�̪�����У�1����2������ʱ��A��B��E��F�缫��Χ�ܱ�����?��ԭ����?��
�ο��𰸣�
��1��BΪ?������1������A�ĵ缫��ӦΪ? O2+4e-+2H2O==4OH-?����2����
������?��Һ�в�����ɫ���������ձ�Ϊ���ɫ?��2����
��2��EΪ?��������1����F���ĵ缫��ӦΪ? 2Cl--2e-==Cl2��?����2����
������?��ʪ��ĵ��ۣ�KI��ֽ���飬��ֽ������˵��������?����2����
��3���ܱ����� AE?����2����ԭ����? A��O2�Ϸŵ����OH-��E����ˮ�ŵ����H2��OH-�������µ缫����ʼ���?����2����
�����������
�����Ѷȣ���
5������� (��)����ϵͳ��������д�����и���������
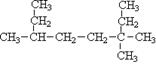 ???
???
(��)��ͼΪ������ļס��������ء��Իش�
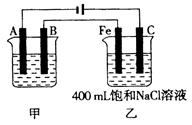
��1�����������õ��ԭ�������϶�����
���������������������������缫���Ϻ͵缫���ƣ���
���еĵ������ӷ���ʽΪ���� ������������?��
��2����������������4.32g�����Ҳ��������Ϸų���������
��״���� ���������������mL��
��3��������������Һʱ��Ϊ�˷�ֹ����ˮ�⣬���Լ���������?����ˮ�ⷽ��ʽΪ ���� ��������������
�ο��𰸣�����3��3��6����������?����1��Fe?����? 2Cl�C+ H2OCl2�� + H2�� +2OH�C[
��3��448 ��4��NaOH? (3)? S2�C + H2O HS�C?+ OH�C
HS�C?+ OH�C
���������AΪ����BΪ��������Ϊ������̼Ϊ������2Cl�C+ H2OCl2�� + H2�� +2OH�C
�����Ѷȣ�һ��