|
���л�ѧ֪ʶ���ܽᡶ���ʵ��������㹮�̣�2017�����°棩(��)
2017-08-22 15:21:23
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������Һ�е�������Ũ����50 mL 1 mol��L-1��AlCl3��Һ��������Ũ����ȵ��ǣ� ��
A��150 mL 1 mol��L-1��NaCl��������
B��75 mL 2 mol��L-1��NH4Cl
C��150 mL 3 mol��L-1��KCl��������
D��75 mL 2 mol��L-1��CaCl2
|
�ο��𰸣�C
������������ݻ�ѧʽ��֪��50 mL 1 mol��L-1��AlCl3��Һ��������Ũ����3mol/L����ѡ��ABCD��������Ũ�ȷֱ��ǣ�mol/L��1��2��3��4����ѡC��
�����Ѷȣ�һ��
2������� ������ʳ�ṹ����ʳϰ�ߵ�Ӱ�죬ȱ���ǹ��˾����ձ��Ե�һ��������ʳ��Ϊ����Ӹƣ��ɱ�֤����һ�����ͳ������ƣ���ͼ��ij��������ij�ּӸ�ʳ�ΰ�װ��ǩ�ϵIJ������֣����Ķ���ش��������⣺
��1����ǩ�ϡ��⣺��20��50��mg/kg���еġ��⡱��ָ______��
A��Ԫ�ء�����������B������
C��ԭ�ӡ�����������D������
��2��Ϊ�˼���������Ƿ���̼��ƣ��ڼ�ͥ�������ѡ�õ�������______��
��3��Ϊ�˲ⶨ���εĸ�Ԫ�غ�����ȡ20g��������ˮ�������������ᣬ����CO2����134.4mL����״���£�������ʽ����˼Ӹ�ʳ���и�Ԫ�ص�����������

�ο��𰸣���1�����ݼӵ�ʳ�εĵ���������̬���ڣ������Ե��ʡ����ӡ�ԭ����ʽ���ڣ����Լӵ�ʳ�εĵ���ָ��Ԫ�أ�
��ѡ��A��
��2���������Ҫ�ɷ���CH3COOH������̼��Ʒ�����ѧ��Ӧ��������������ʴ�Ϊ�����ᣮ
��3��134.4mLCO2��������ʵ���Ϊ0.134422.4moL=0.006moL��������0.006moL������̼��Ҫ̼�������ΪX����
CaCO3+2HCl�TCaCl2+H2O+CO2��
100g1moL
X0.006moL
100gX=1moL0.006moL�����X=0.6g�����Ը�Ԫ������Ϊ0.6mg��40%=0.24g��20g��ʳ���к�����Ϊ��0.24g20g��100%=1.2%��
�ʴ�Ϊ���˼Ӹ�ʳ���и�Ԫ�ص���������Ϊ1.2%��
���������
�����Ѷȣ�һ��
3��ѡ���� ��NAΪ�����ӵ�������ֵ������������ȷ����(? )
A����״���£���22.4L�Ȼ�����������ˮ�У���Һ�к��е�HCl������ΪNA
B�����³�ѹ�£�16g14CH4����������ĿΪ8NA
C�����³�ѹ�£�Na2O2������H2O��Ӧ��������0.2molO2��ת�Ƶ��ӵ���ĿΪ0.4NA
D����״���£�22.4L��������NA�����ʷ���
�ο��𰸣�C
���������HCl��ǿ����ʣ���ˮ��Һ��û��HCl���Ӵ��ڣ�A�����14CH4��������Ϊ18������16g14CH4��������Ŀ��С��8NA��B�����������ɲ����е��ʣ�����CO2�Ȼ����D�����ѡC��
����������٤������������߿��ġ��ȵ㡱���⡣������ȫ���߿���ѧ������ֵļ���Ϊ100%����˫��Ϊ���ȿ�����ѧ�������ʵ�������������������������������ʵ���Ũ��֮��Ĺ�ϵ���ֿ��������ʽṹ������ˮ�⡢������ʵĵ���������ĸ�����֪ʶ���ϳ��ۺ���ϰ�⡣
�����Ѷȣ�һ��
4��ѡ���� ����״���µ�ij���壨Ħ������Ϊ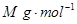 ������agˮ�У�������Һ���ܶ�Ϊ ������agˮ�У�������Һ���ܶ�Ϊ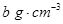 �����ʵ���Ũ��Ϊ �����ʵ���Ũ��Ϊ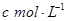 �������������ˮ�е������ �������������ˮ�е������
A��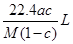
B��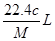
C��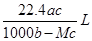
D��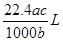
�ο��𰸣�C
�������������Һ�����ΪVaqL,��Һ������Ϊmaq,���ʵ�����Ϊmg�����У�
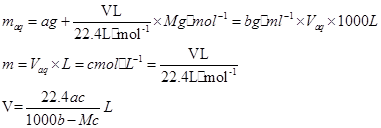
�����Ѷȣ�һ��
5��ѡ���� ��NA��ʾ�����ӵ�����������˵������ȷ����
A���ڱ�״���£���4molHCl��Ũ������������MnO2��Ӧ������22.4L����
B��0.1mol��L��1�Ȼ�����Һ��Cl������0.2NA
C��18gD2O����������ĿΪ10NA�����ԭ��������O��16��
D��4g��������������ΪNA�����ԭ��������He��4��
�ο��𰸣�D
�����������ȻMnO2+4HCl(Ũ)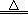 MnCl2+Cl2��+2H2O���������Ȼ����ϵ��֮�ȵ������ʵ���֮�ȣ���������HCl�������Լ�ˮ�����ɣ��ܻ�ԭ�������̵�Ũ������Ϊ������������̷�Ӧ��ϡ���ᣬ��Ӧ��HClһ��С��4mol�����ɵ�����һ��С��1mol����Aѡ�����ȱ����Һ�������������c?V=n���Ȼ��������ʵ�������Bѡ�����D2O����Է�������Ϊ20������m/M=n���D2O�����ʵ���С��1mol��1��D2O����10�����ӣ���18gD2O����������С��10mol����Cѡ�����Ԫ����ϡ�����壬���������ǵ�ԭ�ӷ��ӣ�����Է�������Ϊ4������m/M=n��ú��������ʵ�������1mol����Dѡ����ȷ�� MnCl2+Cl2��+2H2O���������Ȼ����ϵ��֮�ȵ������ʵ���֮�ȣ���������HCl�������Լ�ˮ�����ɣ��ܻ�ԭ�������̵�Ũ������Ϊ������������̷�Ӧ��ϡ���ᣬ��Ӧ��HClһ��С��4mol�����ɵ�����һ��С��1mol����Aѡ�����ȱ����Һ�������������c?V=n���Ȼ��������ʵ�������Bѡ�����D2O����Է�������Ϊ20������m/M=n���D2O�����ʵ���С��1mol��1��D2O����10�����ӣ���18gD2O����������С��10mol����Cѡ�����Ԫ����ϡ�����壬���������ǵ�ԭ�ӷ��ӣ�����Է�������Ϊ4������m/M=n��ú��������ʵ�������1mol����Dѡ����ȷ��
�����Ѷȣ�һ��
|