|
高中化学知识点讲解《离子方程式的书写及正误判断》高频考点强化练习(2017年最新版)(二)
2017-08-22 15:23:34
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
①滴加适量H2O2,紫红色褪去,并有气泡产生;
②再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;
③最后通入足量的SO2气体。
请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为 ;
(2)实验③中的现象为 。
(3)实验①、②中反应的离子方程式分别是 、 。
参考答案:(1)PbO2>KMnO4>H2O2
(2)溶液紫红色褪去,有白色沉淀生成
(3)2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
5PbO2+2Mn2++4H+=5Pb2++2MnO4-+2H2O
本题解析:实验①说明H2O2能被MnO4-氧化,氧化性:KMnO4>H2O2;实验②说明Mn2+能与PbO2反应生成MnO4-,氧化性:PbO2>KMnO4。实验③中SO2还原性较强,能使酸性KMnO4褪色,SO2被氧化为H2SO4,H2SO4和Pb2+反应生成PbSO4白色沉淀。
本题难度:一般
2、填空题 (12分)食盐是重要调味品,随着对饮食健康的重视,出现了各种类型的特种食盐。
(1)常说“饮食过咸会伤骨”,长期摄入食盐过多可能导致骨骼脱钙,下列物质中,可以作为补钙药品主要成分的是 (填标号)。
A.CaCO3
B.CaO
C.Ca(OH)2
D.Ca
| (2)低钠盐因含有氯化钾和硫酸镁可防治高血压和心血管病,往其溶液中滴入氨水,发生反应的化学方程式是 。
(3)加硒盐中含有的硒元素是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实: 。
(4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子 mol,该反应的离子方程式为 。
参考答案:(共12分)(1)A(2分)
(2)MgSO4 +2NH3・H2O=Mg (OH)2↓+ (NH4) 2SO4或Mg2++2NH3・H2O= Mg (OH)2↓+2NH4+(3分)
(3)硒与氢气化合比硫更难(或硒酸酸性比硫酸弱,或硒化氢稳定性比硫化氢弱,或硫能置换出硒等)(2分)
(4)5(2分)2IO3-+5SO32-+2H+===I2+5SO42-+H2O(3分)
本题解析:(1)人体吸收的是钙元素的化合物,同时还不能对人体产生危害。A.CaCO3不会对人体产生危害,会与人体内的酸发生反应产生CaCl2,补充钙元素,正确; B.CaO与水发生反应产生Ca(OH)2,对人体产生腐蚀,、危害,不能使用,错误; C.Ca(OH)2溶于水放热,对人体造成伤害,电离产生的OH-也会对人体造成腐蚀,不能使用,错误;D.Ca是很活泼的金属单质,与人体内的水发生反应产生氢气和强碱Ca(OH)2,对人产生一定危害,错误。故选项是A;(2)低钠盐因含有氯化钾和硫酸镁可防治高血压和心血管病,往其溶液中滴入氨水,发生复分解反应产生沉淀。反应的化学方程式是MgSO4 +2NH3・H2O=Mg (OH)2↓+ (NH4) 2SO4或Mg2++2NH3・H2O= Mg (OH)2↓+2NH4+;(3)硒元素、硫元素是同一主族的元素,元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,相应的氢化物的稳定性就越强,形成氢化物越容易进行解析比较。所以可以通过硒与氢气化合比硫更难(或硒酸酸性比硫酸弱,或硒化氢稳定性比硫化氢弱,或硫能置换出硒等)。(4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,说明产生了I2,根据元素化合价升高或降低的总数等于原子的原子失去或获得的电子数可知:1mol KIO3被还原时,转移电子5mol,该反应的离子方程式为2IO3-+5SO32-+2H+===I2+5SO42-+H2O。
考点:考查补充钙试剂的选择、离子方程式的书写、元素的非金属性强弱比较的方法、氧化还原反应中的电子转移的知识。
本题难度:一般
3、填空题 (8分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式__________________________________________________
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO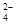 恰好完全沉淀 恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用右图中的曲线表示是________(填序号).
  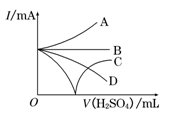
(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________________________.
参考答案:(1)Ba2++2OH-+2H++SO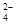 ===BaSO4↓+2H2O (2)A (3)C ===BaSO4↓+2H2O (2)A (3)C
(4)2Ba2++4OH-+Al3++2SO42-=2BaSO4↓ + AlO2-+2H2O
本题解析:(1)Ba(OH)2溶液中逐滴加入与稀硫酸反应的离子方程式是Ba2++2OH-+2H++SO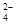 ===BaSO4↓+2H2O;(2) A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,离子方程式是Ba2++2OH-+2H++SO ===BaSO4↓+2H2O;(2) A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,离子方程式是Ba2++2OH-+2H++SO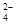 ===BaSO4↓+2H2O;相同,正确;B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO ===BaSO4↓+2H2O;相同,正确;B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO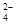 恰好完全沉淀,应该以NaHSO4为标准,离子方程式是:Ba2++OH-+H++SO 恰好完全沉淀,应该以NaHSO4为标准,离子方程式是:Ba2++OH-+H++SO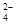 ===BaSO4↓+H2O,不相同,错误;C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,应该以NaHSO4为标准离子方程式是Ba2++OH-+H++SO ===BaSO4↓+H2O,不相同,错误;C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,应该以NaHSO4为标准离子方程式是Ba2++OH-+H++SO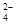 ===BaSO4↓+H2O,不相同,错误;(3) 向Ba(OH)2溶液中逐滴加入稀硫酸,由于发生反应:Ba2++2OH-+2H++SO ===BaSO4↓+H2O,不相同,错误;(3) 向Ba(OH)2溶液中逐滴加入稀硫酸,由于发生反应:Ba2++2OH-+2H++SO ===BaSO4↓+2H2O,溶液中自由移动的离子浓度逐渐减小,所以溶液的导电性逐渐减弱,当Ba(OH)2恰好完全时,由于BaSO4是难溶的强电解质,水是弱电解质,溶液中离子的浓度几乎为0,所以导电能力最小,此后随着硫酸的滴加,溶液中硫酸电离产生的离子浓度逐渐增大,溶液的导电性又逐渐增强,因此整个过程中混合溶液中的导电能力的曲线表示是C;(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.此时由于Al3+与OH-的个数比是1:4,所以Al元素的存在形式是AlO2-,则反应的离子方程式是2Ba2++4OH-+Al3++2SO42-=2BaSO4↓ + AlO2-+2H2O。 ===BaSO4↓+2H2O,溶液中自由移动的离子浓度逐渐减小,所以溶液的导电性逐渐减弱,当Ba(OH)2恰好完全时,由于BaSO4是难溶的强电解质,水是弱电解质,溶液中离子的浓度几乎为0,所以导电能力最小,此后随着硫酸的滴加,溶液中硫酸电离产生的离子浓度逐渐增大,溶液的导电性又逐渐增强,因此整个过程中混合溶液中的导电能力的曲线表示是C;(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.此时由于Al3+与OH-的个数比是1:4,所以Al元素的存在形式是AlO2-,则反应的离子方程式是2Ba2++4OH-+Al3++2SO42-=2BaSO4↓ + AlO2-+2H2O。
考点:考查溶液中离子方程式的书写、比较及溶液的导电性变化的知识。
本题难度:一般
4、填空题 (12分)钾水玻璃以其优异的性能广泛用于防腐、铸造、油田、钻井或各种高档涂料中。钾水玻璃中硅含量的测定可以采用氟硅酸钾容量法,其步骤为:
①称取试样溶解在含有过量的氟离子和钾离子的强酸溶液中,硅能与氟离子、钾离子作用生成氟硅酸钾(K2SiF6)沉淀;
②沉淀分离后于热水中水解,生成HF、H2SiO3、KF;
③过滤除去硅酸沉淀,用氢氧化钠标准溶液滴定滤液。
(1)上述步骤②中的水解反应方程式为 ;
步骤③中反应的离子方程式为: 。
(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得的硅元素含量将 (填“偏高”、或“偏低”或“不变”)。
(3)若每次称取试样的质量为1.00g,重复滴定四次,消耗1.00 mol・L-1氢氧化钠标准溶液的体积为分别为16.80mL、19.90mL、20.00mL、20.10mL,试计算该试样中硅元素的质量分数(以二氧化硅计),写出计算过程。
参考答案:(1)K2SiF6+3H2O=2KF+H2SiO3↓+4HF;(2分);HF+OH-=H2O+F-;(2分)
(2)偏高;(3) 30%。
本题解析:(1)上述步骤产生的氟硅酸钾(K2SiF6)沉淀在热水中水解,生成HF、H2SiO3、KF。②中的水解反应方程式为K2SiF6+3H2O=2KF+H2SiO3↓+4HF;将步骤②中反应产生的硅酸沉淀过滤除去,用氢氧化钠标准溶液滴定滤液,由于HF是弱酸,所以在写离子方程式时应该用化学式,则步骤③中反应的离子方程式为HF+OH-=H2O+F-;(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则消耗标准溶液的体积就偏大,所以使得测得的硅元素含量将偏高;(3)根据实验数据可知第一次数据误差太大,要舍去,则消耗NaOH溶液的体积是:V(NaOH)=(19.90mL+20.00mL+20.10mL)÷3=20.00ml;根据方程式中物质的关系可得关系式:
SiO2――Si――4HF――4NaOH;
60g 4mol
M(SiO2) 0.02Lх1mol/L
求得m(SiO2)=0.30g(2分);硅的质量分数(以二氧化硅计):(0.30g÷1.00g)×100%=30%。
考点:考查物质制取过程的化学方程式、离子方程式的书写、误差分析、物质含量的测定的知识。
本题难度:一般
5、选择题 下列表示对应化学反应的离子方程式正确的是
A.漂白粉溶液通入SO2:Ca2++2ClO-+SO2+H2O=2HClO+CaSO3↓
B.向FeBr2溶液中通入过量氯气:2Fe2++Cl2=2Fe3++2Cl-
C.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
D.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
|