��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� A��B��C���ǽ�������A����C����������Һ�У�A�ı�����C������A��B��ϡ������Һ���ԭ���ʱ��BΪ��صĸ�����A��B��C���ֽ����Ļ��˳��Ϊ��?��
A��A>B>C? B��A>C>B? C��B>A>C? D��B>C>A
�ο��𰸣�C
���������������������ԱȽϡ��ϻ��õĽ������Ѳ����õĽ��������Ӵ�����Һ���û�����������A����C����ԭ����нϻ��õĽ���������������B����A�������ȷ�Ĵ���C��
�����Ѷȣ�һ��
2��ѡ���� ��������ѧ����ίԱ�ὫԪ�����ڱ�ԭ�е������������ȡ�����������Ҹ�Ϊ18�У������Ϊ��1�У�ϡ������Ϊ��18�У�������涨������˵����ȷ����?
A��ԭ���������2�����ӵ�Ԫ��һ���ڵ�2��
B����2��12��Ԫ��ȫΪ����, ��3��Ԫ���������
C����15��Ԫ�ص�����������Ӧˮ����Ļ�ѧʽ��ΪH3RO4
D��115��Ԫ���ڵ�13�У�Ϊ����Ԫ��
�ο��𰸣�B
���������A����ȷ������He��������������2����λ�ڵ�18�У�����Ԫ�����ڱ��Ľṹ��֪������B��ȷ��C����ȷ�����絪Ԫ�ض�Ӧ����HNO3�����Ԫ�����ڱ�ȫ�������������һ��Ԫ�ص�ԭ��������118������115��Ԫ���ڵ�15�У�D����ȷ����ѡB��
�����������Ǹ߿��еij������㣬�����е��Ѷȵ����⣬���������ӱ��ע��֪ʶ��Ǩ�ƣ�����������ѧ����������������������Ҫ�ǿ���ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ�����������
�����Ѷȣ���
3���ƶ��� ����Ԫ��R�����������R2O 4.7g����95.3gˮ�У�������Һ����������Ϊ5.6%��Rԭ�Ӻ��к���20�����ӣ�����Ԫ��Q���䵥������ˮ���ҷ�Ӧ�ų�O2�����ܸ�R�γɵ��͵����ӻ�����RQ����ͨ��������
(1)R��Q��ΪʲôԪ��(д���Ƶ�����)��________________________________________��
(2)д��R��Q��Ԫ�����ڱ��е�λ�ã�________________________________________��
(3)��4.7g R2O���ڶ��ٿ�ˮ�У�ʹÿ50��ˮ��������1��R��(д���������)��________________________________________��
�ο��𰸣�(1)RΪKԪ�أ�QΪFԪ�ء�
(2)R�ڵ�4���ڢ�A�壬Q�ڵ�2���ڢ�A�塣
(3)90.9g
���������(1)��R�����ԭ������ΪM������ROH������Ϊx��
R2O��H2O?===����2ROH
2M��16����������2(M��17)
4��7g������������x

w(ROH)�� ��100%��5.6%
��100%��5.6%
M��39����Rԭ�Ӻ���������Ϊ39��20��19��ΪK������Q����ˮ��Ӧ�û�O2�����ܸ�R�γ����ӻ�����RQ����QΪ��1��Ԫ�أ�Ϊ��A�壬��QΪF��
(2)R�ڵ�4���ڣ���A�壻Q�ڵ�2���ڣ���A�塣
(3)K2O������H2O===2KOH
94g������18g������2mol
4��7g����m(H2O)��n(KOH)
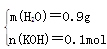
����ˮ��0.9g��0.1mol��50��18g/mol��90.9g��
���������⿼�����Ԫ�����ڱ���Ӧ�úͻ�ѧ��������ʣ���Ŀ�Ѷ��У�����ѧ�������ڱ������ճ̶ȼ���ѧ�����������
�����Ѷȣ�һ��
4������� ÿ��2�֣���10�֣�
������������Ԫ�صĵ��������ݣ���λ��kJ/mol�����ش�������⡣
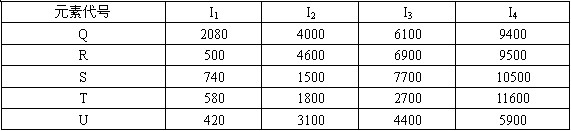
��1�������ڱ��У�����ܴ���ͬһ����ǣ�?��
A.Q��R? B.S��T? C.T��U? D.R��T? E.R��U
��2��������ǵ������Ȼ��������������缫��Ӧʽ�������ȷ���ǣ�?��
A.Q2����2e����Q? B.R2����2e����R? C.S3����3e����S
D.T3����3e����T?E.U2����2e����U
��3�����ǵ��Ȼ���Ļ�ѧʽ���������ȷ���ǣ�?��
A.QCl2? B.RCl? C.SCl3? D.TCl? E.UCl4
��4��SԪ��������ǣ�?��
A.S��Ԫ��? B.ϡ������Ԫ��? C.p��Ԫ��? D.����? E.d��Ԫ��
��5������Ԫ���У���ѧ���ʺ�������������QԪ�ص��ǣ�?��
A.��1s22s22p1�� B.�루1s22s2�� C.ﮣ�1s22s1��D.�⣨1s1��E?����1s2��
�ο��𰸣�(1)E(2)D(3)B(4)A(5)E
�����������1��ͬһ���壬��ѧ���ʾ��������ԣ�����Η�����ҵ��������������ǿ����С����E��R��U��
��2�����ݵ��������ݿ�֪T�ĵ�һ���ڶ����������������ʿ���ʧȥ3����������T3+����������������ԭ��Ӧ��T3����3e�� ��T��R��U��һ�����ܺ�С���ڶ������ܴܺ�����ʧȥ1�����ӣ�S���������ܴܺ�����ʧȥ2�����ӣ�Q�����ܴܺ�����ʧ���ӣ�
��3�������γɵ��Ȼ���ΪA��QCl3 B��RCl C��SCl2 D��TCl3 E��UCl����ѡ��B�
��4��S���������ܴܺ���������ʧȥ2�����ӣ��ʵ����Ų�����Ϊns2�����Կ�������S��Ԫ�أ�
��5��Q�����ܴܺ�����ʧ���ӣ����ڻ�ѧ���ʺ�������������QԪ���Ƕ������庤��1s2����
�����Ѷȣ���
5������� ��11�֣��±�ΪԪ�����ڱ���һ���֣����б�Ŵ�����Ӧ��Ԫ�ء�
��
| ?
| ?
| ?
| ?
| ?
|
?
| ��
| ?
| ��
| ��
| ��
| ��
| ?
| ?
|
��
| ?
| ?
| ?
| ?
| ?
| ��
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ��
| ?
| ?
| ?
| ?
| ��
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
| | | | | | | | | | | | | | | | | | | |
|
��ش��������⣺
��1��д��Ԫ�آߵļ۵����Ų�ͼ__________ �����ԭ�ӽṹʾ��ͼ__________��71��Ԫ������_______���ڣ�________�壬_______����
��2����Ԫ�آ٢ۢ��γɵ�ij������������Ԫ�ص�������Ϊ1��6��8���û����������������ܶ�Ϊ15���÷�������ԭ�ӵ��ӻ���ʽΪ______________��
��3���ܺ͢��γɵķ��ӹ���___________��
��4���۵�ij��ͬ�������屻��Ϊ����;��壬����ƽ���״�ṹ���þ����к��е�������Ϊ______________________________________��
��5��������γɵĻ�������۵�___________������γɻ�������۵㣨����ڡ����ڡ���
��6����ĵ�һ�γ���ͻ��ĵ�����������I2����������һ������ͻ��ĵ�����������_______��
�ο��𰸣�

�����������
�����Ѷȣ�һ��