微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某元素的一种核素X的质量数为A,含N个中子,它与35?Cl原子组成X35?Clm分子,则ag X35?Clm中所含质子的物质的量是(?)
A.(A-N+17m) mol
B.(A-N+17m) mol
C.(A-N) mol
D.(A-N) mol
参考答案:A
本题解析:中子数和质子数之和是质量数,所以该元素的质子数是A-N。所以ag X35?Clm中所含质子的物质的量是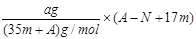 ,即选项A是正确的。
,即选项A是正确的。
本题难度:简单
2、填空题 按要求回答下列问题:
(1)画出第三周期核外未成对电子最多的基态原子的价电子排布图______________;
(2)写出族序数为周期数三倍的主族元素的原子电子排布式_____________________;
(3)用价层电子对互斥模型推测下列分子或离子的空间构型及中心原子的杂化方式。
SCl2 _________、__________;BeCl2_________、_________;
(4)写出所给微粒的一种等电子体的化学式:SO2 ?: ?SO42-___________.
参考答案:(16分) (1)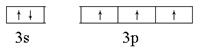 (2)1s22s2sp4?
(2)1s22s2sp4?
(3) V型 ; sp3?;直线型?;sp?(4)? O3; PO43-
本题解析:(1)第三周期核外未成对电子最多的基态原子是P元素,所以价电子排布图为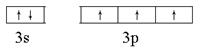 。
。
(2)族序数为周期数三倍的主族元素氧元素,其原子电子排布式为1s22s2sp4。
(3)根据价层电子对互斥理论可知,SCl2和BeCl2中中心原子含有的孤对电子对数分别是(6-2×1)÷2=2、(2-2×1)÷2=0,所以分子的空间构型分别是V型、sp3杂化和直线型、sp杂化。
(4)原子数和电子式分别都相等的是等电子体,则和二氧化硫互为等电子体的是臭氧。和SO42-互为等电子体的是PO43-。
点评:该题是高考中的常见题型,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑思维能力和抽象思维能力,提高学生分析问题、解决问题的能力。
本题难度:一般
3、选择题 短周期Y元素的p轨道上有3个未成对电子,则该元素的最高价氧化物的水化物的化学式可能是
A.H3YO4
B.H4YO4
C.HYO2
D.H2YO4
参考答案:A
本题解析:短周期Y元素的p轨道上有3个未成对电子,则该元素位于周期表的ⅤA族,最高价是+价,因此该元素的最高价氧化物的水化物的化学式可能是H3YO4,A正确;B、C和D中Y元素的化合价分别是+4价、+3价和+6价,均不正确,答案选A。
本题难度:一般
4、选择题 如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是
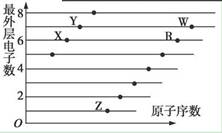
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:X>Y
D.X、Z形成的化合物中可能含有共价键
参考答案:D
本题解析:由题给关系图,推出X为O,Y为F,Z为Na,R为S,W为Cl。A选项,O和S不在同一周期,错误;B选项,同一周期从左到右原子半径依次减小,一般情况下电子层数多的元素半径大,S>Cl>O,错误;C选项,非金属性越强,气态氢化物越稳定,HF>H2O,错误;D选项,X、Z形成的Na2O2含有共价键,正确。
本题难度:一般
5、选择题 短周期金属元素A和非金属元素B,它们的简单离子为aAm+和bBn-,已知bBn-比aAm+多两个电子层,则a的取值可以是:①1 ?②2 ?③3 ?④4 ?⑤5
A.①②
B.③④
C.①④
D.③⑤
参考答案:B
本题解析:bBn-比aAm+多两个电子层,且二者都是短周期元素,则两种微粒的核外电子数相差是10个18-2=16个。又因为A是金属,所以A只能是第二周期的Li或Be元素,即a=3或4,答案选B。
点评:该题设计新颖,基础性强,注重单体的灵活性,有利于激发学生的学习兴趣和学习积极性。该题的关键是熟练掌握核外电子排布规律,然后结合题意灵活运用即可,有利于培养学生的逻辑思维能力和发散思维能力。
本题难度:一般