微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NH3和Cl2可快速反应:2NH3+3Cl2 →N2+6HCl 。有100LNH3和Cl2混合气体,充分反应后的混合气体中N2占混合气体的1/7,则N2的物质的量为(标准状况下数据)
A.0.263 mol
B.0.483 mol
C.0.663 mol
D.0.893 mol
参考答案:AD
本题解析:若按2NH3+3Cl2 →N2+6HCl 反应,生成混合气体中氮气刚好占了1/7,则生成氯化氢的体积为600/5=120L,氮气的体积为20L,物质的量为0.893mol。若氨气过量则有NH3+3Cl2→N2+6HCl,氨过量,所以还会生成氯化铵8NH3+3Cl2→N2 +6NH4Cl;剩余混合气体中氮气和氨气,设氯气体积为x,则氨气为100-x,剩余氨气为100-x-8x/3=100-11x/3,生成氮气的体积为x/3,根据(100-11x/3):x/3=6:1,解得x=17.64L,氮气的物质的量为0.263mol。答案选AD。
本题难度:一般
2、选择题 只给出下列甲中和乙中对应的量,不能组成一个求物质的量公式的是
选项
| 甲
| 乙
|
A
| 物质的粒子数
| 阿伏加德罗常数
|
B
| 标况下气体的体积
| 标况下气体摩尔体积
|
C
| 固体的体积
| 固体的密度
|
D
| 溶液的物质的量浓度
| 溶液的体积
参考答案:C
本题解析:考查物质的量的有关计算。根据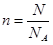 、 、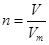 和n=cV可知,选项A、B、D都是正确的。选项C中只能计算出固体的质量,但不能计算固体的物质的量,答案选C。 和n=cV可知,选项A、B、D都是正确的。选项C中只能计算出固体的质量,但不能计算固体的物质的量,答案选C。
本题难度:一般
3、选择题 水的相对分子质量为18,则1个水分子的质量为( )?
A.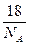
B.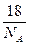 g・mol-1? g・mol-1?
C.18na g
D.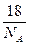 g g
参考答案:D?
本题解析:1 mol H2O的质量为18 g,而1 mol H2O中含有na个水分子,所以1个水分子的质量应为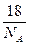 g。 g。
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.100mL 0.1mol・L-1的稀硫酸中含有SO42―个数为0.1NA
B.1molCH3+(碳正离子)中含有电子数为10NA
C.27g金属铝与足量的盐酸反应,铝失去电子数为3NA
D.12.4g白磷(分子式为P4)中含有磷原子数为1.6NA
参考答案:C
本题解析:A错,100mL 0.1mol・L-1的稀硫酸中含有SO42―个数为0.01NA;B错,1molCH3+(碳正离子)中含有电子数为8NA;C正确;D错,12.4g白磷的物质的量为0.1mol,含有磷原子数为0.4NA
本题难度:一般
5、计算题 工业上通过电解饱和的食盐水来制取氯气。现取100mL含NaCl为11.7g的饱和食盐水进行电解,
(1)写出电解饱和食盐水制取氯气的化学方程式
(2)在标准状况下制得Cl2多少升?
(3)所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
参考答案:
(1) 2NaCl + 2H2O =" 2NaOH" + Cl2↑+ H2↑? 2分
(2)2.24L (3分)?(3)2 mol/L? (3分)
本题解析:n(NaCl)=11.7÷58.5=0.2mol
2NaCl + 2H2O =" 2NaOH" + Cl2↑+ H2↑
0.2mol? 0.2mol 0.01mol
标准状况下制得Cl2体积为2.24L;所得NaOH的物质的量浓度c=" 0.2mol÷0.1L=2" mol/L
本题难度:简单
|