��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij�ּ״�ȼ�ϵ���Dz��ò���̼������Ϊ�缫��������ϡ������Һ��ֱ�Ӽ��봿����ļ״���ͬʱ��һ���缫ͨ��������ش��������⣺
��1���˵缫�����������ĵ缫��Ӧʽ��______________________�����������ĵ缫��Ӧʽ��______________________________��
��2�����Һ�е�������__________���ƶ��������·�ͷŵ��ӵĵ缫��___________����(������)
��3������ֱ��ȼ��ȼ�ϲ���������ʹ��ȼ�ϵ���������ŵ㣬������Ҫ�����㣺__________________________________________��
�ο��𰸣���1�� ��
��
��2����������
��3��ȼ�ϵ�ص�����ת��Ч�ʸߣ������˶Կ�������Ⱦ
���������
�����Ѷȣ�һ��
2������� MCFC��ȼ�ϵ�ؿ�ͬʱ��Ӧ���ˮ�������乤���¶�Ϊ600�桫700�棬����ȼ��ΪH2�������Ϊ���ڵ�K2CO3���õ�ص��ܷ�ӦΪ��2H2+O2?2H2O��������ӦΪ��H2+CO32-��H2O+CO2+2e-���������ƶ��У���ȷ���ǣ�?��
A��������ӦΪ4OH����2H2O+O2��+4e-
B�����������1molˮʱ��ת��4mol����
C���ŵ�ʱCO32-���ƶ�
D��ͨH2��һ��Ϊ������������ԭ��Ӧ
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
3������� (14��)�������仯�����ڿ��м������о�������Ҫ��Ӧ�á�
��1��ij����ѧϰС�����Ʊ�����NO���壬д������������ϡ���ᷴӦ�Ʊ�NO�����ӷ���ʽ�� ��
��2��LiFePO4��һ�����Ͷ���﮵�صĵ缫���ϡ�
����ͼΪijLiFePO4��س䡢�ŵ�ʱ�����ֲ��Ŵ�ʾ��ͼ��д���õ�طŵ�ʱ������Ӧ����ʽ�� ��
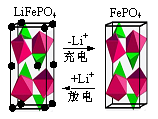
�ڽ�LiOH��FePO4��2H2O���װ�ɫ���壩�뻹ԭ�������ǰ�һ����������ϣ���N2�и��±��տ��Ƶ�﮵����������LiFePO4�����չ�����N2�������� ��ʵ��������Fe3+Ϊԭ���Ƶõ�FePO4��2H2O��ʱ�Ժ��ɫ��FePO4��2H2O�л��е����ʿ���Ϊ ��
��3����������Ҫ��������ת����ͼ��ʾ��
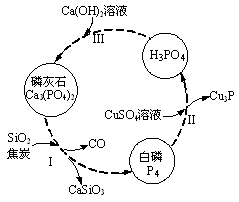
�ٲ����Ϊ���Ĺ�ҵ��������֮һ����Ӧ��1300��ĸ���¯�н��У�����SiO2������������������CaSiO3������̿�������� ��
�ڲ���������մ��Ƥ���ϣ�����0.2mol/L CuSO4��Һ��ϴ�����ݲ������жϣ�1mol CuSO4���������İ������ʵ���Ϊ ��
�۲�����У���Ӧ��ı�����ͬ�ɻ�ò�ͬ�IJ����Ca3(PO4)2����ܵIJ��ﻹ�� ��
�ο��𰸣���1�� Fe+4H+ +NO3- = Fe3+ +NO�� +2H2O������ƽ��1�֣�
��2���� Li++FePO4+e-=LiFePO4
�� ��ֹ���ɵ�Fe2+�ڿ��������±����� Fe(OH)3��������������
��3���� ����ԭ�� �� 0.05mol����д��λ��1�֣� ��Ca (H2PO4)2��CaHPO4��ÿ��1�֣�
(ÿ��2�֣���14��)
�����������1������Fe��ϡ���ᷴӦ������������NO��ˮ�����ӷ���ʽ��Fe+4H+ +NO3- = Fe3+ +NO�� +2H2O��
��2������ͼ��֪���ŵ�ʱ������FePO4�õ����ӣ����Li+������LiFePO4�����Էŵ�ʱ������Ӧʽ��Li++FePO4+e-=LiFePO4
����Ϊ�����е������װ�LiFePO4�е�������������Ϊ�����ӣ������ڵ����ķ�Χ������ȡ�缫���ϣ�ʵ��������Fe3+Ϊԭ���Ƶõ�FePO4��2H2O��ʱ�Ժ��ɫ����������������ɫΪ���ɫ������FePO4��2H2O�е����ʿ�����Fe(OH)3��
��3������Ϊ����I���������ķ�Ӧ��������������������������ƣ���̿�������ǽ�PԪ�ػ�ԭ����������������ΪCO�����Խ�̿������������ԭ����
�ڸ��ݲ���II������������ͭ��Һ��Ӧ����Cu3P�����ᣬ1mol����ͭת��ΪCu3P���õ�1mol���ӣ��������PԪ�صĻ��ϼ����ߵ�+5�ۣ��������Pԭ�ӵ����ʵ�����0.2mol�����ķ���ʽ��P4������1mol����ͭ�������������ʵ�����0.2/4mol=0.05mol��
����������Ԫ�ᣬ�������Ƶ�����ͬ�õ��IJ���Ҳ��ͬ��������Ca3(PO4)2�����⣬����������2����ʽ�Σ�Ca (H2PO4)2��CaHPO4��
���㣺������������ʵķ����жϣ�������ԭ��Ӧ�е�ʧ�����غ���ɵ�Ӧ�ã���Ӧ������ж�
�����Ѷȣ�����
4������� ���Խ�������ԭ��Ӧ2H2��O2===2H2O��Ƴ�ԭ��ء�
(1)��������������������������Һ����ȼ�ϵ�أ���ͨ�������Ӧ��________������ͨ����������________���缫��ӦʽΪ������________________������________________��
(2)���KOH��Ϊϡ����������ʣ���缫��ӦʽΪ������ ������__________________________��
(3)(1)��(2)�ĵ����Һ��ͬ����Ӧ���к�����Һ��pH���кα仯�� ��
(4)���H2��Ϊ���飬KOH��Һ���������Һ����缫��ӦʽΪ������____________________________������________________________________��
�ο��𰸣�(1)H2��O2��O2��2H2O��4e����4OH����H2��2OH����2H2O��2e��
(2)O2��4H����4e����2H2O��H2��2H����2e��
(3)ǰ�߱�С�����߱��
(4)2O2��4H2O��8e����8OH����CH4��10OH����CO32����7H2O��8e��
���������(1)���ݵ�ط�Ӧʽ��֪�ڷ�Ӧ��H2��������O2����ԭ��H2Ӧ���ڸ����Ϸ�Ӧ��O2Ӧ���������Ϸ�Ӧ������Ϊ�Ǽ�����Һ����������H���μӻ����ɣ��ʸ����ĵ缫��ӦΪH2��2OH����2H2O��2e���������ĵ缫��ӦΪO2��2H2O��4e����4OH����
(2)�����������ʻ�Ϊ������Һ����ʱӦ���Dz�������OH�����ɣ��ʸ����ĵ缫��ӦΪH2��2H����2e���������ĵ缫��ӦΪO2��4H����4e����2H2O��
(3)����ǰ���ڼ��������·�Ӧ��KOH�������䣬������ʱH2O���࣬����Һ��ϡ��pH����С��������Ϊ����Һ��H2SO4�������䣬H2O���࣬����Һ��ϡ��pH�����
(4)���H2��Ϊ���飬KOH��Һ������ʣ�������Ϊ2O2��4H2O��8e����8OH������ʱ������CO2�ų�������ΪCH4��10OH����CO32����7H2O��8e����
���㣺��������ȼ�ϵ�ص��жϡ��缫��Ӧʽ����д
���������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ������Ҫ�ǿ���ѧ����ԭ���ԭ������Ϥ�˽�̶ȣ������ڵ���ѧ���������������ͷ�ɢ˼ά���������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷԭ��صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
5������� ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ������������ǿ�������ȶ�����ش�
��1������ȼ�ϵ�ص�����ת����Ҫ��ʽ��______���ڵ����е�����������Ϊ______����a��b��ʾ����
��2��������ӦʽΪ______��
��3���õ�ع���ʱ��H2��O2�������ⲿ��������ؿ����������ṩ���ܣ���ˣ�������ȫ�����ǹؼ�����֮һ���������һ����Ҫ�Ĵ�����ϣ�����ͷ���ԭ�����£�
��2Li+H2
2LiH
��LiH+H2O�TLiOH+H2��
�ٷ�Ӧ���еĻ�ԭ����______����Ӧ���е���������______��
����֪LiH�����ܶ�Ϊ0.82g/cm3���������224L����״����H2�����ɵ�LiH����뱻���յ�H2�����Ϊ______��
���ɢ����ɵ�LiH��H2O���÷ų���H2�������ȼ�ϣ�������ת����Ϊ80%��������ͨ�����ӵ����ʵ���Ϊ______��
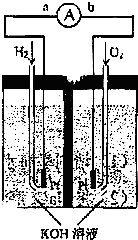
�ο��𰸣���1������Ŀ�У�����ȼ�ϵ�صĹ���ԭ������ԭ���ԭ�����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã���ԭ����У�������������������ͨ��ȼ�������ĵ缫�Ǹ�����ͨ�����ĵ缫�����������Ե�����a��b���ʴ�Ϊ����ѧ��ת��Ϊ���ܣ���a��b��
��2��ȼ�ϵ���У�ͨ��ȼ�������ĵ缫�Ǹ���������ʧ���ӵ�������Ӧ����2H2+4OH--4e-�T4H2O��H2+2OH--2e-�T2H2O��
�ʴ�Ϊ��2H2+4OH--4e-�T4H2O��H2+2OH--2e-�T2H2O��
��3����Li���������+1�ۣ�����ԭ����H2O��H��+1����H2�е���ۣ������������ʴ�Ϊ��Li��H2O��
���ɷ�ӦI��������10molH2ʱ��������20molLiH��V=m��=20��7.9g0.82��103L=197.5��10-3L��V(LiH)V(H2)=197.5��10-3L224L=8.82��10-4���ʴ�Ϊ��8.82��10-4��
��20molLiH������20molH2��ʵ�ʲμӷ�Ӧ��H2Ϊ20mol��80%=16mol��1molH2ת����1molH2O��ת��2mol���ӣ�����16molH2��ת��32mol�ĵ��ӣ��ʴ�Ϊ��32mol��
���������
�����Ѷȣ�һ��