微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氯酸钾多用来制造火柴和烟花等。电解法是工业制造氯酸钾的主要方法:电解热的氯化钠水溶液,电解的生成物相互反应制得氯酸钠;再以氯酸钠和氯化钾为原料制备氯酸钾。
(1)写出电解时的电极反应方程式阴极:____________________________,阳极:_____________________________。
(2)电解的生成物相互反应生成氯酸钠的化学方程式为__________________________。
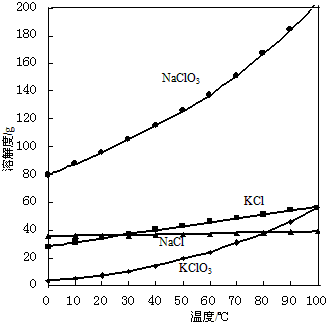
(3)几种物质的溶解度曲线如下图所示,低温有利于析出KClO3晶体,原因是:
_________________________________
(4)产品KClO3中常含有其他杂质离子,提纯的方法是_______________。
(5)该生产工艺可以循环利用的物质是__________,副产品是__________。
参考答案:(1)2H++2e-==H2↑;2Cl--2e-== Cl2↑
(2)3Cl2+6NaOH==NaClO3+5NaCl+3H2O
(3)KClO3的溶解度随温度降低而降低,低温时KClO3在四种物质中溶解度最小
(4)重结晶
(5)NaCl;H2
本题解析:
本题难度:困难
2、填空题
研究化学反应原理对于生产生活是很有意义的。
(1)25℃时,醋酸溶液中CH3COOH CH3COO-+ H+;Ka= 1.75×10-5 mol/L,若向0.10 mol/LCH3COOH溶 液中加入一定量的固体CH3COONa(假设溶液体积不变),若溶液中c(CH3COO-)为1.0 mol/L,则溶液中c(H+)=_______mol/L(计算结果保留小数点后两位数字)。溶液中各种离子浓度关系是__________。
CH3COO-+ H+;Ka= 1.75×10-5 mol/L,若向0.10 mol/LCH3COOH溶 液中加入一定量的固体CH3COONa(假设溶液体积不变),若溶液中c(CH3COO-)为1.0 mol/L,则溶液中c(H+)=_______mol/L(计算结果保留小数点后两位数字)。溶液中各种离子浓度关系是__________。
(2)牙釉质对牙齿起着保护作用,其主要成分为Ca5(PO4)3OH,该物质在水中存在沉淀溶解平衡,试写出该物质的溶度积常数表达式Ksp=_____________。
(3)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。

①该电解槽的阳极反应式为________,通过阴离子交换膜的离子数________(填“>”“<”或“=”)通 过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为________;
③电解一段时间后,B口与C口产生气体的质量比为__________
参考答案:(1)1.75×10-6;c(CH3COO-)> c(Na+)>c(H+)>c(OH-)
(2)c5(Ca2+)・c3(PO43-)・c(OH-)
(3)①4OH--4e-=2H2O+O2↑;<;②b<a<c<d;③8:1
本题解析:
本题难度:困难
3、选择题 某同学组装了如图所示的电化学装置,电极Ⅰ为 Zn,电极Ⅱ为Cu,其他电极均为石墨,则下列说法正确的是
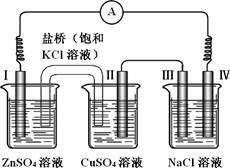
A.电流方向:电极Ⅳ →○→电极ⅠB.盐桥中的K+会移向ZnSO4溶液
C.处得到标况下气体2.24L,电极II上析出6.4g固体
D.NaCl溶液中,电极Ⅲ制得氯气,电极Ⅳ制得金属钠
参考答案:AC
本题解析:A、装置中左边两个烧杯构成为原电池,锌做原电池的负极,铜为原电池的正极,电流从铜电离流出经过电流表流向锌,所以选A;B、盐桥中钾离子向阴极负极移动,即流向硫酸铜溶液,不选B;C、第三个烧杯是电解氯化钠溶液,电极Ⅲ为电解池的阳极,产生氯气,当有2.24升氯气产生时有2.24/22.4摩尔氯气,有0.2摩尔电子转移,所以电极II上析出0.1摩尔铜,即析出6.4g固体,选C;D、氯化钠溶液中电解得到氯气和氢气和氢氧化钠,没有得到金属钠,不选D。
考点:原电池和电解池的原理的应用。
本题难度:一般
4、填空题 如图所示,若电解5min时,C中铜电极质量增加4.32g,试回答
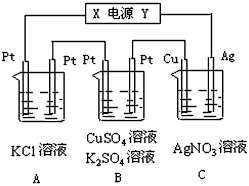
(1)电源电极X名称为________。
(2)各池pH值的变化A________ B_________、C__________。(填“增大”、“减小”或“不变” )
(3)通电5min后,B池中共收集到448mL气体(标况),溶液体积为200mL(假设反应前后溶液体积不变化),则通电前硫酸铜溶液的物质的量浓度为______________。
(4)常温下若A池中KCl溶液的体积仍是40mL,电解生成的气体全部排出, 电解后溶液的pH 值是_________。如果想使反应溶液恢复到原来状态,应该向B池中加入________,其质量为_________。
参考答案:(1)负极
(2)增大;减小;不变
(3)0.05mol/L
(4)14;Cu(OH)2(或CuO、H2O);0.98g(0.8g、0.18g)
本题解析:
本题难度:一般
5、选择题 将0.1 L含有0.02mol CuSO4和0.01molNaCl的水溶液用惰性电极电解。电解一段时间后,一个电极上得到0.01 mol Cu,另一电极析出的气体
A.只有Cl2
B.只有O2
C.既有Cl2又有O2
D.只有H2