微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 化合物A是一种不稳定的物质,它的分子组成可用OxFy来表示,10mLA气体能分解生成15mLO2和10mLF2(同温同压下)。则:
(1)我们可以通过计算来确定A的化学式为 ,摩尔质量为 g/mol
(2)已知A分子中x个氧原子呈…―O―O―O―…链状排列,则A分子的电子式是 ,
结构式是 。
参考答案:(1) O3F2 86 g/ mol (2) F―O―O―O―F
F―O―O―O―F
本题解析:
试题解析:(1)根据原子守恒配平方程式,
OxFy = x/2O2 + y/2F2,
1×22.4L x/2×22.4L y/2×22.4L
10mL 15mL 10mL
所以x=3;y=2;故答案为:O3F2(2)该分子中含3个O原子,根据“A分子中X个氧原子是…-O-O-O-…链状排列”知,两个F原子位于该分子的两端,所以该分子的结构式为F-O-O-O-F,电子式为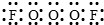 .故答案为:
.故答案为: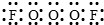 ,F-O-O-O-F。
,F-O-O-O-F。
考点:方程式的计算 电子式 结构式
本题难度:一般
2、选择题 设NA为阿伏伽德罗常数的数值,则下列说法中正确的是
①2.24L氨气含有NA个电子,②1.4g乙烯与丙烯的混合气体含有NA个碳原子,③精炼铜,?若阳极失去2NA个电子,则阴极增重64g,④标准状况下,22.4L空气含有NA个分子,⑤过氧化钠与水反应,若电子转移4NA,则产生的氧气为32 g,⑥将1L 2mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA,⑦在1L 0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA
A.②③④⑦
B.①③④⑦
C.②③④⑤⑦
D.②④⑤⑦
参考答案:A
本题解析:①不正确,因为不一定是在标准状况下;乙烯和丙烯的最简式相同,都是CH2,所以1.4g含有0.1mol碳原子,②正确;根据电荷守恒可知,③正确;根据阿伏加德罗定律可知,④正确;过氧化钠中氧元素是-1价的,所以如果转移4Na个电子,则生成氧气2mol,质量是64g,⑤不正确;生成氢氧化铁胶体的反应是可逆反应,转化率达不到100%,⑥不正确;根据碳酸钠的水解方程式CO32-+H2O HCO3-+OH-可知,选项⑦正确,所以答案选A。
HCO3-+OH-可知,选项⑦正确,所以答案选A。
本题难度:一般
3、填空题 Ⅰ.(3分)下列物质中:①氯化钠?②干冰?③盐酸?④铜?⑤硫酸钡?⑥蔗糖
⑦I2?⑧熔融的硝酸钾?⑨食盐水
(1)能导电的是(填编号,下同)?;
(2)属于电解质的是?;
(3)属于非电解质的是?。
Ⅱ.(6分)100mL 1 mol・L-1Al2(SO4)3溶液中含SO42-离子?个,含Al3+离子?mol。0.6mol O2与0.4mol O3质量之比为?,分子个数之比为?,原子个数之比?,它们在同温同压下的体积比是?。
参考答案:Ⅰ(3分)(1)③④⑧⑨?(2)①⑤⑧?(3)②⑥?(各1分)
Ⅱ.(6分)1.806×1023 (或0.3NA) ;? 0.2;? 1:1;? 3:2;? 1:1;? 3:2 (各1分)
本题解析:根据导电原因、电解质、化合物的定义判断.能导电的物质必须含有自由电子或自由离子.
电解质:在水溶液里或熔融状态下能导电的化合物.该定义的前提必须是化合物。
非电解质:在水溶液里或熔融状态下都不能导电的化合物.该定义的前提必须是化合物。
①氯化钠是电解质,但?没有自由电子或自由离子,所以不导电 ;
②干冰是非电解质,因没有自由电子或自由离子,所以不导电;
③盐酸?是混合物,但溶液中含有自由离子,所以能导电;
④铜是单质,所以既不是电解质也不是非电解质,铜中有自由电子,所以能导电;
⑤硫酸钡是电解质,但?没有自由电子或自由离子,所以不导电;
⑥蔗糖是非电解质,因没有自由电子或自由离子,所以不导电;
⑦I2是单质,所以既不是电解质也不是非电解质 ,因没有自由电子或自由离子,所以不导电;
⑧熔融的硝酸钾是电解质,有自由电子或自由离子,所以导电;
⑨食盐水是混合物,但溶液中含有自由离子,所以能导电;
Ⅱ.100mL 1 mol・L-1Al2(SO4)3溶液中含SO42-离子:0.1L?1mol/L?3?6.02?1023=1.806×1023;含Al3+离子0.1L?1mol/L?2=0.2mol;
0.6mol O2与0.4mol O3质量之比为:0.6?32:0.4?48=1:1,
分子个数之比等于物质的量之比:0.6:0.4=3:2,
原子个数之比:0.6?2:0.4?3=1:1,它们在同温同压下的体积比等于物质的量之比:0.6:0.4=3:2
点评:掌握有关物质的量的计算公式。
本题难度:一般
4、填空题 (4分)将00C 101KPa条件下的氯化氢(HCl)气体44.8L,通入492mL水中,(已知水的密度为:1.00g/mL),得到密度为1.13g/mL的盐酸(即氯化氢的水溶液)。[
(1)求此盐酸的质量分数?(计算结果保留一位小数)
(2)求此盐酸的物质的量浓度? (计算结果保留一位小数)
参考答案: (1) 12.9%? (2)4.0moI/L
(1) 12.9%? (2)4.0moI/L
本题解析:略
本题难度:简单
5、选择题 下列有关阿佛加德罗常数(N A)的说法错误的是
A)的说法错误的是
A.32克O2所含的原子数目为NA
B.0.5molH2O含有的原子数目为1. 5NA
5NA
C.1molH2O含有的H2O分子数目为NA
D.0.5NA个氯气分子的物质的量是0.5mol
参考答案:A
本题解析:略
本题难度:一般