微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 2.1 g CO在足量的O2中充分燃烧,然后通过足量的Na2O2固体,固体增加的质量为(?)

A.7.2 g
B.4.2 g
C.3.3 g
D.2.1 g
参考答案:D
本题解析:略
本题难度:简单
2、选择题 将3.2克H2和CO的混合气体(其密度为相同条件下氧气密度的1/2),通入一盛有足量Na2O2密闭容器中,再通入过量O2,并用电火花点燃使其充分反应,最后容器中固体的质量增加了
A.3.2g
B.4.4g
C.5.6g
D.6.4g
参考答案:A
本题解析:CO与氧气反应:2CO+O2 =2CO2,二氧化碳与过氧化钠反应:2CO2+2Na2O2=2Na2CO3+O2,总方程式为2CO+2Na2O2=2Na2CO3,固体增加的质量为CO的质量,氢气与氧气反应:2H2+O2 =2H2O,Na2O2与H2O反应:2H2O+2Na2O2=4NaOH+O2,总方程式为:2H2+2Na2O2=4NaOH,固体增加的质量为氢气质量,则CO和H2的混合气共3.2g与足量的Na2O2于密闭容器中,通入氧气用电火花点燃,充分反应后,固体增重质量是3.2g,故选A。2、H2O与Na2O2生成固体质量的变化分析规律,是解答该题的关键。
本题难度:一般
3、实验题 某实验小组把CO2通入饱和Na2CO3溶液制取NaHCO3,装置如图所示(气密性已检验,部分夹持装置略):
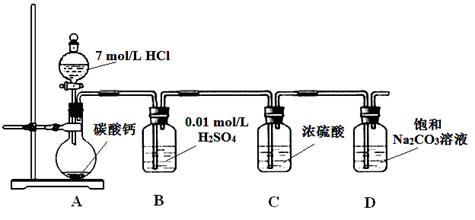
(1)D中产生NaHCO3的化学方程式是?。
(2)请结合化学平衡移动原理解释B中溶液的作用?。
(3)当D中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。为确定固体的成分,实验小组设计方案如下(称取一定质量的固体,配成1000 mL溶液作为样液,其余固体备用):
① 方案1:取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀。
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是 ?。
② 方案2:取样液与BaCl2溶液混合,出现白色沉淀并有气体产生。
实验小组认为固体中存在NaHCO3,其离子方程式是?。
该小组认为不能确定是否存在Na2CO3,你认为该结论是否合理?_____。
③ 方案3:实验小组中甲、乙同学利用NaHCO3的不稳定性进行如下实验:
甲同学:取样液400 mL,用pH计测溶液pH,再水浴加热蒸发至200 mL,接下来的操作是?,结果表明白色固体中存在NaHCO3。为进一步证明白色固体是否为纯净的NaHCO3,结合甲同学实验,还应补充的实验是?。
乙同学:利用仪器测定了固体残留率随温度变化的曲线,如下图所示。
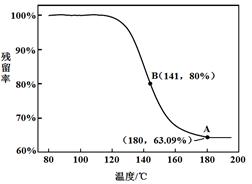
a. 根据A点坐标得到的结论是?。
b. 根据B点坐标,计算残留固体中n(NaHCO3:n(Na2CO3))=?。
通过上述实验,该小组认为,可以向饱和Na2CO3溶液中通入过量CO2制备NaHCO3。
参考答案:(1)Na2CO3+CO2+H2O = 2NaHCO3 (2分)
(2)CO2在水中存在平衡:CO2+H2O H2CO3
H2CO3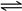 HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体(2分)
HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体(2分)
(3)① Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO3。(2分)
② 2HCO3-+Ba2+=BaCO3↓+ CO2↑+H2O(2分)
合理(1分)
③ 接下来的操作:冷却到室温,加水至溶液体积为400 mL,再次测定pH(2分)
补充实验:取相同质量的纯净的N aHCO3配成1000 mL溶液,取400 mL,重复甲的实验,进行对照。(2分)
a.白色固体为NaHCO3(2分)
b.71:42(或1.69)(1分)
本题解析: A装置中反应制备CO2,其中有杂质HCl、H2O(g),B装置既减少CO2的溶解,又能吸收HCl,C装置干燥CO2,D装置制备碳酸氢钠。(3)Na2CO3和NaHCO3都能和Ca(OH)2反应生成白色沉淀,方案1不合理,方案2 Na2CO3和BaCl2反应有白色沉淀,NaHCO3和BaCl2反应有白色沉淀和气体,因此可以确定NaHCO3存在,但不能确定Na2CO3的存在。方案3 Na2CO3和NaHCO3溶液都显碱性,但水解程度不同,可通过比较PH值前后大小进行区别。乙同学在温度为180时,残留率正好符合NaHCO3完全分解的计算,B点根据差量法进行计算,设原来有100克NaHCO3,反应后剩余80克,减少20克是CO2和H2O的质量,列方程组计算。
本题难度:困难
4、选择题 在273K、101.73kPa条件下,2L的CO和H2以任意比例混合,在电火花不断的引燃下,通入112mL的O2使之燃烧,将生成的产物通过足量的Na2O2粉末,则反应后气体的体积为(?)
A.2L
B.112mL
C.1.776mL
D.无法确定
参考答案:B
本题解析:根据发生的反应的方程式可找出解题的突破口,在电火花不断的引燃下,2CO+O2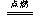 2CO2,2Na2O2+2CO2 = 2Na2CO3+O2,将两个方程式叠加得:Na2O2+CO=Na2CO3,即被CO“吸收”O2又“释放”出来;同理,2H2+O2
2CO2,2Na2O2+2CO2 = 2Na2CO3+O2,将两个方程式叠加得:Na2O2+CO=Na2CO3,即被CO“吸收”O2又“释放”出来;同理,2H2+O2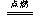 2H2O,2Na2O2+2H2O = 4NaOH+O2↑,将这两个方程式也叠加得:Na2O2+H2 = 2NaOH,故被H2O“吸收”O2又“释放”也出来;。因此,本题中反应后气体的体积仍为原O2的体积。故选B项。
2H2O,2Na2O2+2H2O = 4NaOH+O2↑,将这两个方程式也叠加得:Na2O2+H2 = 2NaOH,故被H2O“吸收”O2又“释放”也出来;。因此,本题中反应后气体的体积仍为原O2的体积。故选B项。
本题难度:简单
5、选择题 某同学用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),则下列分析推理中不正确的是( )
?
| 50 mL盐酸
| 50 mL盐酸
| 50 mL盐酸
|
m(混合物)
| 9.2 g
| 15.7 g
| 27.6 g
|
V(CO2)(标准状况)
| 2.24 L
| 3.36 L
| 3.36 L
|
A.盐酸的物质的量浓度为3.0 mol・L-1
B.根据表中数据能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2 g时盐酸过量
D.15.7 g混合物恰好与盐酸完全反应
参考答案:D
本题解析:由表中数据得出第1组中盐酸过量,第2、3组中盐酸不足,全部与HCO3-反应放出CO2。c(HCl)==3 mol・L-1,A选项正确;由第1组数据列方程式可求出NaHCO3的质量分数,B选项正确,加入混合物9.2 g时盐酸过量,C项正确;13.8 g混合物恰好与盐酸完全反应,D项不正确。
本题难度:一般