��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
��1������ȼ�շų��������ȣ�����Ϊ��Դ������������������
��֪��
��2CH4��g��+3O2��g��=2CO��g��+4H2O��l����H1=-1214kJ/mol
��2CO��g��+O2��g��=2CO2��g����H2=-566kJ/mol
���ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ______��
��2��������ʯī�缫����KOH��Һ�У��������ֱ�ͨ��CH4��O2�����ɼ���ȼ�ϵ�أ��为���缫��Ӧʽ�ǣ�______��
��3��ijͬѧ���ü���ȼ�ϵ�������һ�ֵ�ⷨ��ȡFe��OH��2��ʵ��װ�ã�����ͼ��ʾ����ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ������˵������ȷ����______������ţ�
A����Դ�е�aһ��Ϊ������bһ��Ϊ����
B��������NaCl��Һ��Ϊ���Һ
C��A��B���˶������������缫
D�����������ķ�Ӧ�ǣ�2H++2e-=H2��
��4������ͬ����CO��g����H2O��g���ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У����з�Ӧ��CO��g��+H2O��g��
CO2��g��+H2��g�����õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min
H2O
CO
CO2
1
650
2
4
1.6
5
2
900
1
2
0.4
3
3
900
1
2
0.4
1
|
��ʵ��1�У���v?��H2����ʾ��ƽ����Ӧ����Ϊ______��
��ʵ��3��ʵ��2��ȣ��ı������������______����һ��������ɣ���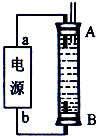
�ο��𰸣���1���ɢ�2CH4��g��+3O2��g��=2CO��g��+4H2O��l����H1=-1214kJ/mol
��2CO��g��+O2��g��=2CO2��g����H2=-566kJ/mol
���ݸ�˹���ɣ��ɢ�+��2�ɵü���ȼ���ȵ��Ȼ�ѧ��Ӧ����ʽΪCH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890KJ��mol-1��
�ʴ�Ϊ��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890KJ��mol-1��
��2���������ȼ�ϵ���У�����Ϊ������ʧȥ���ӷ���������Ӧ��������ӦΪCH4-8e-+10OH-�TCO32-+7H2O��
�ʴ�Ϊ��CH4-8e-+10OH-�TCO32-+7H2O��
��3��ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ����ͼ��֪BӦΪ��������BΪFe�缫��AΪ�����������ӷŵ磬
A����Դ�е�a��A��������aΪ������b��B��������bΪ��������A����
B��������NaCl��Һ��Ϊ���Һ�����������ӷŵ����ɼ��B��ȷ��
C��A�ĵ缫������ѡ����B�缫һ��ΪFe����C����
D�����������ӷŵ磬��缫��ӦΪ2H++2e-=H2������D��ȷ��
�ʴ�Ϊ��BD��
��4�������ɱ����е����ݿ�֪��v?��CO��=1.6mol2L5min=0.16mol/��L?min�����ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v?��H2��=0.16mol/��L?min����
�ʴ�Ϊ��0.16mol/��L?min����
��ʵ��3��ʵ��2��ȣ���ʼ�¶ȡ�Ũ�Ⱦ���ͬ����ƽ��Ũ����ͬ����ʵ��3�ķ�Ӧ���ʴ������ʹ���˴�����������ѹǿ�ȣ�
�ʴ�Ϊ��ʹ���˴�������Ӵ���ѹǿ����
���������
�����Ѷȣ���
2������� ��6�֣���֪����a��2H2(g)+O2(g)=2H2O(g) ��H = -Q1
(b)2H2(g)+O2(g)=2H2O��1�� ��H = -Q2
(c)2CO(g)+O2(g)=2CO2(g) ��H = -Q3
��1��Q1 (��>��=��<)Q2����Ϊ ��
��2��CO��H2�ֱ�ȼ������CO2��H2O��g�������õ���ͬ������������CO��H2��������ǣ� ��
�ο��𰸣���6�֣���1��<,H2O(g)=H2O(l) ��H<0 ��2��Q1/Q3
�����������1������Һ̬ˮʱ��������̬ˮ�ų��������࣬����Q1<Q2����2���õ���ͬ������������CO��H2������ȵ��������ʵ���֮�ȣ�����������Ϊ1������CO�����ʵ���Ϊ2/Q3����H2�����ʵ���Ϊ2/Q1�����ʵ���֮��ΪQ1/Q3 ��
���㣺��Ӧ�ȵļ���
�����Ѷȣ�һ��
3��ѡ���� �����Ȼ�ѧ����ʽ��S��s��+O2��g��=SO2��g����H=-297.23kJ/mol��������˵������ȷ���ǣ�������
A��S��g��+O2��g��=SO2��g��|��H|��297.23kJ/mol
B��S��g��+O2��g��=SO2��g��|��H|��297.23kJ/mol
C��1molSO2��g�������е���������1molS��s����1molO2��g�������е�����֮��
D��1molSO2��g�������������1molO2��g�����������
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4��ѡ���� 2011��3��9�գ����������֡��ź���ɻ������������һ�η���ʹ�����ڷ���������Ϻ���������½��δ���ĺ���Ƽ��ֽ������µ�ƪ�£���״Һ�⣨��Ҫ�ɷ���H2��CH4����������δ�������ػ���Ϳռ�����ϵͳ��ʵ���ã�101kPaʱ��1mol?H2��ȫȼ������Һ̬ˮ���ų�285.8kJ��������1mol?CH4��ȫȼ������Һ̬ˮ��CO2���ų�890.3kJ������������˵�����Ȼ�ѧ����ʽ��д��ȷ���ǣ�������
A����״Һ��ı�ȼ���ȱȼ���Ҫ��
B��CH4��g��+2O2��g���TCO2��g��+2H2O��l������H=-890.3kJ?mol-1
C��һ��H2��ѹ����Һ̬��ʽ���棬��Һ��ȼ��Ч��������Ҫ�ã��ͷ���������
D��2H2��g��+O2��g���T2H2O��l������H=-285.8kJ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
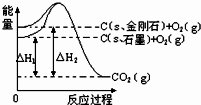
5��ѡ���� ��ͼ��ʾ����H1=-393.5kJ?mol-1��H2=-395.4kJ?mol-1������˵�����ʾʽ��ȷ���ǣ�������
A��C��s��ʯī��=C��s�����ʯ����H=+1.9kJ?mol-1
B��ʯī�������Ƚ��ʯ��
C�����ʯ���ȶ���ǿ��ʯī
D�����ʯȼ�յ��Ȼ�ѧ����ʽΪ��C��s�����ʯ��+O2��g��=CO2��g����H=395.4kJ?mol-1