��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��A��B���������ȵ�������A�������ݻ����䣬B�����Ļ������ϡ��»�������������ѹǿ��ȡ�����ͬ�����£��������ʵ�����NO2ѹ���ݻ���ͬ��A��B�������н��з�Ӧ: 2NO2 N2O4(����ӦΪ���ȷ�Ӧ)�����á�>����<����=����գ�
N2O4(����ӦΪ���ȷ�Ӧ)�����á�>����<����=����գ�
��1����Ӧ��ʼʱ������N2O4������vA_______vB��
��2����Ӧ�����У�����N2O4������vA_______vB��
�ο��𰸣���1��=
��2��<
���������
�����Ѷȣ�һ��
2��ѡ���� ��þ��Ͷ�뵽ʢ������ij������������H2��������ͼ��ʾ�������������У�Ӱ��O��t1ʱ��η�Ӧ���ʵ���Ҫ������(����)
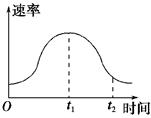
A�������Ũ��
B��þ���ı����
C��Cl����Ũ��
D����Һ���¶�
�ο��𰸣�D
������������ڷ�Ӧ�Ƿ��ȷ�Ӧ��������Һ���¶��淴Ӧ�Ľ��ж����ߣ��¶�Խ�ߣ���Ӧ����Խ�����Դ�ѡD��
�����Ѷȣ�һ��
3��ѡ���� ��þ��Ͷ��ʢ��ϡ�������������������У�����������������й�ϵ���ǣ�������
A�������Ũ��
B��þ��������
C���¶�
D����Һ�������ӵ�Ũ��
�ο��𰸣�A�����������Ũ�ȣ�H+Ũ������Ӧ��������A��ȷ��
B��Ӱ�췴Ӧ���ʵ����ؿ�����þ�ı����������״��ͬ��þ��������С�뷴Ӧ�����أ���B����
C�������¶ȣ���Ӧ��������C��ȷ��
D����Ӧ��ʵ����Mg+2H+=Mg2++H2������Һ�������ӶԷ�Ӧ����û��Ӱ�죬��D����
��ѡAC��
���������
�����Ѷȣ�һ��
4��ѡ���� ��þ��Ͷ�뵽ʢ������ij��������У�����H2�����ʿ�����ͼ��ʾ�������������жԲ���H2����û��Ӱ����ǣ�������
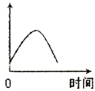
A��H+��Ũ��
B��þ���ı����
C����Һ���¶�
D��Cl-��Ũ��
�ο��𰸣���ͼ��֪������H2������������С��ΪMg+2H+�TMg2++H2��
A����ʼ�����Ũ�Ƚϴ�Ӧ���ʿ죬���淴Ӧ�Ľ��У�Ũ�ȼ�С����Ӧ���ʼ�С����A��ȷ��
B���ɷ�Ӧ��֪Mg�μӷ�Ӧ����ʼ�Ӵ������Ӧ���ʿ죬���淴Ӧ�Ľ��У��Ӵ������С����Ӧ���ʼ�С����B��ȷ��
C����Ӧ��ʼH+����Ũ��������ŷ�Ӧ����Ũ�Ȼ���С������Ӧ������������÷�ӦΪ���ȷ�Ӧ������ʹ�¶����ߣ���Ӧ���ʼӿ죬��C��ȷ��
D����Cl-���μӷ�Ӧ��Cl-��Ũ��������С����Ӱ�컯ѧ��Ӧ���ʣ��Ҹ÷�Ӧ��Cl-��Ũ�Ȳ��䣬��D����
��ѡ��D��
���������
�����Ѷȣ���
5��ѡ���� ��ѧ�г���ͼ��ֱ�۵�������ѧ��Ӧ�Ľ��̻���������ͼ��������ȷ���ǣ�������

A��ͼ�ٿ��Ա�ʾ��ij��ѧƽ����ϵ�ı��¶Ⱥ�Ӧ������ʱ��ı仯
B��ͼ�ڱ�ʾѹǿ�Կ��淴Ӧ2A��g��+2B��g��?3C��g��+D��g����Ӱ�죬���ҵ�ѹǿ��
C��ͼ�۱�ʾ��Al2��SO4��3��MgSO4�Ļ��Һ�еμ�NaOH��Һ�����ɳ������������NaOH��Һ����Ĺ�ϵ
D������ͼ�ܿ�ȷ����ȥCuSO4��Һ�е�Fe3+��������Һ�м���Cu��OH��2����pH��4����
�ο��𰸣�A�������¶�ʱ�����۸÷�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ�����淴Ӧ���ʶ�������һ������һ����С����A����
B����ͼ���֪��������б�ʴ��ҷ�Ӧ����ƽ���õ�ʱ���٣����ҷ�Ӧ���ʿ죬����ѹǿ�Է�Ӧ���ʵ�Ӱ�죬ѹǿԽ��Ӧ����Խ����������ѹǿ�÷�Ӧ��һ����Ӧǰ�������������Ļ�ѧ��Ӧ������ѹǿƽ�ⲻ�ƶ�ֻ���������淴Ӧ���ʣ����̵���ƽ���ʱ�䣬����A�ĺ������䣬����ʵ�ʣ���B��ȷ��
C��þ���Ӻ������Ӷ������������ӷ�Ӧ����������þ�������������������������ƹ���ʱ�����������ֺ��������Ʒ�Ӧ���ɿ����Ե�ƫ�����ƣ����²��ֳ����ܽ⣬�����������٣�������������ȫת��Ϊƫ�����ƺ����������ټ�����һ���㶨ֵ����C����
D��CuSO4��Һ�м�������Cu��OH��2��������Cu��OH��2+2H+�TCu2++2H2O����Һ��H+Ũ�ȼ�С������Fe3+ˮ�����ɳ�����������pH��4����ʱ��Fe3+ȫ��ˮ�����ɳ�������ȥ����D��ȷ��
��ѡBD��
���������
�����Ѷȣ���