��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��C+CO2==2CO;��H��0,��Ӧ����Ϊv1��N2+3H2==2NH3;��H��0����Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ������ ��
A��ͬʱ����
B��ͬʱ��С
C��v1����v2��С
D��v1����v2����
�ο��𰸣�A
��������������¶ȣ����۶������Ȼ��Ƿ��ȷ�Ӧ������ʹ��Ӧ��������
�����Ѷȣ�һ��
2������� ����þ���仯���ﲻ���ڹ���������ҪӦ�ã��ڻ�ѧ�о���Ҳ�й㷺Ӧ�ã�
��1��ijͬѧ�о���Ӧ����ʱ�����·�����ȡһ��þ������ɰֽ��ȥ���������Ĥ��ʹ����þ����һ�������ᷴӦ����H2�����뷴Ӧʱ��Ĺ�ϵ������ͼ��ʾ��þ�����ᷴӦ�����ӷ���ʽΪ______����ǰ4min�ڣ�þ��������ķ�Ӧ�����ӿ죬��4min֮��Ӧ�����������������ԭ��______��
��2����������Mg��OH��2����Һ�м��������ı����Ȼ����Һ��������ȫ�ܽ⣬д��NH4Cl������ҺʹMg��OH��2����Һ�ܽ�����ӷ���ʽ______��
��3��Mg-Al���γ�ԭ��أ�
| ��� | �缫���� | �������Һ | ��������
����
1
Mg-Al
ϡ����
Mg����Al
2
Mg-Al
NaOH��Һ
|
�����ϱ��е�ʵ����������������⣺
��ʵ��1��MgΪ______����
��ʵ��2�е�����������______��AlΪ______����Ϊʲô��______��
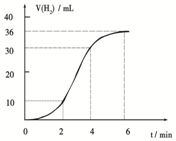
�ο��𰸣���1��þ�����ᷴӦ�����Ȼ�þ����������Ӧ�����ӷ���ʽΪMg+2H+�TMg2++H2������ǰ4min�ڣ�þ��������ķ�Ӧ�����ӿ죬ԭ����þ�����ᷴӦ�Ƿ��ȷ�Ӧ�����ŷ�Ӧ��ϵ�¶����ߣ���Ӧ����������4min֮��Ӧ����������ԭ����4min��������Һ��H+Ũ�Ƚ��ͣ����Ե��·�Ӧ���ʼ�С��
�ʴ�Ϊ��Mg+2H+�TMg2++H2����þ�����ᷴӦ�Ƿ��ȷ�Ӧ�����ŷ�Ӧ��ϵ�¶����ߣ���Ӧ��������4min��������Һ��H+Ũ�Ƚ��ͣ����Ե��·�Ӧ���ʼ�С��
��2��������þ���Ȼ�立�Ӧ�����Ȼ�þ��һˮ�ϰ�����Ӧ�����ӷ���ʽΪMg��OH��2��s��+2NH4+�TMg2++2NH3?H2O��
�ʴ�Ϊ��Mg��OH��2��s��+2NH4+�TMg2++2NH3?H2O��
��3����Mg��Al���ã�������������þΪ������
�ʴ�Ϊ������
����������ǿ�Ӧ�����ڼ�����������Ϊ������������������þ��
�ʴ�Ϊ��Al����Mg������Al�ܺ�NaOH��Һ��Ӧ��Mg���ܣ���Al��������Mg��������
���������
�����Ѷȣ���
3��ѡ���� �����ӷ�Ӧ������л���Ӱٷ������ǣ�?��
A�������¶�
B�������ݻ������
C������ѹǿ
D������Ũ��
�ο��𰸣�A
���������A �������¶ȣ������ӻ��������Ҳ���ӻ���Ӱٷ���
B�������ݻ�������������˻������
C ��Dֻ�������˻����������û���������Ӱٷ�����
�����Ѷȣ���
4��ѡ���� I2��KI��Һ�д�������ƽ�⣺I2(aq)+ I��(aq) ?I3��(aq)��ijI2��KI�����Һ�У�I3�������ʵ���Ũ��c(I3��)���¶�T�Ĺ�ϵ��ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵������ȷ����
?I3��(aq)��ijI2��KI�����Һ�У�I3�������ʵ���Ũ��c(I3��)���¶�T�Ĺ�ϵ��ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵������ȷ����

A����Ӧ I2(aq)+ I��(aq) ?I3��(aq) �Ħ�H��0
B������Ӧ���е�״̬Dʱ����Ӧ����һ����V(��)