��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ����̵����ӷ���ʽ��ȷ����
A��ͭƬ������������Һ�У�Cu��Ag����Cu2����Ag
B��̼������������NaOH��Һ��ӦCa2����2HCO3����2OH����CaCO3����2H2O��CO32��
C����ʯī���缫���AlCl3��Һ��2Cl����2H2O  Cl2����H2����2OH��
Cl2����H2����2OH��
D��������������Һ�����ԣ�NaHSO3��Na��+H��+ SO32��
�ο��𰸣�B
���������A����ɲ��غ㣬����B��̼������������NaOH��Һ��Ӧ����ζ��̼�����������̼����Ƶ�������ĸ�������̼��������Ӷ����������Ʒ�Ӧ������̼��Ƴ�����̼������ӡ�ˮ����ȷ��C�������е���������������Һ�е������ӽ������������������������D��������������Һ����������ΪHSO3-���ֵ������H����SO32��������ѡB��
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��д��ȷ����
[? ]
A��Na2S��Һ��ˮ�⣺S2-+ 2H2O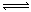 H2S + 2OH-
H2S + 2OH-
B��NaHCO3��Һ�ĵ��룺NaHCO3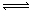 Na+��H+��CO32-
Na+��H+��CO32-
C��NH4Cl��Һ��ˮ�⣺NH4+ + H2O 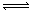 NH3��H2O + H+
NH3��H2O + H+
D���ѽ���������ϡ�����У�2 Fe + 6H+ = 2Fe3+ + 3 H2��
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A��ʯ��ʯ���ڴ��CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2��+H2O
B��п������ͭ��Һ��Ӧ��Cu2++Zn=Zn2++Cu
C����м���ڹ���ϡ���3Fe+8H++2NO3-=3Fe2++2NO��+4H2O
D��FeI2��Һ��ͨ������������2Fe2++Cl2=2Fe3++2Cl-
�ο��𰸣�A��ʯ��ʯ���ڴ�������ӷ�ӦΪCaCO3+2CH3COOH=2CH3COO-+Ca2++CO2��+H2O����A��ȷ��
B��п������ͭ��Һ��Ӧ�����ӷ�ӦΪCu2++Zn=Zn2++Cu����B��ȷ��
C����м���ڹ���ϡ��������ӷ�ӦΪFe+4H++NO3-=Fe3++NO��+2H2O����C����
D��FeI2��Һ��ͨ���������������ӷ�ӦΪ2I-+Cl2=I2+2Cl-����D����
��ѡAB��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ����д��ȷ����
A������ϡ���ᷴӦ 2Fe+6H+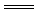 2Fe3++3H2��
2Fe3++3H2��
B����������Һ�м���ͭ�� Ag++Cu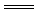 Cu2++Ag
Cu2++Ag
C������ͭ�����ᷴӦ O2�D +2H��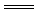 H2O
H2O
D��̼��þ��ϡ���ᷴӦ��MgCO3��2H��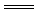 Mg2����H2O��CO2��
Mg2����H2O��CO2��
�ο��𰸣�D
���������A������ϡ���ᷴӦ��������Fe3+��B���ɲ��غ㣻C������ͭ������������ܲ�֡���ѡD��
���������ӷ���ʽ�����ж�Ҫע�⣺���Ƿ���Ͽ���ʵ�����Ƿ���������غ㡢���Ƿ���ϵ���غ㡢���Ƿ���ϵ�ʧ������ȡ����ܵ���������ʲ�����ӡ�ע������������������ȡ�
�����Ѷȣ�һ��
5������� ��̼���Ƶ�Ũ��Һ����μ���ϡ���ᣬ�����ٲ���CO2����Ϊֹ���ڴ˹����У���Һ�е�̼���������Ũ�ȵı仯���ƿ�����______���������ѡ����ѡ����Ӧ�������й����ӷ���ʽΪ��______��______��
����С�����������������Ȼ���С������С��Ȼ������
�ο��𰸣�̼����Ϊ��Ԫ�����Ӧ�����Σ���μ������ᣬ�ȷ�����Ӧ������ʽ�Σ���Ӧ�����ӷ���ʽΪCO32-+H+=HCO3-����ʱ��Һ�е�̼���������Ũ����������ȫ����̼���������ʱ��������Ӧ���ɶ�����̼��ˮ����Ӧ�����ӷ���ʽΪ
HCO3-+H+=H2O+CO2������Һ�е�̼���������Ũ������С��
�ʴ�Ϊ���ۣ�CO32-+H+=HCO3-��HCO3-+H+=H2O+CO2����
���������
�����Ѷȣ���