| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《影响盐类水解的因素》高频考点预测(2017年最新版)(二)
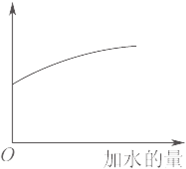 参考答案:A、水解的平衡常数只与温度有关,加水稀释平衡常数不变,故A错误; 本题解析: 本题难度:简单 2、选择题 短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是( ) 参考答案:根据?短周期元素W、X、Y、Z的原子序数依次增大及各选项可以推出,W为O2-、X为Na+、Y为Al3+、Z为S2-,Al3+和S2-均能发生水解,水解打破了水的电离平衡;O2-不能在水溶液存在,而Na+不水解,故正确的是C; 本题解析: 本题难度:一般 3、选择题 室温下,某浓度的醋酸溶液中n(CH3COO-)=0.01mol,下列叙述正确的是 参考答案:AD 本题解析:醋酸是弱酸,盐酸是强酸,前者部分电离,后者完全电离,加入等浓度盐酸,增大溶液中氢离子浓度,使CH3OOH 本题难度:一般 4、填空题 (12分)在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解。试回答下列问题: |
参考答案:(1)?酸?Fe2++2H2O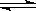 Fe(OH)2+2H+?抑制?
Fe(OH)2+2H+?抑制?
(2)? Al3++3HCO3-=Al(OH)3↓+3CO2↑? (3)? D?(4)Al2O3
本题解析:(1)氯化亚铁是强酸铁弱碱盐,水解显酸性,因此增大氢离子浓度,能抑制其水解。
(2)硫酸铝水解显酸性,碳酸氢钠水解显碱性,所以二者混合时水解相互促进,生成氢氧化铝沉淀和CO2气体。
(3)A不正确,因为中和反应是放热反应。B不正确,硝酸铵溶于水是吸热过程。C不正确,因为是增大了NH4+的浓度,抑制了氨水的电离,所以pH减小。因此选项D是正确,红色加深,说明升高温度,平衡向正反应方向移动,即水解是吸热反应。
(4)氯化铝溶液中存在水解平衡AlCl3+3H2O Al(OH)3+3HCl,加热促进水解,同时生成物氯化氢易挥发,进一步促进水解,所以最终得到的是氢氧化铝沉淀,灼烧得到氧化铝。
Al(OH)3+3HCl,加热促进水解,同时生成物氯化氢易挥发,进一步促进水解,所以最终得到的是氢氧化铝沉淀,灼烧得到氧化铝。
本题难度:简单
5、选择题 相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温、同体积、同浓度的HCN和HClO溶液的说法中正确的是( )
A.酸的强弱:HCN>HClO
B.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)<c(ClO-)
参考答案:D
本题解析:强碱弱酸盐的水溶液呈碱性,相应酸的酸性越弱,其强碱盐溶液的碱性越强。NaCN溶液的pH比NaClO大,说明HCN比HClO酸性弱。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《氨气》考点.. | |