微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Ⅰ.硬铝废料(含90%铝、2.5%镁、7.5%铜)可以制取明矾KAl(SO4)2.12H2O,某探究小组设计了下列实验.
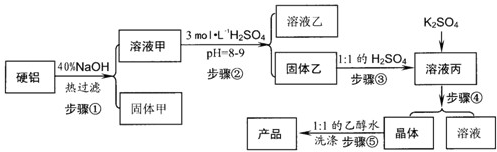
请回答以下问题:
(1)写出步骤③的离子方程式______.
(2)步骤④包括三个环节,分别是______、冷却结晶、______.
(3)步骤⑤不直接用水洗的原因是______.
Ⅱ.某课题小组同学测量液态奶含氮量的实验过程如下:
原理:液态奶
(NH4)2SO4溶液NH3(NH4)2B4O7溶液→用标准盐酸滴定
步骤:
①在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
②将反应液转移到大试管中;
③按如下装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
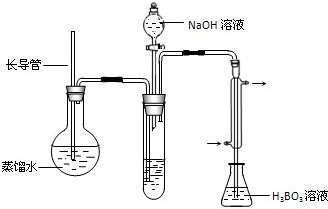
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
⑤重复测定两次,再用10.00mL蒸馏水代替液态奶进行上述操作.
数据记录如下:
| 实验编号 | 样品和辅助试剂 | 消耗盐酸
体积(mL)
1
10.00mL液态奶、0.2g催化剂、20mL浓硫酸
33.45
2
10.00mL液态奶、0.2g催化剂、20mL浓硫酸
33.55
3
10.00mL液态奶、0.2g催化剂、20mL浓硫酸
33.50
4
10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸
1.50
|
回答下列问题:
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为______.
(2)步骤③的实验装置中需要加热的仪器是______(填仪器名称),长导管的作用是______.
(3)设计4号空白对照实验的目的是______.
(4)计算该液态奶的含氮量为______mg?mL-1.
参考答案:Ⅰ.(1)氢氧化铝与硫酸反应生成硫酸铝和水,离子方程式为Al(OH)3+3H+=Al3++3H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;?
(2)向硫酸铝溶液中加入硫酸钾,得混合溶液,通过蒸发、结晶、过滤制得明矾,故答案为:蒸发;过滤;
(3)明矾在酒精中的溶解度小,用酒精洗涤减少产品的损失,故答案为:减少产品的损失;
Ⅱ.(1)硼的化合价未变化,发生类似复分解反应,反应方程式为(NH4)2B4O7+2HCl+5H2O=4?H3BO3+2NH4Cl,
故答案为:(NH4)2B4O7+2HCl+5H2O=4?H3BO3+2NH4Cl;?
(2)加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,长导管防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用,
故答案为:圆底烧瓶;安全管;
(3)对照使用目的是消除其他试剂、实验操作等因素引起的误差,故答案为:消除其他试剂、实验操作等因素引起的误差;
(4)盐酸的体积为33.45ml+33.55ml+33.50ml3-1.5ml=32.00ml=0.03200L,
?令10ml该液态奶的含氮量的质量为mg,则?
? ?2N~(NH4)2B4O7~2HCl
? 28g? 2mol
?mg? 0.03200L×0.1000mol/L
所以m=28g×0.03200ml×0.1000mol/L2mol=0.04480g,
该液态奶的含氮量为44.8mg10ml=4.48mg/ml,
故答案为:4.48.
本题解析:
本题难度:一般
2、简答题 将镁、铝的混合物0.1mol溶于100mL?2mol/L的H2S04溶液中,然后再滴加1mol/L的NaOH溶液.请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液的体积V变化如图所示.当V1=160mL时,则金属粉末中,n(Mg)=______mol,V2=______mL.
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、A13+刚好沉淀完全,则滴入NaOH溶液的体积
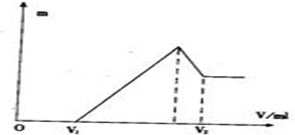
参考答案:(1)当V1=160mL时,此时,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,
由Na+离子守恒可知,n(Na2SO4)=12n(Na+)=12n(NaOH)=12×0.16L×1mol/L=0.08mol
令MgSO4为xmol,Al2(SO4)3为ymol,则:
根据Mg原子、Al原子守恒有:x+2y=0.1
根据SO42-离子守恒有:x+3y=0.2-0.08
联立方程,解得:x=0.06;y=0.02
所以金属粉末中n(Mg)=0.06mol,n(Al)=2y=2×0.02mol=0.04mol
滴加NaOH溶液到体积V2时时,溶液是Na2SO4和NaAlO2混合液,根据SO42-离子、Na+离子和Al原子守恒有:
n(NaOH)=2n(Na2SO4)+n(NaAlO2)=2n(H2SO4)+n(Al)=2×0.1L×2mol/L×+0.04mol=0.44mol,
所以,V2=0.44mol1mol/L=0.44L=440ml
故答案为:0.06mol,440?mL.
(2)当溶液中Mg2+、Al3+恰好沉淀完全时,此时,溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有:n(Na+)=2n(Na2SO4)=2(H2SO4)=2×0.1L×2mol/L=0.4mol,所以,V(NaOH)=0.4mol1mol/L=0.4L=400ml
故答案为:400ml;
本题解析:
本题难度:一般
3、选择题 将两种金属混合而成的粉末30 g,与足量的盐酸反应,产生氢气22.4 L,该混合物可能是(?)
A.镁和铜
B.钠和锌
C.铁和钙
D.铝和镁
参考答案:A
本题解析:由极限法分析:若全部为选项中某金属产生氢气22.4 L所消耗的质量分别为:镁24 g、钠46 g、锌65 g、铁56 g、钙40 g、铝18 g,铜不反应可认为需要无穷大的质量,混合物30 g就可产生同样量的气体,一定含有镁,答案为A。
本题难度:简单
4、填空题 工业制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的是Al2O3,然后电解是
Al2O3得到铝。下图是从铝土矿中提纯是Al2O3的简单示意图。其中牵涉到的一个反应是:
2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。
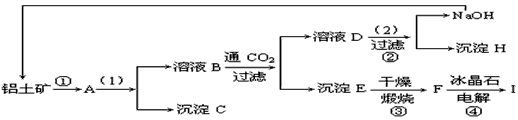
(1)写出图示中(1)的实验操作是____________;图示中(2)加入的试剂_____________。
(2)试推断物质(写化学式)B___________;C___________;H_____________;F______________。
(3)写出化学方程式:
①______________________。 ②______________________。
③______________________。 ④______________________。
参考答案:(1)过滤;Ca(OH)2
(2)NaAlO2;Fe2O3;CaCO3;Al2O3
(3)①Al2O3+2NaOH==2NaAlO2+H2O
②Na2CO3+Ca(OH)2==CaCO3↓+2NaOH
③2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
④2Al2O3 4Al+3O2↑
4Al+3O2↑
本题解析:
本题难度:一般
5、选择题 以Al、CuO、CuCl2溶液、盐酸、氢氧化钾溶液为反应物,常温下两两间可发生的反应有
A.6个
B.5个
C.4个
D.3个
参考答案:A
本题解析:铝和氧化铜可发生铝热反应,和氯化铜可发生置换反应,和盐酸及氢氧化钾溶液都反应生成氢气,氧化铜能和盐酸反应,氯化铜能和氢氧化钾反应,所以答案选A。
本题难度:一般