| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《弱电解质电离平衡》考点强化练习(2017年押题版)(十)
参考答案:A 本题解析:①有自由移动的电子或自由移动离子的物质能导电;②根据电解质的定义:必须是化合物,在水溶液里或熔融状态下有自由移动的离子,且离子是物质本身电离的,不能是与其它物质反应后的物质电离的;③能全部电离的电解质是强电解质;只有部分电离的电解质是弱电解质。①盐酸-HCl的水溶液,混合物,能导电 ②食盐水-NaCl的水溶液,能导电 ③熔化的氯化钠 本题难度:一般 2、填空题 在相同条件下进行Mg和酸反应的对应实验,相关数据如下:
参考答案: 本题解析: 本题难度:一般 3、选择题 将0.1mol・L-1醋酸溶液加水稀释,下列说法正确的是 [? ] A.溶液中c (H+)和c(OH-)都减小 B.溶液中c (H+)增大 C.醋酸电离平衡向左移动 D.溶液的pH增大 参考答案:D 本题解析: 本题难度:一般 4、选择题 下列混合溶液中,各离子浓度的大小顺序的表示中,正确的是? (? ) |
参考答案:B
本题解析:略
本题难度:简单
5、填空题 (8分)常温下有浓度均为0.5mol/L的五种溶液:①NaHCO3;②C6H5ONa;③ NH4HCO3;④ NH3・H2O;⑤ HCl
(1)上述五种溶液中既能跟盐酸反应又能跟NaOH溶液反应的是 (填序号)。
(2)上述②的水溶液呈碱性的原因是(用离子方程式表示) 。
(3)③跟足量的NaOH浓溶液在加热条件下反应的离子方程式是 。
(4)取10mL⑤的溶液加水稀释到500mL,则该溶液中由水电离出的c(H+)= mol/L.
参考答案:(1)①③(2分)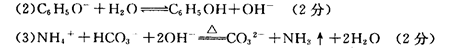
(4)10―12(2分)
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《元素周期律.. | |