微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 以下是一些物质的熔沸点数据(常压):
| 钾
| 钠
| Na2CO3
| 金刚石
| 石墨
|
熔点(℃)
| 63.65
| 97.8
| 851
| 3550
| 3850
|
沸点(℃)
| 774
| 882.9
| 1850(分解产生CO2)
| ----
| 4250
|
金属钠和CO2在常压、890℃发生如下反应:4 Na(g)+ 3CO2(g)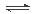 2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
(1)若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,若反应时间为10min, 金属钠的物质的量减少了0.2mol,则10min内CO2的平均反应速率为 。
(2)高压下有利于金刚石的制备,理由是 。
(3)由CO2(g)+ 4Na(g)=2Na2O(s)+ C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
(4)下图开关K接M时,石墨电极反应式为 。
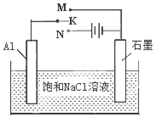
(5)请运用原电池原理设计实验,验证Cu2+、Ag+氧化性的强弱。
在方框内画出实验装置图,要求用烧杯和盐桥(在同一烧杯中,
电极与溶液含相同的金属元素),并标出外电路电子流向。
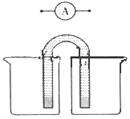
参考答案:(1)0.0015 mol/(L ・min)(2分)
(2)增大压强加快反应速率,反应向正反应方向移动(2分);
(3)3Na2O(s)+C(s,金刚石) = 4Na(g)+Na2CO3(l)△H= ―4.2kJ/mol(2分);
(4)O2+2H2O+4e- =4OH-(2分);
(5) (2分)
(2分)
本题解析:(1)先根据定义式求v(Na),再根据速率之比等于化学方程式中的系数之比求v(CO2),即v(Na) =0.0020mol/(L?min), v(CO2)="3" v(Na)/4=0.0015mol/(L?min);(2)增大压强加快反应速率,反应向正反应方向移动;(3)将已知两个热化学方程式编号为①②,①―②×3可以约去3 CO2(g),根据盖斯定律,则6Na2O(s)+2C(s,金刚石)=8Na(g)+2Na2CO3(l) △H=―8.4kJ/mol,若系数减半,则焓变也减半,则3Na2O(s)+ C(s,金刚石)=4Na(g)+Na2CO3(l) △H=―4.2kJ/mol;(4)若K接M,则该装置为原电池,模拟铝的吸氧腐蚀,由于铝比石墨活泼,则铝是负极,石墨是正极,负极反应式为Al―3e―=Al3+,正极反应式为O2+4e―+2H2O=4OH―;(5)验证Cu2+、Ag+氧化性的强弱,可根据置换反应:
Cu+2Ag+=Cu2++2Ag来设计原电池,铜发生氧化反应,银离子发生还原反应。所以铜作负极,银作正极,硫酸铜和硝酸银作电解质溶液。
考点:考查化学反应速率、化学平衡、电化学等相关知识。
本题难度:困难
2、填空题 (8分)将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L・min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L・min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol;
(2)B的平均反应速率v(B)=________mol/(L・min);
(3)x的值为________。?
参考答案:(1)0.75 3? (2)0.05? (3)2
本题解析:C的平均反应速率为0.1 mol/(L・min),所以5min后生成的C是0.5mol/L,又因为同时有0.5 mol/L的D生成,所以根据浓度的变化量之比是相应的化学计量数之比看得出x=2。
3A(g)+B(g) 2C(g)+2D(g)
2C(g)+2D(g)
起始量(mol)? y? y? 0? 0
转化量(mol)? 1.5? 0.5? 1.0? 1.0
5min后(mol)? y-1.5? y-0.5? 1.0? 1.0
因为c(A)∶c(B)=3∶5,所以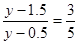 ,解得y=3mol。则此时A的浓度是
,解得y=3mol。则此时A的浓度是
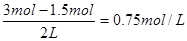 。B的平均反应速率v(B)=
。B的平均反应速率v(B)=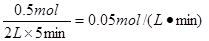 。
。
本题难度:一般
3、选择题 在2A+B=3C+4D反应中,表示该反应速率最快的数据是( )
A.υA= 0.5mol/(L・s)
B.υB= 0.3mol/(L・s)
C.υC= 0.8mol/(L・s)
D.υD= 1.0mol/(L・s)