微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 T ℃时,在1 L的密闭容器中充入2 mol CO2和6 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ・mol-1,测得H2和CH3OH(g)的浓度随时间变化如下表所示。下列说法不正确的是( )
CH3OH(g)+H2O(g) ΔH=-49.0 kJ・mol-1,测得H2和CH3OH(g)的浓度随时间变化如下表所示。下列说法不正确的是( )
时间/min
| c(H2)/mol・L-1
| c(CH3OH)/mol・L-1
| v(正)和v(逆)比较
|
t0
| 6
| 0
| ?
|
t1
| 3
| 1
| v(正)=v(逆)
|
?
A.t0~t1时间内v(H2)=3/(t1-t0) mol・L-1・min-1
B.t1时,若升高温度或再充入CO2气体,都可以提高H2的转化率
C.t0时,v(正)>v(逆)
D.T ℃时,平衡常数K=1/27,CO2与H2的转化率相等
参考答案:B
本题解析:t0~t1时间内v(H2)=(6-3)/(t1-t0)mol・L-1・min-1,正确;t1时,平衡常数K=1/27,CO2与H2的转化率为50%;t0时,平衡向正方向移动,故v(正)>v(逆);t1时,处于平衡状态,升高温度平衡要向逆方向移动,H2的转化率要减小,故B项错误。
本题难度:简单
2、选择题 一定量的锌粉和6mol/L的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,又不影响产生H2的总量的是
( )
①石墨粉 ?②CuO ?③铜粉 ?④铁粉 ?⑤浓盐酸.
A.①②⑤
B.①③⑤
C.③④⑤
D.①③④
参考答案:①加入石墨粉,构成原电池,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故①正确;
②加入CuO,与盐酸反应生成氯化铜,氯化铜与锌反应生成铜,形成原电池,加快反应,但与盐酸反应的锌的量减少,生成氢气的总量减少,故②错误;
③加入铜粉,构成原电池,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故③正确;
④加入铁粉,构成原电池,反应速率加快,锌反应完毕,铁可以与盐酸反应生成氢气,产生H2的总量增大,故④错误;
⑤加入浓盐酸,氢离子浓度增大,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故⑤正确;
故选B.
本题解析:
本题难度:一般
3、填空题 在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s)
| 0
| 1
| 2
| 3
| 4
| 5
|
n(NO)/mol
| 0.020
| 0.010
| 0.008
| 0.007
| 0.007
| 0.007
|
?
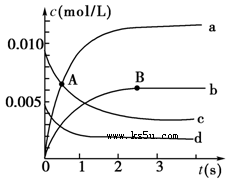
(1)A点处,v(正)________v(逆),A点正反应速率________B点正反应速率(用“大于”、“小于”或“等于”填空)。
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________________。
(3)能说明该反应已经达到平衡状态的是________。
a.v(NO2)=2v(O2)?b.容器内压强保持不变
c.v逆(NO)=2v正(O2)?d.容器内的密度保持不变
(4)能使该反应的反应速率增大的是________。
a.及时分离出NO2气体?b.适当升高温度
c.增大O2的浓度?d.选择高效的催化剂
参考答案:(1)大于 大于 (2)b 1.5×10-3mol/(L・s)?(3)bc (4)bcd
本题解析:(1)NO是反应物,起始浓度是0.020mol÷2L=0.010mol/L,所以曲线c表示NO的浓度变化曲线。A点NO的浓度继续降低,没有达到平衡状态,反应仍然是向正反应方向进行的,正反应速率大于逆反应速率,所以A点正反应速率大于B点正反应速率。
(2)NO2是生成物,在反应过程中浓度是增大的。由表中数据可知,平衡时c(NO)=0.007mol/L÷2L=0.0035mol/L。曲线b平衡时的浓度为0.0035mol/L,根据反应方程式中的化学计量数可知,曲线b表示NO2的浓度变化曲线。反应进行到2s是,NO浓度减少了0.010mol/L-0.004mol/L=0.006mol/L,所以氧气的浓度变化量是0.003mol/L,则氧气的反应速率是0.0030mol/L÷2s=1.5×10-3mol/(L・s)。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。a.始终都存在v(NO2)=2v(O2)关系,故不能说明到达平衡,故a错误;b.随反应进行气体的物质的量减小,压强逐渐减小,因此容器内压强保持不变时,可以说明到达平衡,故b正确;c.不同物质表示的正逆速率之比等于化学计量数之比,反应到达平衡,故v逆(NO)=2v正(O2),可以说明到达平衡,故c正确;d.反应混合气体的质量不变,容器的体积不变,密度始终不变,故容器内物质的密度保持不变,不能说明到达平衡,故d错误,答案选bc。
(4)a.及时分离出NO2气体,平衡向正反应移动,但反应速率降低,故a错误;b.适当升高温度,反应速率增大,平衡向逆反应移动,故b正确;c.增大O2的浓度,反应速率增大,平衡向正反应移动,故c正确;d.选择高效的催化剂,增大反应速率,不影响平衡移动,故d正确,答案选bcd。
点评:该题是高考中的常见题型,属于中等难度的试题,试题贴近高考,基础性强,侧重对学生能力的培养,有利于调动学生的学习兴趣,有助于培养学生的逻辑推理能力和创新思维能力。难点是平衡状态的判断,答题时应注意平衡状态判断选择判断的物理量,应随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态。
本题难度:一般
4、选择题 实验室利用Zn和稀HCl反应制取H2,下列措施中,不能提高化学反应速率的是(?)
A.增大盐酸的浓度
B.给反应液加热
C.向溶液中加入少量硫酸铜溶液
D.向溶液中加入醋酸钠晶体
参考答案:D
本题解析:考察影响化学反应速率的因素,分别为:增大反应物的浓度、升温、形成原电池,而D生成难电离的醋酸,减小了氢离子的浓度,反应速率减慢。
本题难度:一般
5、选择题 对某一可逆反应来说,使用催化剂的作用是
[? ]
A.提高反应物的平衡转化率
B.以同等程度改变正逆反应的速率
C.增大正反应速率,减小逆反应速率
D.改变平衡混合物的组成
参考答案:B
本题解析:
本题难度:简单