| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《盐类水解的原理》考点预测(2017年强化版)(八)
参考答案:B 本题解析:酸式盐(NaHX)溶液显碱性,HX-离子水解大于电离,说明H2X是弱酸,A、NaHX的电离方程式为NaHX===Na+ + HX¯,A错误;B、溶液显碱性,HX¯的电离程度小于HX¯的水解程度,B正确;C、由电荷守恒可知离子浓度关系:c(Na+) + c(H+) = c(OH¯) + c(HX¯) + 2c(X2¯),C错误;D、加水稀释,促进HX¯水解,c(HX¯)减小,不是增大,D错误;答案选B。 本题难度:一般 3、填空题 盐是一类常见的电解质,事实表明盐的溶液不一定呈中性. 参考答案:(1)CH3COONa是强碱弱酸盐水解显碱性,NH4Cl是强酸弱碱盐水解显酸性,KNO3是强酸强碱盐不水解显中性;故答案为:碱;酸;中; 本题解析: 本题难度:简单 4、选择题 在Na2CO3溶液中,下列离子浓度的关系正确的是 ( )。 |
参考答案:D
本题解析:由于CO32-水解,所以有c(Na+)>2c(CO32-)。一般说,水解的程度是较小的,即水解生成的HCO3-较少,同时HCO3-还要发生水解,因此应有:c(CO32-)>c(HCO3-)。Na2CO3水解呈碱性,故c(OH-)>c(H+)。
本题难度:一般
5、填空题 (8分)⑴浓度均为0.1mol/L的8种溶液:① HNO3 ② H2SO4 ③ CH3COOH ④ Ba(OH)2 ⑤NaOH ⑥ CH3COONa ⑦ KCl ⑧ NH4Cl,溶液pH值由小到大的顺序是(填写编号) ________________。
(2)氯化铝水溶液呈 性,原 因是(用离子方程式表示): ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 (写化学式)。
因是(用离子方程式表示): ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 (写化学式)。
参考答案:(8分)
⑴②①③⑧⑦⑥⑤④ (2)酸,Al3++3H2O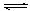 Al(OH)3+3H+,Al2O3
Al(OH)3+3H+,Al2O3
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《物质的量》.. | |