微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 电子计算器所用的纽扣电池中,还原剂是锌,氧化剂是Ag2O,电解质溶液为KOH溶液;其电极反应如下.Zn-2e-+2OH-═ZnO+H2O,Ag2O+2e-+H2O═2Ag+2OH-.
下列叙述正确的是( )
A.锌为正极
B.放电时,负极区溶液的pH增大
C.锌为负极
D.放电时,正极区溶液的pH减小
参考答案:A、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,故A错误;
B、原电池工作时,负发生反应Zn+2OH--2e-=ZnO+H2O,溶液pH值减小,故B错误;
C、根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,故C正确;
D、原电池工作时,正发生反应Ag2O+H2O+2e-=2Ag+2OH-,该极区溶液pH值增大,故D错误.
故选C.
本题解析:
本题难度:简单
2、选择题 下列有关电池的说法不正确的是
[? ]
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
参考答案:B
本题解析:
本题难度:一般
3、选择题 高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
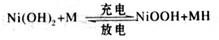
下列叙述不正确的是
A.该电池放电时的正极和充电时的阴极均发生还原反应
B.放电时负极反应为:MH+OH——e—=M+H2O
C.充电时阳极反应为:NiOOH+H2O+e—=Ni(OH)2+OH—
D.放电时每转移1mol电子,正极有1molNiOOH被还原
参考答案:C
本题解析:A项该电池放电时的正极发生还原反应,充电时的阴极均发生还原反应,正确;B项放电时负极反应为:MH+OH——e—=M+H2O,正确;C项充电时阳极反应不正确,应该是Ni(OH)2+OH—-e—= NiOOH+H2O,错误;D项根据电极反应,放电时每转移1mol电子,正极有1molNiOOH被还原,正确。
点评:对于可充电电池,原电池的负极就是电解池的阴极的逆反应。
本题难度:简单
4、选择题 高铁电池的总反应为:
3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
下列叙述错误的是?(?)
A.放电时每转移6mol电子,负极有2mol K2FeO4被还原
B.充电时阴极反应为:Zn(OH)2 + 2e— = Zn+ 2OH—
C.放电时正极反应为:FeO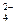 + 3e— + 4H2O = Fe(OH)3 + 5OH—
+ 3e— + 4H2O = Fe(OH)3 + 5OH—
D.充电时Zn电极与外电源的负极相连
参考答案:A
本题解析:略
本题难度:一般
5、填空题 (14分)氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)某课外学习小组欲制备少量NO气体,写出铁粉与足量稀硝酸反应制备NO的离子方程式: 。
(2)LiFePO4是一种新型动力锂电池的电极材料。
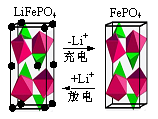
①下图为某LiFePO4电池充、放电时正极局部放大示意图,写出该电池放电时正极反应方程式: 。
②将LiOH、FePO4·2H2O(米白色固体)与还原剂葡萄糖按一定计量数混合,在N2中高温焙烧可制得锂电池正极材料LiFePO4。焙烧过程中N2的作用是 ;实验室中以Fe3+为原料制得的FePO4·2H2O有时显红褐色,FePO4·2H2O中混有的杂质可能为 。
(3)磷及部分重要化合物的相互转化如图所示。
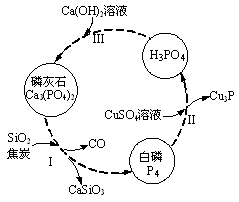
①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 。
③步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有 。
参考答案:(1) Fe+4H+ +NO3- = Fe3+ +NO↑ +2H2O(不配平扣1分)
(2)① Li++FePO4+e-=LiFePO4
② 防止生成的Fe2+在空气中重新被氧化 Fe(OH)3(或氢氧化铁)
(3)① 作还原剂 ② 0.05mol(不写单位扣1分) ③Ca (H2PO4)2、CaHPO4(每点1分)
(每空2分,共14分)
本题解析:(1)少量Fe与稀硝酸反应生成硝酸铁和NO、水,离子方程式是Fe+4H+ +NO3- = Fe3+ +NO↑ +2H2O;
(2)①由图可知,放电时正极中FePO4得到电子,结合Li+,生成LiFePO4,所以放电时正极反应式是Li++FePO4+e-=LiFePO4
②因为空气中的氧气易把LiFePO4中的亚铁离子氧化为铁离子,所以在氮气的氛围中来制取电极材料;实验室中以Fe3+为原料制得的FePO4·2H2O有时显红褐色,而氢氧化铁的颜色为红褐色,所以FePO4·2H2O中的杂质可能是Fe(OH)3;
(3)①因为步骤I是生产白磷的反应,二氧化硅用于造渣生产硅酸钙,则焦炭的作用是将P元素还原出来,本身被氧化为CO,所以焦炭的作用是作还原剂;
②根据步骤II,白磷与硫酸铜溶液反应生成Cu3P和磷酸,1mol硫酸铜转化为Cu3P,得到1mol电子,则白磷中P元素的化合价升高到+5价,则可氧化P原子的物质的量是0.2mol,白磷的分子式是P4,所以1mol硫酸铜可氧化白磷的物质的量是0.2/4mol=0.05mol;
③磷酸是三元酸,氢氧化钙的量不同得到的产物也不同,除生成Ca3(PO4)2正盐外,还可能生成2种酸式盐,Ca (H2PO4)2、CaHPO4。
考点:考查对物质性质的分析判断,氧化还原反应中得失电子守恒规律的应用,反应产物的判断
本题难度:困难