��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij������ȤС��Ϊ̽��ij�����Ͻ𣨺Ͻ�Ԫ��ΪMg?Al���Ƿ���Ϲ��������������ҹ涨�������������ܵ���78%���������ͼװ�ý���ʵ�飮
��1����μ����װ�õ�������______��
��2���Ͻ���Ʒ����M������������Һ��Ӧ�����ӷ���ʽ______��
��3����б���װ��ʹ����������Һ����������ag�Ͻ��ĩ������M����ַ�Ӧ������Ӧֹͣ������������������ΪVmL��������ɱ�״���������������������Ϊ50mL���������M������������mA1����ΧΪ______��
��4������װ���е�����������Һ�滻Ϊ���������ᣬ��Ӧֹͣ�����������������______?���������������=����VmL��
��5����a=38mg��V=44.8mL����״��������ͨ������˵���úϽ��Ƿ���Ϲ��ұ�����д������̣�______?������ϡ������ϡ�����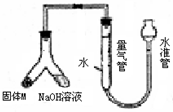
�ο��𰸣���1������װ�õ������Գ��÷���Ϊ�������������������Һ�������γ�Һ��߶Ȳ��װ��ͼ��֪�ʺ�ѡ��Һ�������γ�Һ��߶Ȳ�����װ�������Եķ���Ϊ����װ��װ�ò����������ڼ���ˮ�������ƶ�ˮ�ܣ�����Ƭ�̣���ˮ����Һ����������Һ��ά��һ���ĸ߶Ȳ˵��װ���ܷ⣬
�ʴ�Ϊ����װ��װ�ò����������ڼ���ˮ�������ƶ�ˮ�ܣ�����Ƭ�̣���ˮ����Һ����������Һ��ά��һ���ĸ߶Ȳ˵��װ���ܷ⣻
��2�������������ơ�ˮ��Ӧ�������ǻ��������ơ���������Ӧ���ӷ���ʽΪ2OH-+2Al+6H2O�T2[Al��OH��4]-+3H2����
�ʴ�Ϊ��2OH-+2Al+6H2O�T2[Al��OH��4]-+3H2����
��3���������������Ϊ50mL��������������������Ϊ50mL������������������ʵ���Ϊ0.05L22.4L/mol=0.0522.4mol�����ݵ���ת���غ��֪3n��Al��=2n��H2��=0.0522.4mol��2���������������Ϊ13��0.0522.4mol��2��27g/mol=0.04g�����Խ�������������ΧΪ0��mAl��0.04g��
�ʴ�Ϊ��0��mAl��0.04g��
��4��Mg��Al�������ᷴӦ����������������������������������ʴ�Ϊ������
��5��44.8mL���������ʵ���Ϊ0.0448L22.4L/mol=0.002mol�����ݵ���ת���غ��֪3n��Al��=2n��H2��=0.002mol��2=0.004mol�����ԺϽ�����������13��0.004mol��27g/mol=0.036g���Ͻ���Al����������Ϊ0.036g0.038��100%=94.74%��78%���ʸúϽ���ϱ����ʴ�Ϊ�����ϣ�
���������
�����Ѷȣ�һ��
2��ѡ���� ij���κ�����NaOH��Һ��ַ�Ӧ��Ȼ����������μ�������������Һ����Ӧ�в��������������ͼ�������������Һ�����֮��Ĺ�ϵ����ͼ�з����������ǣ�������������������Һ�������
[? ]
A.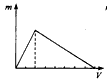
B.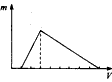
C.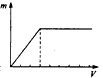
D.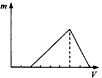
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� �����ȼ�ұ�����۽���������Ϊ���ǣ�������
A���������
B��������չ��
C���������ᷴӦ������Ӧ
D�������������зų���������
�ο��𰸣������ȼ�ұ�����۽���������Ϊ�������������зų��������ȣ�ʹ�û����Ľ���������̬���ɣ��͵����ԡ���չ���أ�
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� �����йس�������Ʒ��ʹ���У�����Ϊ�������ǣ�������
A��ʢ��ʳ��
B������ˮ
C���ý���˿��ϴ������۹�
D���ü�ˮϴ��
�ο��𰸣����������ᷴӦ������Ӧ����AD�������C������Ʒ������һ�����ܵ�������Ĥ�������������ã����ý���˿��������۹������ƻ�����Ĥ������ȡ��
������ˮ����Ӧ������B����ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
5�������� ����NaOH��AlCl3��MgCl2���ֹ�����ɵĻ������������ˮ�У���0.58 g��ɫ��������������������Һ����μ���0.5 mol��L-1�����ᣬ�����������������ɳ�������������ͼ��ʾ��
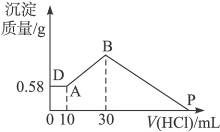
��1���������NaOH��������___________g��AlCl3��������___________g��MgCl2������Ϊ___________g��
��2��P���ʾ�����������Ϊ___________mL��
�ο��𰸣���1��2.6? 1.335? 0.95?��2��130
�����������1����ͼ��֪���������ʻ��ʱ��0.58 g����������˻�����м���10 mL����ʱ�������������䣬˵���������NaOH�������ó�����Mg(OH)2����þԪ���غ��֪��n(MgCl2)=n��Mg(OH)2��=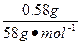 ="0.01" mol����m(MgCl2)="0.01" mol��95 g��mol-1="0.95" g�������¹�ϵ�ã�
="0.01" mol����m(MgCl2)="0.01" mol��95 g��mol-1="0.95" g�������¹�ϵ�ã�
2NaOH?��? MgCl2��Mg(OH)2
0.02 mol? 0.01 mol
AlCl3?��? NaAlO2��HCl
0.01 mol?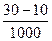 ��0.5 mol��L-1="0.01?" mol
��0.5 mol��L-1="0.01?" mol
m(AlCl3)="0.01" mol��133.5 g��mol-1="1.335" g
��ͼ��֪��B���dz��������㣬��ʱ��Һ������ֻ��NaCl����Ԫ���غ��֪��
n(NaOH)=n(HCl)+2n(MgCl2)+3n(AlCl3)="0.5" mol��L-1��0.03 L+2��0.01 mol+3��0.01 mol="0.065" mol�����ԣ�m(NaOH)="0.065" mol��40 g��mol-1="2.6" g��
��2����ͼ��֪��P��ʱAl(OH)3��Mg(OH)2����ǡ��ȫ���ܽ��������У�����ΪNaCl��AlCl3��MgCl2�����ԣ���ʱ�ܽ�Al(OH)3��Mg(OH)2����ǡ���������
V��HCl��=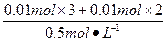 ="0.1" L="100" mL��
="0.1" L="100" mL��
�ɴ˿�֪��P��ʱ��V��HCl��="30" mL+100 mL="130" mL��
�����Ѷȣ���