微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应中可判断为可逆反应的是( )
A.氢气和氯气点燃生成氯化氢,氯化氢受热分解为氢气和氯气
B.氮气和氢气在高温、高压、催化剂作用下可以生成氨气,同时氨气又分解为氮气和氢气
C.单质溴可以置换出碘,氯气又可以置换出溴
D.氯气和水反应生成盐酸和次氯酸,次氯酸光照条件下可分解为盐酸和氧气
参考答案:B
本题解析:可 逆反应是在在相同条件下,既能向正反应方向进行,又能向逆反应方向进行的反应是可逆反应,所以只有选项B是正确的。答案选B。
本题难度:一般
2、选择题 在一定温度下,在恒容的密闭容器中进行的可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
A.C生成的速率和C分解的速率相等
B.单位时间内生成n mol A,同时生成3n mol B
C.B的消耗速率与C的消耗速率之比为1∶1
D.混合气体密度保持不变
参考答案:A
本题解析:A选项是由同种物质的两种速率来判断平衡,因此A对;B与C是由不同反应物的速率表示,而B表示的速率方向一致,所以不对;C表示的速率方向相反,但速率之比不等于计量数之比,所以B、C均不对;反应若是恒容条件下,由于反应物和生成物均为气体,混合气体密度始终保持不变,故D错误。
本题难度:一般
3、填空题 钢铁是21世纪用途最广的结构材料和功能材料。其成分主要是Fe和少量C。
(1)工业上在炼铁高炉中用CO热还原Fe2O3冶炼铁。写出该反应的化学方程式并用单线桥表示电子转移的方向和数目?。
(2)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图(黑球代表Fe,白球代表Mg)。则铁镁合金的化学式为?。

(3)Fe3+的电子排布式为?;CH3+微粒的中心原子杂化轨道类型为?;
(4)向一定量的FeCl3溶液中加入适量KSCN溶液,溶液变红色。该反应体系中存在化学平衡?(用反应式表示);向上述红色溶液中加入Mg(OH)2固体,可观察到溶液红色变浅,有红褐色沉淀析出。试用平衡移动原理解释该现象?。(不考虑SCN―与Mg2+反应)
参考答案:
(1)
(2)FeMg2 ?
(3)1S22S23S23P63d5?SP2
Fe2++3SCN- Fe(SCN-)3?(红色) 由于氢氧化铁的溶解度小于氢氧化镁的溶解度,向上述体系中加入氢氧化镁后,发生沉淀转化:氢氧化镁沉淀转化成氢氧化铁沉淀,消耗了三价铁离子,使Fe2++3SCN-
Fe(SCN-)3?(红色) 由于氢氧化铁的溶解度小于氢氧化镁的溶解度,向上述体系中加入氢氧化镁后,发生沉淀转化:氢氧化镁沉淀转化成氢氧化铁沉淀,消耗了三价铁离子,使Fe2++3SCN- Fe(SCN-)3 平衡向左移动,Fe(SCN-)3 减少。
Fe(SCN-)3 平衡向左移动,Fe(SCN-)3 减少。
本题解析:(1)根据元素守恒和质量守恒定律,不难写出相关化学方程式和画出单线桥;(2)利用均摊法,
Fe:8× +6×
+6× =4;Mg:8;得到铁镁合金化学式:FeMg2;(3)根据能量最低原理和核外电子排布原理,不难写出Fe3+,核外电子排布式;CH3+微粒的中心原子C,含有3δ,孤电子对数:
=4;Mg:8;得到铁镁合金化学式:FeMg2;(3)根据能量最低原理和核外电子排布原理,不难写出Fe3+,核外电子排布式;CH3+微粒的中心原子C,含有3δ,孤电子对数: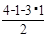 =0,
=0,
价层电子对数为4,杂化轨道类型SP2。(4)存在平衡Fe3++3SCN- Fe(SCN)3,根据勒夏特列原理不
Fe(SCN)3,根据勒夏特列原理不
难判断化学平衡的移动方向。
本题难度:一般
4、选择题 在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O发生反应:CO(g)+H2O(g) CO2(g)+H2(g),达到平衡时测得n(H2)为0.5mol,下列说法不正确的是?(?)
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5mol,下列说法不正确的是?(?)
A.在该温度下平衡常数K="1"
B.平衡常数与反应温度无关
C.CO的转化率为50%
D.其他条件不变时,改变压强平衡不移动
参考答案:B
本题解析:略
本题难度:简单
5、选择题 可逆反应A(g) + 3B(g)  2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是(?)
2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是(?)
A.甲中A的转化率为75%
B.甲、乙中C的体积分数相同
C.平衡后再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向生成C的方向移动
D.乙中的热化学反应方程式为2C(g) A(g)+3B(g);△H=+3Q2 kJ・mol-1
A(g)+3B(g);△H=+3Q2 kJ・mol-1
参考答案:D
本题解析:略
本题难度:一般