��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ڳ����£�ijˮ��ҺM�У�
��1����M�д��ڵ�����ֻ�У�Na+��CH3COO-��H+��OH-�����й�ϵ��������______��
��c��Na+����c��CH3COO-����c��OH-����c��H+��?��c��Na+����c��OH-����c��CH3COO-����c��H+��
��c��H+����c��OH-����c��Na+����c��CH3COO-��?��c��Na+��=c��CH3COO-����c��OH-��=c��H+��
��2����M��������ͬ���ʵ���Ũ�ȵ���Һ��϶��ɣ�����ֻ����OH-��H+��NH4+��Cl-�������ӣ���c��NH4+����c��Cl-����c��OH-����c��H+������������Һ��������______��
��3����MΪ0.01mol/L�İ�ˮ�������м�������pH=2��������Һ��������Һ����仯�������û��Һ�У�c��NH4+��+c��H+��-c��OH-��=______������ֵ��
��4������֪H2AΪ��Ԫ���ᣬ��ҺM�����������������0.01mol?L-1��H2A��Һ��0.01mol?L-1��NaHA��Һ��0.02mol?L-1��HCl��0.04mol?L-1��NaHA��Һ��������Һ���������������Һ��H2A����Ũ������Ϊ______��pH�ɴ�С��˳��Ϊ______��
��5����MΪ20mLϡ�����������Һ����û������Һ����μ���pH=13��Ba��OH��2��Һ������BaSO4�����ʵ���Ϊ0.001mol��������60mL?Ba��OH��2��Һʱ����Һ��pH=7��������Һ����仯�����Լ��㣺����������Һ��c��H2SO4��=______��c��HCl��=______��
�ο��𰸣���1��������Һ���������������ƣ��ɴ��������ˮ���Լ��Կ�֪��c��Na+����c��CH3COO-����c��OH-����c��H+�����ʢ���ȷ��
������ҺΪ�����ƺ�NaOH�Ļ�����Һ�Լ��ԣ���NaOH�����ʵ���Զ���ڴ����Ƶ����ʵ���ʱ����c��Na+����c��OH-����c��CH3COO-����c��H+�����ʢ���ȷ��
��������c��H+����c��OH-����c��Na+����c��CH3COO-��������ѭ����غ㣬�ʢ۴���?
����Ϊ�����ƺʹ���Ļ��Һ����ҺΪ���ԣ���c��Na+��=c��CH3COO-����c��OH-��=c��H+�����ʢ���ȷ��
�ʴ�Ϊ���٢ڢܣ�
��2��M��������ͬ���ʵ���Ũ�ȵ���Һ��϶��ɣ�����ֻ����OH-��H+��NH4+��Cl-�������ӣ���Һ����Ϊ�Ȼ�狀Ͱ�ˮ���Ȼ�狀����ᣬc��NH4+����c��Cl-����c��OH-����c��H+��������ҺNH4Cl��NH3?H2O���ʴ�Ϊ��NH4Cl��NH3?H2O��
��3��MΪ0.01mol/L�İ�ˮ�������м�������pH=2��������Һ����0.005mol/LNH4Cl��Һ�����ɵ���غ��֪c��NH4+��+c��H+��-c��OH-��=c��Cl-��=0.005mol/L��
�ʴ�Ϊ��0.005mol/L��
��4����0.01mol?L-1��H2A��Һ�У�ֻ���ڵ�����Һ�����ԣ���0.01mol?L-1��NaHA��Һ��ˮ��ʹ��Һ�Լ��ԣ���0.02mol?L-1��HCl��0.04mol?L-1��NaHA��Һ�������Ϻ�õ�0.01mol?L-1��H2A��0.01mol?L-1��NaHA���ε��������HA-������H2A�ĵ��룬��Һ�����ԣ�������С�ڢ٣����۵�H2A������࣬�ʴ�Ϊ�ۣ��ڢۢ٣�
��5����Ba��OH��2+H2SO4�TBaSO4��+2H2O��
? 1?1? 1
?x?0.001mol
��c��H2SO4��=0.001mol0.02L=0.05?mol/L��
����60mL?Ba��OH��2��Һʱ����Һ��pH=7���������Ũ��Ϊy����
0.06L��0.05mol/L=0.02L��0.05?mol/L��2+0.02L��y��
���y=0.05mol/L����c��HCl��=0.05?mol/L��
�ʴ�Ϊ��0.05mol/L��0.05?mol/L��
���������
�����Ѷȣ�һ��
2��ѡ���� ������������ˮʱ���ƻ�ˮ�ĵ���ƽ�⣬�����ڵ���ʵ���?��?��
A������
B��������̼
C��������
D���⻯��
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
3��ѡ���� Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ����pH��С���������˳����
��Na2CO3��Һ? ��NaHSO4��Һ? ��NaCl��Һ? ��AlCl3��Һ
A.�٣��ڣ��ۣ���
B.�٣��ۣ��ܣ���
C.�ڣ��ܣ��ۣ���
D.�ܣ��ۣ��ڣ���
�ο��𰸣�C
������������������������Һ��pH���Էֳ����࣬���ԡ����ԡ����ԡ� ��NaHSO4��Һ����ʽ�Σ���Һ�����ԣ�������ǿ����AlCl3��Һ��ǿ�������Σ�ˮ�����ʾ���ԣ���NaCl��Һ��ǿ��ǿ���Σ���ˮ�⣬��ʾ���ԣ� ��Na2CO3��Һ ��ǿ�������Σ�ˮ����ʾ���ԣ�����Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ����pH��С���������˳���Ǣڣ��ܣ��ۣ���?����ѡC��
���㣺�ε�ˮ��
�������ڴ�С��һ���ε�ˮ�⣺
��ʵ�ʣ�����Һ�У������ε������������ˮ����������ӽ������������ʣ��Ӷ��ƻ���ˮ�ĵ���ƽ�⣬ʹˮ�ĵ���ƽ�������ķ����ƶ�����ʾ����ͬŨ�ȵ����ԡ����Ի����ԡ�[1]
�����ɣ����ܲ�ˮ�⣬������ˮ�⣬������ˮ�⣻˭��˭ˮ�⣬Խ��Խˮ�⣬������ˮ�⣻˭ǿ��˭�ԣ�ͬǿ�����ԣ��������嶨��Խ��Խˮ�⣬ԽϡԽˮ�⡣
�����εĹ����г������������ӻ�����������ӣ����ξͻ�ˮ�⣻��Щ���Ӷ�Ӧ�ļ����Խ����ˮ��̶�Խ����Һ��pH�仯Խ��ˮ�����Һ��������ɹ��ɸ������Ӷ�Ӧ����ͼ����ǿ����������ǿ�����ԣ���ǿ�Լ��ԡ���
�����Ѷȣ���
4��ѡ���� �����йص������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
[? ]
A. ��0.1 mol/L NaHCO3��Һ�У�c(Na+)?> c(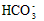 )> c(
)> c( )?> c(H2CO3)
)?> c(H2CO3)
B. ��0.1 mol/L Na2CO3��Һ�У�c(OH-) - c(H+)?= c(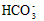 ) + c(H2CO3)
) + c(H2CO3)
C. ��0.2 mol/L NaHCO3��Һ�м�������0.1 mol/L NaOH��Һ��c( )?>c(
)?>c( )?>c(OH-)?>c(H+)
)?>c(OH-)?>c(H+)
D. �� 0.1 mol/L��CH3COONa��Һ�м�������0.1 mol/L CH3COOH��Һ��2c(H+) - c(CH3COO-) =2c(OH-) - c(CH3COOH)
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ���й��ڵ���ʵ�˵����ȷ���ǣ�������
A��NaHCO3����ˮ������뷽��ʽΪ��NaHCO3=Na++HCO3-��HCO3-=H++CO32-
B��SO2��ˮ��Һ�ܵ��磬����SO2Ϊ�����
C��Ũ�Ⱦ�Ϊ1?mol/L��NaCl��MgSO4��Һ������������ͬ
D��ǿ�������Һ�ĵ����Բ�һ�������������Һ�ĵ�������ǿ
�ο��𰸣�A��������ʽ�εĵ���ǿ��������NaHCO3����ΪNa+��HCO3-д�Ⱥţ�HCO3-����д����ţ���A����
B�����������ˮ��Һ�ܵ��磬ԭ���Ƕ��������ˮ��Ӧ���������ᣬ�������ܵ���������ƶ����������Ӷ�ʹ��Һ���磬�������ǵ���ʣ����������Ƿǵ���ʣ���B����
C��ͬŨ��ʱ����Na+��Cl-����ɱ�Mg2+��SO42-��NaCl��Һ�����Ա�MgSO4������C����
D��ǿ����ʵ�ˮ��Һ��һ�����к�ǿ�ĵ��������������ᱵ����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��