微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于Na2CO3和NaHCO3的说法不正确的是
A.在水中溶解度:Na2CO3> NaHC O3
B.二者都能与酸反应生成CO2
C.热稳定性:Na2CO3< NaHCO3
D.水溶液的碱性:Na2CO3> NaHCO3
参考答案:C
本题解析:该题考察碳酸钠和碳酸氢钠的性质比较,只有C错误,碳酸氢钠分解生成碳酸钠、水和二氧化碳,碳酸钠比较稳定。
本题难度:简单
2、选择题 化学式与其俗名相符的是(?)
A.纯碱NaOH
B.苏打NaHCO3
C.小苏打Na2CO3
D.芒硝Na2SO4・10H2O
参考答案:D
本题解析:Na2CO3俗称苏打、纯碱,NaHCO3俗称小苏打。
本题难度:简单
3、选择题 下列对Na2O2的叙述中,正确的是
A.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
B.Na2O2中氧元素的化合价为-2价
C.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
D.Na2O2需要密封保存
参考答案:D
本题解析:A、能和酸反应生成盐和水的氧化物是碱性氧化物,氧化钠是碱性氧化物。过氧化钠和酸反应除了生成盐和水以外,还有氧气生成,过氧化钠不是碱性氧化物,A不正确;B、过氧化钠中氧元素的化合价是-1价,B不正确;C、一种单质与一种化合物反应生成另外一种单质和化合物的反应是置换反应。过氧化钠与CO2发生氧化还原反应生成碳酸钠和氧气,该反应不是置换反应,C不正确;过氧化钠极易与水和CO2反应,因此过氧化钠需要密封保存,D正确,答案选D。
本题难度:一般
4、选择题 下面关于Na2CO3和NaHCO3性质的叙述,正确的是
A.受热时NaHCO3比Na2CO3稳定
B.在水中NaHCO3比Na2CO3溶解性大
C.质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多
D.物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多
参考答案:C
本题解析:受热时Na2CO3比NaHCO3稳定;在水中Na2CO3比NaHCO3溶解性大;碳酸钠和碳酸氢钠与盐酸反应的化学方程式是:Na2CO3+2HCl="2NaCl" +H2O +CO2↑
NaHCO3+HCl="NaCl" +H2O +CO2↑由此可知,物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2和Na2CO3一样多;质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多,故选C。
点评:本题考查的的钠的化合物的性质,内容源自于教材,熟悉碳酸钠和碳酸氢钠的性质,此类问题便不难解决。
本题难度:一般
5、选择题 有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,A、B中分别有10 mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中
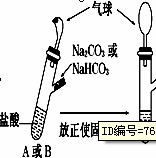
下列叙述正确的是?
A.A装置的气球膨胀速率大
B.若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L
D.最终两试管中Na+、Cl-的物质的量一定相同
参考答案:B
本题解析:A错,碳酸钠与盐酸反应先生成碳酸氢钠,而碳酸氢钠与盐酸反应立即有二氧化碳气体生成,所以,B装置的气球膨胀速率大;B正确,1.06 g Na2CO3的物质的量为0.01mol,完全反应需消耗HCL0.02mol,0.84 g NaHCO3的物质的量为0.01mol,完全反应需消耗HCL0.01mol,所以若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L;C错,若最终两气球体积不同,则盐酸的浓度一定小于2 mol/L;D错,因碳酸钠含钠的量为碳酸氢钠中钠的量的两倍,即,最终两溶液中Na+、Cl-的物质的量不相同;
本题难度:一般