��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� Ҫ��֤��ij��Һ���Ƿ���Fe3+�����в�������ȷ����
A���μ�KSCN��Һ
B����������
C��ͨ������
D����������
�ο��𰸣�A
������������������ӵ��Լ���KSCN��Һ����������Һ�Ժ�ɫ����ѡA��
�����Ѷȣ�һ��
2��ѡ���� ����ɫ��Һ�У����������ܴ���������ǣ�������
A��Mg2+��SO42-��K+��Cl-
B��Na+��NH4+��NO3-��MnO4-
C��K+��Cu2+��Cl-��NO3-
D��Ba2+��Na+��OH-��HCO3-
�ο��𰸣�A����Һ��ɫ��������֮�䲻�����κη�Ӧ���ܴ������棬��A��ȷ��
B��MnO4-����ɫ������Ŀ��ɫ��������B����
C��Cu2+����ɫ������Ŀ��ɫ��������C����
D��Ba2+��OH-��HCO3-���߷�Ӧ����BaCO3������ˮ�����ܴ������棬��D����
��ѡA��
���������
�����Ѷȣ�һ��
3��ѡ���� �������£����и���������ָ����Һ��һ���ܴ���������ǣ�
A����ˮ��Һ�У� H����I�D��NO3�D��SiO32��
B��������ˮ�У� Cl����NO3����Na����SO32��
C��������CO2ͨ��ʱ��H����NH4����Al3����SO42��
D��������Һ�У�NO3����I����Na����Al3��
�ο��𰸣�C
���������A����ˮ��Һ�У�? H����SiO32�����ɹ�������������ܹ��棻
B��������ˮ�У�? Cl2��SO32��������������ԭ�������棻
D��������Һ�У�OH-��Al3������������������ܹ��档
���������⿼�����ӹ������⣬��Ŀ�ѶȲ���ע�������֮���ܷ�����Ӧ���ɳ��������塢������ʡ�������ԭ��Ӧ�Լ���ٽ���ˮ��ȽǶȷ�����ע�����е�������Ϣ��������ɫ�����ԡ����Ե����⣮
�����Ѷȣ���
4������� �������γɶ������ӣ���N3����NH2����N3����NH4����N2H5����N2H6���ȡ���֪N2H5�����γɹ���������NH4�����γɹ��̣�N2H5���ڼ�����Һ�н����ɵ����Եķ��Ӻ�ˮ����д����
��1���õ����Է��ӵĻ�ѧʽ��?��
��2��N2H5���ĵ���ʽ��?��
��3��1 mol N3������?mol ���ӣ�
��4��д�����ַǽ����������N3����������ͬ�����ʵĻ�ѧʽ?��?��
�ο��𰸣���1����ѧʽ��? N2H4?��?��2������ʽ��?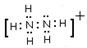 ?��
?��
��3����? 22?mol ���ӣ�?��4����ѧʽ? CO2?��? N2O?��
N2O?��
�����������
�����Ѷȣ�һ��
5������� ��4�֣���MgCl2��xH2O�ľ���4.06g����ˮ���100mL��Һ������Һ50mL������50mL0.4mol/L��AgNO3��Һ��ȫ���á����������ݿ�֪4.06g��MgCl2��xH2O���ʵ�����_______mol��ʽ��x����ֵ��_____��
�ο��𰸣�29. 0.02 6
������������ݹ�ϵʽ��MgCl2��xH2O-- MgCl2-- xH2O--2AgNO3
1 2
n 0.1x0.4 ���n=0.02moL
����M="m/n" ��95+18x��=4.06/0.02 ��� x=6.
���㣺���黯ѧ���㡣
�����Ѷȣ�һ��