微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题
(14分)工业废水中常含有一定量的Cr2O72―和CrO42―,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为

其中第①步存在平衡:2CrO42―(黄色)+2H+ Cr2O72―(橙色)+H2O
Cr2O72―(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72―和CrO42―的浓度相同 b.2v (Cr2O72―) ="v" (CrO42―) c.溶液的颜色不变
(3)第②步中,还原1mol Cr2O72―离子,需要________mol的FeSO4・7H2O。
( 4 ) 第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+ (aq)+3OH―(aq)
Cr3+ (aq)+3OH―(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)・c3(OH―)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72―的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
2、选择题 可逆反应:A(g)+3B(g)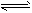 2C(g)达到平衡后,保持其他条件不变,将容器体积扩大到原来的两倍,下列叙述正确的是
2C(g)达到平衡后,保持其他条件不变,将容器体积扩大到原来的两倍,下列叙述正确的是
[? ]
正反应速率 逆反应速率 平衡运动方向
A. 增大 减小 正方向
B. 减小 增大 逆方向
C. 减小 减小 逆方向
D. 增大 增大 正方向
3、选择题 某一容器中发生如下反应:2NO(g)+O2(g)  2NO2(g); ΔH =" Q" kJ・mol-1,在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的关系如图所示。下列判断正确的是
2NO2(g); ΔH =" Q" kJ・mol-1,在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的关系如图所示。下列判断正确的是

A.p2 > p1且Q <0
B.p2 > p1且Q >0
C.p2 < p1且Q <0
D.p2 < p1且Q >0