微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某研究性学习小组为完成浓硝酸、稀硝酸、NO2、NO的部分实验,并有效地防止NO2、NO的污染。设计了如下图所示的装置进行实验。
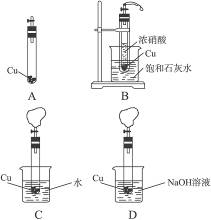
先将适量块状CaCO3和过量铜片放入底部开一小孔的试管中,塞上塞子(连有带活塞的导气管),如图A所示,再将试管放入盛有适量盐酸的烧杯中,打开活塞,发生反应:CaCO3+2HCl====CaCl2+H2O+CO2↑,用产生的CO2排尽试管内的空气。
(1)待CaCO3反应完全后,关闭活塞,在导气管上套一排尽空气的气球,然后将试管放入盛有浓硝酸的大试管中,如图B所示。再打开活塞,观察到的现象是_________________。上述现象说明____________________________________________________。有关反应的离子方程式为_____________________________________________________________________。
(2)上述反应进行一段时间后,关闭活塞,迅速将带小孔的试管取出,放入盛有适量水的烧杯中,如图C所示,再打开活塞,观察到的现象是_______________________________。
(3)关闭活塞,迅速将试管取出,放入盛有足量NaOH溶液的烧杯中,如图D所示。打开活塞,NO、NO2与NaOH溶液发生反应:2NaOH+NO+NO2====2NaNO2+H2O,气球逐渐变小,试管内液面上升。NO不能单独与NaOH溶液反应,若要将氮的氧化物完全吸收,应该如何操作?___________________________________________________。
参考答案:(1)铜片逐渐溶解,产生红棕色气体,气球逐渐膨胀,大试管中液体变为蓝色,烧杯内析出固体?铜与浓硝酸反应生成NO2气体和Cu(NO3)2蓝色溶液,该反应为放热反应? Cu+4H++2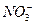 ====Cu2++2NO2↑+2H2O
====Cu2++2NO2↑+2H2O
(2)先看到气球逐渐变小,气体颜色逐渐变淡,烧杯内溶液变为浅蓝色,后气球慢慢膨胀
(3)取下气球,打开活塞(待试管内液面降到与烧杯中液面相平时),关闭活塞(此时试管内液面上升,气体颜色逐渐变淡)。重复上述操作至打开活塞不再出现红棕色为止
本题解析:根据题意弄清各仪器、试剂的作用是解题的关键。装置A相当于一个简易启普发生器,用CO2排尽试管内的空气的目的是避免NO被空气氧化成NO2而产生干扰;装置B中烧杯中饱和石灰水与反应无关,但可利用Ca(OH)2的溶解性的特殊性来检验反应是否放热;装置C中水可与气球内NO2反应3NO2+H2O====2HNO3+NO,HNO3再与Cu反应8HNO3+3Cu====3Cu(NO3)2+2NO↑+4H2O,因此气球先变小后回胀;装置D中NaOH可吸收NO2、NO混合气体,但不单独与NO反应,必须使NO与空气接触氧化成NO2再吸收。
本题难度:简单
2、选择题 由反应8NH3+3Cl2====N2+6NH4Cl可知,30 mL Cl2能氧化相同条件下的NH3的体积为(?)
A.80 ml
B.40 mL
C.20 mL
D.10 mL
参考答案:C
本题解析:被氧化NH3占整体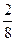 。
。
本题难度:简单
3、填空题 (15分)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
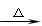
① A + H2O → B + C? ② C + F → D? ③ D + NaOH ?F + E + H2O
(1)写出它们的化学式:A?、B?、 D?、
E?、F?;
(2)写出各步反应的离子方程式,并指反应①的氧化剂和还原剂物质的量比。
① ?、氧化剂与还原剂物质的量比为:?。?
② ?。
③ ?。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式?。
参考答案:(1)A? NO2? B? NO? D? NH4NO3? E? NaNO3? F? NH3
 ?(2)① 3NO2 + H2O = 2H+ + 2NO3― + NO? 1:2
?(2)① 3NO2 + H2O = 2H+ + 2NO3― + NO? 1:2
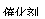 ? ③ H+ + NH3 = NH4+? ④ NH4+ + OH― ="====" NH3↑+ H2O
? ③ H+ + NH3 = NH4+? ④ NH4+ + OH― ="====" NH3↑+ H2O
(3)4NH3 + 5O2 ="=====" 4NO + 6H2O((1)题每空1分,其余每空2分)
本题解析:本题突破口在F,F是能使红色湿润石蕊是指变蓝的气体,说明F为NH3,可知A,B,C,D,E,F都含氮元素,而F与C生成D,且D与NaOH反应生成F与E还有H2O,说明E为钠盐,C为酸,再由①可知C为硝酸,B为NO,A为NO2为硝酸铵,E为硝酸钠
本题难度:一般
4、填空题 (12分)(Ⅰ)工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)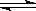 2NH3(g),其部分工艺流程如下:
2NH3(g),其部分工艺流程如下:
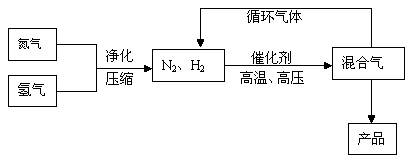
回答下列问题:
⑴已知:N2(g)+O2(g) =2NO(g);△H=180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ;△H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g) ;△H=-483.6kJ/mol
则N2(g)+3H2(g)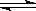 2NH3(g)的△H=_________________。
2NH3(g)的△H=_________________。
(2)假如该厂生产的氨水的pH=a,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH_________14-a,此时c(NH4+)________c(Cl-)(填“大于”“小于”或“等于”)。
Ⅱ:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa
时,16.0gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ,写出表示N2H4燃烧热的热化学方程式是?。
(2)肼―空气燃料电池是一种碱性燃料电池,电解质溶液是20%―30%的KOH溶液。肼―空气燃料电池放电时:
正极的电极反应式是?。
负极的电极反应式?。
(3)图是一个电化学过程示意图。
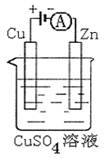
①锌片上发生的电极反应是?。
②假设使用肼―空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气??L(假设空气中氧气体积含量为20%)
参考答案:Ⅰ:(1)-92.4kJ/mol
(2)小于?等于
Ⅱ:(1) N2H4(l)+O2(g)=N2(g)+H2O(l);△H="-624kJ/mol?"
(2)? O2+4e-+2H2O=4OH-? N2H4-4e-+4OH-=N2↑+4H2O?
(3)? Cu2+ + 2e -=" Cu?" 112
本题解析:略
本题难度:简单
5、填空题 (14分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,则氧化剂与氧化产物的物质的量之比为?。
(2)上述反应中产生的气体可用?吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3― = 2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成48g S,则生成标准状况下的NO2的体积为?L。若准确测得的实际体积小于理论值(计算值),请分析可能原因?。
(4)某课外活动小组设计了以下实验方案验证Ag与浓HNO3反应的过程中可能产生NO。其实验流程图如下:
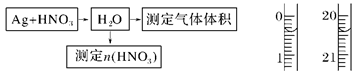
①测定硝酸的物质的量:
反应结束后,从如图B装置中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol・L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为?。
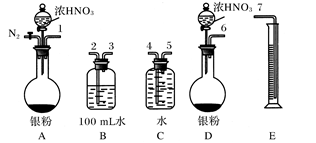
②测定NO的体积:
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中?(填“有”或“没有”)NO产生,作此判断的依据是?。
参考答案:(1)1:1?(2)氢氧化钠(或硫酸铜)溶液
(3)112L?部分NO2转化为N2O4使体积减小(或其它合理答案)
(4)①0.008 mol?②有?因为NO2与水反应生成的NO的体积小于收集到的NO的体积(89.6<112.0)
本题解析:(1)As由+3降为+2,Sn由+2升为+4,根据得失电子总数相等,As2S3和SnCl2的物质的量之比为1:1。
(2)反应中氧化剂是As2S3,生成的H2S气体可用NaOH溶液(或其它碱溶液)或硫酸铜溶液吸收。
(3)由反应式可知3×32gS对应标准状况下10×22.4LNO2,若生成48g S,则生成标准状况下的NO2的体积为112L;
由于存在可逆反应2NO2 N2O4,部分NO2转化为N2O4,致使测得的实际体积小于理论值
N2O4,部分NO2转化为N2O4,致使测得的实际体积小于理论值
(4)实验装置图为:

①消耗的NaOH溶液的体积为20.40―0.40=20.00ml,则硝酸的浓度为:c(HNO3)×25=0.1×20,c(HNO3)=0.08mol/L;
则在B容器中生成硝酸的物质的量为0.08×0.1=0.008mol
②由反应3NO2+H2O=2HNO3+NO可知,当生成0.008molHNO3时,生成的NO的体积为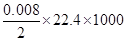 =89.6ml,但小于实验测得NO的体积为112.0 mL,故一定有NO生成
=89.6ml,但小于实验测得NO的体积为112.0 mL,故一定有NO生成
本题难度:一般