微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向CuSO4溶液中加入金属钠后,观察到的现象有(? )
A.看到红色铜生成
B.有气泡生成并产生蓝色沉淀
C.只看到蓝色沉淀生成
D.只有气泡生成
参考答案:B
本题解析:在金属活动性顺序表中,排在最前面的三种金属因其性质活泼,在与溶液反应时先与水反应而不能与金属阳离子发生置换反应。
将金属钠投入到溶液中,因钠性质活泼首先与H2O发生反应,生成NaOH与H2,生成的NaOH再与CuSO4溶液发生反应生成Cu(OH)2沉淀。
本题难度:简单
2、填空题 X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有如下转化关系:(部分反应物、产物及反应条件已略去)。
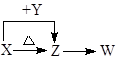
请回答下列问题:
(1)X与Y在水溶液中反应的离子方程式为?;
(2)W的结构式为??
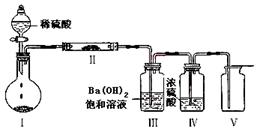
(3)将Z装入圆底烧瓶,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅱ中的物质由短周期元素组成,装置Ⅲ中产生白色沉淀,装置Ⅴ 中可收集到一种能使带火星木条复燃的气体。装置Ⅱ中物质的化学键类型为 ?;
(4)下列关于X、Z的鉴别方法不正确的是?
A.分别加热X、Z的粉末,将产生的气体通入澄清石灰水,观察现象
B.分别将X、Z配成稀溶液,逐滴滴加稀盐酸,观察现象
C.分别将X、Z配成稀溶液,分别加入氯化钙溶液,观察现象
D.分别将X、Z配成稀溶液,分别加入澄清石灰水,观察现象
参考答案:(7分)(1)HCO3- + OH-= CO32- + H2O? (2分)?(2)? O=C=O? (1分)
(3)离子键、共价键? (2分)?(4)D? (2分)
本题解析:X、Y、Z的焰色反应均为黄色,说明均含有钠元素。因此根据转化关系可知,X是碳酸氢钠,Z是碳酸钠,Y是氢氧化钠。W为无色无味气体,所以W是CO2。
(1)X与Y在水溶液中反应的离子方程式为HCO3- + OH-= CO32- + H2O。
(2)CO2是直线型结构,其结构式是O=C=O。
(3)稀硫酸和碳酸钠反应生成CO2,又因为装置Ⅲ中产生白色沉淀,因此该沉淀应该是碳酸钡。装置Ⅴ中可收集到一种能使带火星木条复燃的气体,则该气体是氧气,所以装置Ⅱ中物质是过氧化钠。其中含有的化学键类型为离子键、共价键。
(4)A中碳酸钠受热不分解,碳酸氢钠加热分解生成CO2,CO2能使澄清的石灰水变混浊,所以可以鉴别;B中碳酸钠和盐酸的反应是分步进行的,首先生成碳酸氢钠和氯化钠。而碳酸氢钠立即和盐酸反应生成CO2气体,可以鉴别。C中碳酸氢钠和氯化钙不反应,而碳酸钠和氯化钙反应生成白色沉淀碳酸钙,可以鉴别。D中碳酸钠和碳酸氢钠都能和澄清石灰水反应生成白色沉淀碳酸钙,不能鉴别,答案选D。
点评:该题是中等难度的试题,主要是考查学生读一钠及其化合物结构和性质,特别是有关转化的鉴别的熟悉了解程度,意在培养学生分析、归纳、总结问题的能力。有利于调动学生的学习兴趣,也有助于培养学生的逻辑推理能力和规范实验设计能力。
本题难度:一般
3、选择题 过氧化钠具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中不正确的是?(?)
A.Na2O2与木炭的反应是放热反应
B.熔融Na2O2时可使用石英器皿
C.Na2O2与Al反应时Na2O2表现出强氧化性
D.Na2O2与SO2反应可生成Na2SO4
参考答案:B
本题解析:略
本题难度:简单
4、选择题 在10mL 0.01mol・L-1的纯碱溶液中,逐滴加入1.2mL 0.05mol・L-1的盐酸并不断搅拌,完全反应后在标准状况下生成二氧化碳的体积是(?)
A.1.344mL
B.2.240mL
C.0.672mL
D.0mL
参考答案:D
本题解析:纯碱的物质的量为0.0001 mol,盐酸的物质的量为0.00006mol
向纯碱溶液中滴加盐酸可能依次发生如下反应:
CO32-+H+?= HCO3-
HCO3-+H+? = H2O +? CO2↑
从中可看出,盐酸不足,第二个反应根本没有发生,所以产生的气体为0ml,答案为D
本题难度:简单
5、选择题 将4.34gNa、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到672mL混合气体,该混合气体通过放电,恰好完全反应,则它们的物质的量之比为
A.1:1:1
B.1:1:2
C.1:2:1
D.4:3:2
参考答案:D
本题解析:因为Na2O和水反应是不会有任何气体产生的。这也是突破点。Na与水反应生成的是氢气,Na2O2与水反应生成的是氧气。混合气体为O2和H2的混合物,其物质的量为0.03mol,根据H2和O2反应的物质的量比为2:1,所以H2为0.02mol,O2为0.01mol,对应的Na就为0.04mol(0.92g),过氧化钠为0.02mol(1.56g),所以Na2O为4.34-0.92-1.56=1.86g,即为0.03mol,所以三者之比为0.04:0.03:0.02=4:3:2
点评:本题涉及到了物质的量的简单计算,其中有两个细节要抓住,一个是混合气体的成分,以及混合气体通过放点,恰好完全反应提示了氢气与氧气的物质的量之比是2:1。
本题难度:简单