| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《化学基本概念》高频试题强化练习(2017年最新版)(十)
参考答案:B 本题解析: 本题难度:一般 2、选择题 某温度下,将Cl2通入氢氧化钾溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量之比是1∶2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 |
参考答案:D
本题解析:Cl2生成ClO-与ClO3-是被氧化的过程,化合价分别由0价升高为+1价和+5价,经测定ClO-和ClO3-物质的量之比为1:2,则可设ClO-为1mol,ClO3-为2mol,被氧化的氯元素的物质的量为:1mol+2mol=3mol,根据化合价变化可知,反应中失去电子的总物质的量为:1mol×(1-0)+2mol×(5-0)=11mol,氧化还原反应中得失来源:91考试网 91eXAm.org电子数目一定相等,则该反应中失去电子的物质的量也是11mol,Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,则被还原的Cl的物质的量为: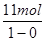 =11mol,所以被还原的氯元素和被氧化的氯元素的物质的量之比为11mol:3mol=11:3,答案选D。
=11mol,所以被还原的氯元素和被氧化的氯元素的物质的量之比为11mol:3mol=11:3,答案选D。
考点:考查氧化还原反应的计算。
本题难度:一般
3、选择题 下列反应的离子方程式正确的是
A.碳酸钠溶液与氯化钡溶液混合:Ba2++CO32-=BaCO3↓
B.铁片溶于稀硝酸中:2Fe+6H+=2Fe3++3H2↑
C.碳酸钙溶于盐酸中:CO32-+2H+=CO2↑+H2O
D.氢氧化铜溶于稀硫酸中:OH-+H+=H2O
参考答案:A
本题解析:硝酸是强氧化剂,铁与硝酸不生成氢气,生成NO,离子方程式为Fe+4H++NO3-=Fe3++NO↑+2H2O或3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,B错误;碳酸钙不溶于水,不能拆开,离子方程式应为CaCO3+2H+=Ca2++H2O+CO2↑,C错误;氢氧化铜不溶于水,不能拆开,离子方程式应为Cu(OH)2+2H+=Cu2++2H2O,D错误。
考点:离子方程式
点评:书写离子方程式时,易溶于水、易电离的物质拆成离子形式,难溶的物质、气体和水等仍用化学式表示。
本题难度:简单
4、填空题 在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原,若0.3mol氯气生成则若0.3mol氯气生成转移的电子数目为 。
参考答案:K2Cr2O7; HCl; Cl; Cr; 0.6 NA..
本题解析:K2Cr2O7中Cr的化合价由+6变为CrCl3中的+3,化合价降低,被还原,所以K2Cr2O7是氧化剂;HCl中一部分Cl的化合价由-1变为Cl2中的0,化合价升高,被氧化,是还原剂。若生成0.3mol氯气,转移的电子数目为0.6 NA..
考点:氧化还原反应的综合考查
本题难度:一般
5、选择题 下列各组混合气体中,比乙烯含碳量高的是
A.甲烷和丙烯
B.乙烷和丁烯
C.丙烷与丙烯
D.丙烯与丙炔
参考答案:D
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《反应速率与.. | |