��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ˮ������֮Դ��ˮ��������������������ռ����Ҫ��λ������ˮ����������ʾ��ͼ���¡�����ˮ����ƻ����������õľ�ˮ���оۺ��Ȼ�������ʽ�Ȼ����������������۱�ϩ�������ۺ��Ȼ����������Ȼ������ۺ��������ȣ�
��1��FeSO4��7H2O�dz��õĻ�����������ˮ����������?������
��2��[A12��OH��nClm]��һ�����߷��ӵĸ۾ۺϵ���ʻ�����������Ϊ�������Ȼ�������������֮���һ���м�ˮ������m��n֮��Ĺ�ϵ??��
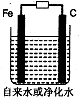
��3��������ˮ��������������ˮ�����ʵ�飬װ����ͼ��һ��ʱ��������������ɫ���������ܿ��ɺ��ɫ��Ȼ���þ�ˮ���������ˮ�����ʵ�飻������ֻ�����������ˮ�в��������Դ���˵������ˮ�ܡ��ࡱ���������ɺ��ɫʱ�������Ļ�ѧ��Ӧ����ʽΪ��?��
��4��MnSO4��ˮ�ʼ���е�һ�ֳ����Լ�
��MnSO4������أ�K2S2O8����������Һ�������Ӵ��¿ɷ���������ԭ��Ӧ�����ɸ�����ء������μ�����һ�ֲ��д������ƽ������Ӧ�Ļ�ѧ����ʽ��?��?
��ˮ�е��ܽ����ⶨ����Ϊ��ȡˮ����Ѹ�ټ���MnSO4��KOH���Һ���ټ���KI��Һ�������������ӣ���ʹ��ȫ��Ӧ����ӦΪ��Mn2++O2+H2O��MnOOH��δ��ƽ���������ӣ�Ѹ�ټ�������������Һ����ʱ�еⵥ�����ɡ�������ӷ�Ӧ����ʽ��?����Na2S2O3��Һ�ζ����ɵĵ⣬����������Һ������ɼ����ˮ���ܽ���������
2��ѡ���� �����£�ijδ֪��Һ��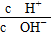 ��1��1012���Һ��д���Al3����NO3������
��1��1012���Һ��д���Al3����NO3������
�����Һ���Ƿ������������6�����ӣ���SiO32������NH4+����Fe2������Na������HCO3������Cl�������в��ؼ�����ܼ��Է�������(����)
A���٢ۢ�
B���ڢۢ�
C���٢ڢ�
D���ܢݢ�
3��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����
A.FeCl3��Һ�м������ۣ�Fe3++Fe��2Fe2+
B.�ƺ�ˮ��Ӧ��Na+H2O ��Na++OH-+H2��
C.������Һ�еμ�����������Һ��Ba2++SO42-��BaSO4��
D.���ռ���Һ�еμ����OH-+H+��H2O
4������� I����������20mL0��1mol/L Na2CO3��Һ����μ���0��1mol/L HCl��Һ40mL����Һ��pH���ͣ���ʱ��Һ�к�̼Ԫ�ص������ʵ���Ũ�ȵİٷֺ��������ᣩҲ�����仯��CO2���ݳ�δ����������ͼ��ʾ���ش���������
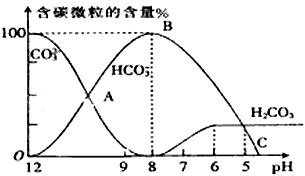
��1��H2CO3��HCO3-��CO32-�в��ܴ���������ͬһ��Һ�е���___________________��
��2��ʵ���ҿ��á�˫ָʾ�������ⶨ̼���ơ�̼�����ƻ����Һ�и������ʵĺ����������������£�
��ȡ������Ʒ�����Һ��
��ȡ25mL��Ʒ��Һ��ָʾ��A����0��1010mol/LNaOH����Һ�ζ����յ㣻
���ټ�ָʾ��B������0��1010mol/LNaOH����Һ�ζ����յ㡭��
ָʾ��B�ı�ɫ��Χ��pH=______���������롣
��3����pH=7ʱ����ʱ�ٵ���������Һ��������Ӧ���ӷ���ʽ��____________________��
��4����֪��25��ʱ��CO32-ˮ�ⷴӦ��ƽ�ⳣ����ˮ�ⳣ��Kh=2��10-4������Һ��c(HCO3-)�Uc(CO32-)=
2�U1ʱ����Һ��pH=_____________��
II��ij��Ԫ���ᣨ��дΪH2A����Һ������ʽ����һ���Ͷ������룺H2A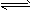 H++HA-��HA-
H++HA-��HA-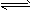 H++A2-
H++A2-
��֪��ͬŨ��ʱ�ĵ���Ȧ�(H2A)> ��(HA-)����������������Һ��
��A��0��01mol/L ��H2A��Һ
��B��0��01mol/L ��NaHA��Һ
��C��0��01mol/L ��HCl��0��04mol/L��NaHA��Һ��������Һ
��D��0��02mol/L ��NaOH��0��02 mol/L��NaHA��Һ��������Һ
�ݴˣ���д���пհף�����ţ� ��
��5��c(H+)������_________��c(H2A)������___________��c(A2-)������_________��
5������� ��9�֣�1 Lij�����Һ�����ܺ��е� �������±���
�������±���
���ܴ������е�������
| H+?NH4+ ?Al3+?K+
|
���ܴ������е�������
| Cl?- ?Br- ?I? ?ClO?AlO?2-
|
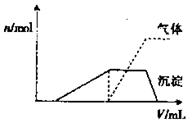
?(1)������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ�����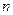 �����NaOH��Һ�������
�����NaOH��Һ�������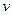 ���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
����ȷ���Ƿ��е���������__________��Ҫȷ������ڿɲ�������ʵ����________��
��2������⣬����Һ�к��д�����Cl�� ��Br����I��������1 L�û����Һ��ͨ�롪������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2�������״������ ��ϵ���±���ʾ��������ش��������⣺
��ϵ���±���ʾ��������ش��������⣺
Cl2���������״����
| 2.8L
| 5.6 L
| 11.2 L
|
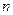 ��Cl���� ��Cl����
| 1.25mol
| 1.5 mol
| 2 mol
|
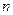 ��Br���� ��Br����
| 1.5 mol
| 1.4 mol
| 0.9 mol
|
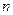 ��I���� ��I����
|  ?mol ?mol
| 0
| 0
|
�ٵ�ͨ��Cl2�����Ϊ2.8 Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ___?��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ_____________��