微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
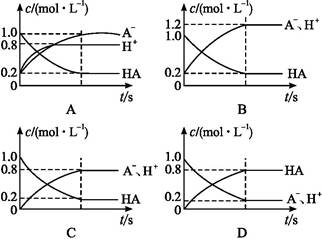
1、选择题 一元弱酸HA(aq)中存在下列电离平衡:HA A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
参考答案:C
本题解析:本题考查电离平衡原理与图像分析能力。根据弱酸HA的电离平衡知,HA的浓度由大到小,排除D项;A-、H+浓度由0增大,排除了A、B;平衡时,HA减小量等于A-的增加量。
本题难度:一般
2、选择题 在0.1 mol・L-1的HCN溶液中存在如下电离平衡HCN H++CN-,对该平衡,下列叙述正确的是( )
H++CN-,对该平衡,下列叙述正确的是( )
A.加入少量NaOH固体,平衡向正反应方向移动
B.加水,平衡向逆反应方向移动
C.滴加少量0.1 mol・L-1 HCl溶液,溶液中c(H+)减少
D.加入少量NaCN固体,平衡向正反应方向移动
参考答案:A
本题解析:加NaOH固体,OH-+H+ H2O,平衡正向移动,A项正确;加水平衡正向移动,B项错误;滴加少量0.1 mol・L-1 HCl溶液,c(H+)增大,C项错误;加入少量NaCN固体,c(CN-)增大,平衡逆向移动。
H2O,平衡正向移动,A项正确;加水平衡正向移动,B项错误;滴加少量0.1 mol・L-1 HCl溶液,c(H+)增大,C项错误;加入少量NaCN固体,c(CN-)增大,平衡逆向移动。
本题难度:一般
3、填空题 常温下,将0.05 mol・L-1盐酸溶液和未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的pH=12。用上述NaOH溶液12.5 mL和pH=3的某一元弱酸HA溶液20.0mL恰好完全反应生成NaA。
(1)此一元弱酸的物质的量浓度为?;
(2)此条件下该一元弱酸的电离平衡常数为?。
参考答案:
(1)0.025 mol・L-1?(2)4.0×10-5
本题解析:(1)首先求出题出所给的氢氧化钠的物质的量浓度c(NaOH):设盐酸和氢氧化钠的体积分别为1L和2L,那么有如下关系: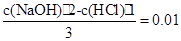 ,解之得:c(NaOH)="0.04" mol・L-1
,解之得:c(NaOH)="0.04" mol・L-1
用上述NaOH溶液12.5 mL和pH=3的某一元弱酸HA溶液20.0mL恰好完全反应生成NaA,表明有如下关系:0.04 mol・L-1×12.5 mL=c(某酸) ×20 mL,解之得:c(某酸)=? 0.025 mol・L-1
(2)一元弱酸HA溶液pH=3,? HA?=? H+?+? A-
起始:? 0.025?0? 0
转化:?0.001? 0.001? 0.001
平衡:? 0.024? 0.001? 0.001
因此此条件下该一元弱酸的电离平衡常数为:?
本题难度:一般
4、选择题 将体积均为10mL、pH都等于3的醋酸和盐酸,加水稀释至amL和bmL,测得稀释后溶液的pH均为5。则稀释后的溶液的体积
[? ]
A.a=b=100mL
B.a=b=1000mL
C.a<b
D.a>b?
参考答案:D
本题解析:
本题难度:一般
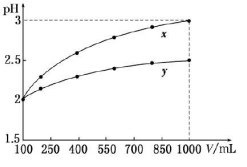
5、选择题 pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示。分别滴加NaOH溶液(c=0.1mol/L)至pH =7,消耗NaOH溶液的体积为 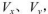 ,则
,则
A.x为弱酸,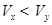
B.y为弱酸,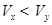
C.x为强酸,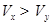
D.y为弱酸,