|
���л�ѧ֪ʶ�㽲�⡶�����йص����ӷ���ʽ����д�����߲��ԣ�2017�����°棩(ʮ)
2017-08-26 00:22:47
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��ȷ����
A������������ˮ��Ӧ�� 2O22-+2H2O==O2��+4OH-
B������������Fe(OH)3�ڼ�����Һ�з�Ӧ����Na2FeO4��
3ClO-+2Fe(OH)3==2FeO42-+3Cl-+H2O+4H+
C����������KAl(SO4)2��12H2O����Һ����μ���Ba(OH)2��Һ��SO42-ǡ����ȫ������
2Al3++3SO42-+3Ba2++6OH-==2Al(OH)3��+3BaSO4��
D����̼����þ��Һ�м�������ij���ʯ��ˮ��
| Mg2++2HCO3-+2Ca2++4OH-==Mg(OH)2��+2CaCO3��+2H2O
�ο��𰸣�D
���������A����ȷ����������Ӧ���û�ѧʽ��ʾ��B����Һ�Լ��ԣ����������в������������ӣ�����ȷ��C�е�SO42��ǡ�ó���ʱ��Al3��ǡ������ƫ����أ�C����ȷ�������ȷ�Ĵ�ѡD��
�����Ѷȣ�һ��
2��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ѧ����ʽ��ȷ����(? )
A��ϡ�����������м��Ӧ��Fe+4H++ NO3����Fe3++NO��+2H2O
B��̼������Һˮ������ӷ���ʽ��CO32��+2H2O H2CO3+2OH�� H2CO3+2OH��
C��������ȼ����Ϊ285.8 kJ/mol�����ʾ����ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g) + O2(g) = 2H2O(g)����H =" �C571.6" kJ/mol
D��Ũ������MnO2������������MnO2��4H����2Cl�� Mn2����Cl2����2H2O Mn2����Cl2����2H2O
�ο��𰸣�D
���������A����ȷ��������ʱ���ɵ����������ӣ�B����ȷ��CO32��ˮ���Ƿֲ����еģ�ȼ��������һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų������������C����ȷ��������ȷ�Ĵ�ѡD��
�������ж����ӷ���ʽ��ȷ���ķ���һ���ǣ���1����鷴Ӧ�ܷ�������2����鷴Ӧ��������Ƿ���ȷ����3���������ʲ���Ƿ���ȷ����4������Ƿ�����غ��ϵ���磺�����غ�͵���غ�ȣ�����5������Ƿ����ԭ��ѧ����ʽ��
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ���ӷ���ʽ��ȷ���ǣ�������
A������������������Һ��ӦC6H5OH+OH--C6H5O-+H2O
B��̼������ڴ���CaCO3+2H+=Ca2++CO2��+H2O
C��̼������Һ��������ı���2C6H5OH+CO32--2C6H5O-+CO2��+H2O
D������������Һ��HCHO+2[Ag��NH3��2]++2OH--HCOO-+NH4++2Ag��+3NH3+H2O
�ο��𰸣�A������������������Һ��Ӧ�����ӷ�ӦΪC6H5OH+OH-��C6H5O-+H2O����A��ȷ��
B��̼������ڴ�������ӷ�ӦΪCaCO3+2HAc=Ca2++2Ac-+CO2��+H2O����B����
C��̼������Һ��������ı��ӵ����ӷ�ӦΪC6H5OH+CO32-��C6H5O-+HCO3-����C����
D����ȩ�����������Һ��Ӧ�����ӷ�ӦΪHCHO+4[Ag��NH3��2]++4OH-��CO32-+2NH4++4Ag��+6NH3+2H2O����D����
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A���������м���ϡ���2Fe+6H+�T3Fe3++3H2��
B���������������ϣ�Ag++HCl�TAgCl��+H+
C��ʯ��ʯ���ڴ��CaCO3+2CH3COOH�T2CH3COO-+Ca2++CO2��+H2O
D���Ȼ�����Һ�м���������ˮ��Al3++3OH-�TAl��OH��3��
�ο��𰸣�A���������м���ϡ���ᣬ��Ӧ���ɵ����������ӣ���ȷ�����ӷ���ʽΪ��Fe+2H+�TFe2++H2������A����
B���������������ϣ�����Ӧ�ò���ȷ�����ӷ���ʽΪ��Ag++Cl-�TAgCl������B����
C��ʯ��ʯ���ڴ��ᣬ��Ӧ�����˴���ơ�������̼��ˮ����Ӧ�����ӷ���ʽΪ��CaCO3+2CH3COOH�T2CH3COO-+Ca2++CO2��+H2O����C��ȷ��
D���Ȼ������������ˮ�������������������Ȼ�泥������������������ˮ��һˮ�ϰ�Ϊ���Ӧ�ñ�������ʽ����ȷ�����ӷ���ʽΪ��Al3++3NH3?H2O=Al��OH��3��+3NH4+����D����
��ѡC��
���������
�����Ѷȣ���
5������� ��ÿ��2�֣���12�֣�д�����з�Ӧ�����ӷ���ʽ��
��1��������������ˮ����������������������������������������
��2���մ���Һ�е�������������������������������������������
��3��ʵ������Cl2������������������������������������������
��4��Al��NaOH��Һ��Ӧ������������������������������������
��5����NaHSO4��Һ����μ���Ba (OH)2��Һ����Һ������������������������������������������Һ�У������μ�Ba(OH)2��Һ��������������������������������
�ο��𰸣���12�֣�(1) 2Na2O2+ 2H2O= 4Na++OH- +O2��
(2) CO32-+H+= HCO3-
(3) 4H++2Cl-+MnO2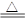 Mn2+ +Cl2+2H2O Mn2+ +Cl2+2H2O
(4) 2Al + 2OH- + 2H2O =2AlO2- + 3H2
(5)2H++SO42-+Ba2++2OH-=BaSO4��+2H2O�� Ba2++ SO42- =BaSO4��
ÿ��2�֣���14�֡�
�����������1��������������ˮ�Ļ�ѧ����ʽΪ2Na2O2+ 2H2O= 4NaOH+O2����ֻ��NaOH���Բ�����ܲ������ӷ���ʽΪ2Na2O2+ 2H2O= 4Na++OH- +O2������2����Ϊ�������ᣬ����ֻ������̼�����ƣ��������ɶ�����̼��CO32-+H+= HCO3-����3��ʵ������Cl2һ����Ũ����Ͷ������̣���Ҫ���ȣ�4H++2Cl-+MnO2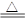 Mn2+ +Cl2+2H2O����4��Al��NaOH��Һ��Ӧ����ƫ��������������Ҫע����ˮ���뷴Ӧ��2Al + 2OH- + 2H2O =2AlO2- + 3H2����5����NaHSO4��Һ����μ���Ba (OH)2��Һ����Һ�����������ߵı�����2:1���������ӷ���ʽΪ2H++SO42-+Ba2++2OH-=BaSO4��+2H2O�������μ�Ba(OH)2��Һ���Ѿ���Ӧ��ɣ�ֻ�ж��������������뱵���ӷ�Ӧ��Ba2++ SO42- =BaSO4���� Mn2+ +Cl2+2H2O����4��Al��NaOH��Һ��Ӧ����ƫ��������������Ҫע����ˮ���뷴Ӧ��2Al + 2OH- + 2H2O =2AlO2- + 3H2����5����NaHSO4��Һ����μ���Ba (OH)2��Һ����Һ�����������ߵı�����2:1���������ӷ���ʽΪ2H++SO42-+Ba2++2OH-=BaSO4��+2H2O�������μ�Ba(OH)2��Һ���Ѿ���Ӧ��ɣ�ֻ�ж��������������뱵���ӷ�Ӧ��Ba2++ SO42- =BaSO4����
����������д���ӷ���ʽ�У�һ����д����ɾ�����IJ����ѵ�����Щ���ʸò���Щ���ʲ��ò�ǿ�ᡢǿ��Ϳ�������Ҫ��д��������ʽ�����������ʻ��ѵ�������ʣ��������Ρ����ᡢ������塢���ʡ����������û�ѧʽ��
�����Ѷȣ�һ��
|