��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ijNa2CO3��NaAlO2�Ļ����Һ����μ���1 mol��L-1������,�����Һ�е�C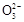 ��HC
��HC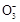 ��Al
��Al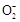 ��Al3+�����ʵ�����������������仯��ϵ��ͼ��ʾ,������˵����ȷ���ǣ�?��
��Al3+�����ʵ�����������������仯��ϵ��ͼ��ʾ,������˵����ȷ���ǣ�?��
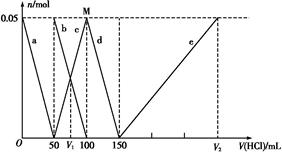
A��ԭ�����Һ�е�C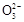 ��Al
��Al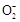 �����ʵ���֮��Ϊ1��2
�����ʵ���֮��Ϊ1��2
B��V1��V2=1��5
C��M��ʱ���ɵ�CO2Ϊ0.05 mol
D��a�߱�ʾ�����ӷ���ʽΪ:Al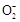 +H++H2O
+H++H2O Al(OH)3��
Al(OH)3��
�ο��𰸣�D
�����������������:HCl>H2CO3>HC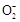 >C
>C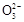 >Al(OH)3,��������Na2CO3��NaAlO2�Ļ����Һ����μ���1 mol��L-1������Ĺ�����,���ȷ�����Ӧ��Al
>Al(OH)3,��������Na2CO3��NaAlO2�Ļ����Һ����μ���1 mol��L-1������Ĺ�����,���ȷ�����Ӧ��Al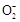 +H++H2O
+H++H2O Al(OH)3��,��a�߱�ʾ����Al
Al(OH)3��,��a�߱�ʾ����Al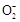 �����ʵ���,Dѡ����ȷ,��n(Al
�����ʵ���,Dѡ����ȷ,��n(Al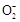 )="n(HCl)=0.05" mol;Ȼ������Ӧ��C
)="n(HCl)=0.05" mol;Ȼ������Ӧ��C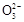 +H+
+H+ HC
HC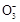 ,b�߱�ʾ����C
,b�߱�ʾ����C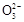 �����ʵ���,c�߱�ʾ����HC
�����ʵ���,c�߱�ʾ����HC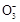 �����ʵ���,n(C
�����ʵ���,n(C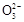 )="n(HCl)=0.05" mol,��n(C
)="n(HCl)=0.05" mol,��n(C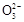 )��n(Al
)��n(Al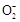 )=1��1,Aѡ���;V1��ʾC
)=1��1,Aѡ���;V1��ʾC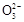 ��HC
��HC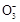 ���ʵ������ʱ������������,��ʱV1="75" mL,M��ʾ��ӦC
���ʵ������ʱ������������,��ʱV1="75" mL,M��ʾ��ӦC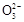 +H+
+H+ HC
HC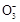 ǡ�����,��ʱ��û�зų�CO2,Cѡ���;�ٺ�����Ӧ��H++HC
ǡ�����,��ʱ��û�зų�CO2,Cѡ���;�ٺ�����Ӧ��H++HC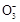
 CO2��+H2O,HC
CO2��+H2O,HC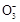 �����ʵ�����Ӧ����d��,�ٺ��� ��Ӧ��Al(OH)3+3H+
�����ʵ�����Ӧ����d��,�ٺ��� ��Ӧ��Al(OH)3+3H+ Al3++3H2O,Al3+�����ʵ�����Ӧ����e��,V2="3��50" mL+150 mL="300" mL,V1��V2=75��300=1��4,Bѡ�����
Al3++3H2O,Al3+�����ʵ�����Ӧ����e��,V2="3��50" mL+150 mL="300" mL,V1��V2=75��300=1��4,Bѡ�����
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����?
[? ]
A��̼����þ��Һ�������ʯ��ˮ��Mg2++2HCO3-?+Ca2++2OH��=?CaCO3��+2H2O+MgCO3��
B����̼������Һ�������������������壺2CO32-+?SO2?+?H2O?=?2HCO3-?+?SO32-
C������Fe�ͽ���Cu�������缫���������ҺΪŨ���ṹ�ɵ�ԭ��صĸ�����Ӧ��Fe?-?2e��?=?Fe2+
D������SO2ͨ�뵽Ba(NO3)2��Һ�У�3SO2?+?2NO3�C+?3Ba2+?+?2H2O?=?3BaSO4��+?2NO?+?4H+
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3������� ��8�֣������������ܶ࣬����H2SO4��H2SO3��SO2��Na2SO3��BaSO4��CuSO4��Na2SO4��7�ֳ����ĺ�����ش��������⣺
��1��д����Ԫ�������ڱ���λ��______________
��2��Ba2+�о綾��ij��������һ�𡰶��ձ����¼����������ձ�̯���������ձ��Ĺ�������̼�ᱵ�����ɷ�ʹ�ã����¶���ʳ���ձ����ж�����д��̼�ᱵ��θ�ᣨ�������ʾ����Ӧ�����ӷ�Ӧ����ʽ����?������������
��3�������£�����������Ũ�����У����������α��Ͻ���Ϊ�����˶ۻ�����������Ϊδ������Ӧ��Ϊ��֤�˹��̣�ijͬѧ����˼�������������ʵ�飺����Ũ���ᴦ����������ϴ��������CuSO4��Һ�У������������� �����������������������������˶ۻ���
��4������SO2����Ⱦ�����Ϊ�����ҹ�����̽����һ����������CO��ԭSO2�õ�������ķ�������ȥSO2���÷�Ӧ�Ļ�ѧ����ʽ������������?����������
�ο��𰸣�(1)3? VIA ;?(2) BaCO3+2H+��Ba2++CO2+H2O; (3)����������;?(4) SO2+2CO S+2CO2
S+2CO2
�����������1��16��Ԫ����Ԫ�غ�������Ų���2��8��6�����S�����ڱ���λ����λ�ڵ������ڵ�VIA�� ; ��2��̼�ᱵ��θ�ᣨ�������ʾ����Ӧ�����ӷ�Ӧ����ʽ��BaCO3+ 2H+��Ba2++H2O+CO2������3������Ũ���ᴦ����������ϴ��������CuSO4��Һ�У���δ���������ͻᷢ����Ӧ��Fe+ CuSO4= Cu+FeSO4,������Ϊ��ɫ��������������������������������;��40�������⣬�÷�Ӧ�ķ���ʽΪSO2+2CO S+2CO2��
S+2CO2��
�����Ѷȣ�һ��
4��ѡ���� ���л�ѧ����ʽ�����ӷ���ʽ����ȷ���ǣ�?��
A��S��Cu��Ӧ Cu+S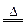 CuS
CuS
B��������ù�����pH��С 2H2SO3+O2�T2H2SO4
C�������������Һ������ʯ��ˮ���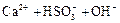 �TCaSO3��+H2O
�TCaSO3��+H2O
D����Na2S��Na2SO3�Ļ����Һ�еμ�ϡH2SO4[n(Na2S)��n(Na2SO3)=2��1]
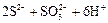 �T3S����3H2O
�T3S����3H2O