��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ����һѧ����ʵ���Ҳ�ij��ҺpH��ʵ��ʱ������������ˮ��ʪpH��ֽ��Ȼ���ýྻ����IJ�����պȡ�������м�⡣
�����ִ������?���һ����/��һ������/����һ�������ᵼ��ʵ��������
�������˷��ֱ�ⶨc(H+)��ȵ�����ʹ�����Һ��pH�����ϴ����?��
�ơ�����֪Ũ�ȵ� NaOH ��Һ�ⶨij HCl��Һ��Ũ�ȣ��ο���ͼ���ӱ���ѡ����ȷ��� _____________
���
| ��ƿ����Һ
| �ζ�������Һ
| ѡ��ָʾ��
|  ѡ�õζ��� ѡ�õζ���
|
A
| ��
| ��
| ʯо
| ���ң�
|
B
| ��
| ��
| ��̪
| ���ף�
|
C
| ��
| ��
| ����
| ���ף�
|
D
| ��
| ��
| ��̪
| ���ң�
|
�ǡ��ñ���NaOH�ζ�δ֪Ũ�ȵ����ᣬѡ�÷�̪Ϊָʾ������ɲⶨ���ƫ�ߵ�ԭ�������?��
A. ���Ʊ���Һ�����������л���Na2CO3����
B. �ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ�������������ȷ
C. ʢװδ֪Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
D. �ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ
E. δ�ñ�Һ��ϴ��ʽ�ζ���
�ȡ���֪�ζ�����װ��Ũ��Ϊ0.112mol/L�����ᡣ��μ��뵽װ���������Ƶ���Һ����ƿ�С���ʼʱ������ǡ�÷�Ӧʱ����Ķ������±���
ʵ��
���
| ��������������Һ�����mL��
| �ζ���ʼ������mL��
| �����������mL��
| �������������mL��
|
��
| 25��00
| 0��02
| 26��40
| ?
|
��
| 25��00
| 0��04
| 25��81
| ?
|
��
| 25��00
| 0��03
| 25��78
| ?
|
��
| 25��00
| 0��20
| 25��96
| ?
|
?�Լ��������������Ƶ����ʵ���Ũ��=?.
�ο��𰸣��Ţٲ�һ��? ������?��? D ?��? ADE?��? 0.1158mol/L
�����������1������������ˮ��ʪ��pH��ֽ������Һ��pHʱ���൱�ڰ�ԭ��Һϡ�ͣ����Բ�һ������������ԭ��Һ�����ԣ����Dz�Ӱ��ġ�
�����ڴ��������ᣬ���ڵ���ƽ�⣬��ϡ�ʹٽ����룬���������˷��ֱ�ⶨc(H+)��ȵ�����ʹ�����Һ��pH�����ϴ��Ӧ�������ᡣ
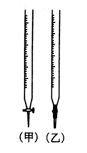
��2������֪Ũ�ȵ� NaOH ��Һ�ⶨij HCl��Һ��Ũ�ȣ�����Ҫ��ʽ�ζ��ܣ���ѡ���ң�����Ϊһ�㲻ѡ��ʯ����Һ��ָʾ��������Ӧ��ѡ���̪��ָʾ��������ѡD��
��3�����ڵ�������̼�������ĵ�����С�ڵ������������������ĵ����ᣬ�����ڵζ����������ĵļ�Һ���ƫ�࣬��ⶨ���ƫ�ߣ��ζ��ܵĿ̶����϶�����������ģ����Եζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ������ƫС�����Բⶨ���ƫ�ͣ�C���DZ�ҪӰ��ģ��ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ������������������Һ�����ƫ�࣬���Բⶨ���ƫ�ߣ�δ�ñ�Һ��ϴ��ʽ�ζ��ܣ����൱��ϡ������������Һ��������������������Һ�����ƫ�࣬�ⶨ���ƫ�ߣ���˴�ѡADE��
��4�����ݱ������ݿ�֪�����ĵ���������ֱ���25.98ml��25.77ml��25.75ml��25.76ml���������������ƽ��ֵ�ǣ�25.98ml��25.77ml��25.75ml��25.76ml����4��25.87ml����������������Һ��Ũ����25.87ml��0.112mol/L��25.00ml��0.1158mol/L��
�������ڽ����к͵ζ�������ʱ����Ҫ����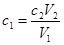 ������ʵ������У�V1��C2�Dz���ģ���˹ؼ��Ƿ�����������ε���V2�仯�ļ��ɡ�
������ʵ������У�V1��C2�Dz���ģ���˹ؼ��Ƿ�����������ε���V2�仯�ļ��ɡ�
�����Ѷȣ�һ��
2��ѡ���� ij�¶��µ���Һ��c(H��)��10xmol/L��c(OH��)��10ymol/L��x��y�Ĺ�ϵͼ��ʾ������˵����ȷ����
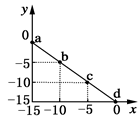
A�����¶ȸ���25��
B��ͼ��a����Һ�ʼ���
C�����¶��£�0.01 mol��L��1��HCl��Һ��pH=2
D�����¶��£�0.01 mol��L��1��NaOH��Һ��pH=12
�ο��𰸣�BC
���������A��c(OH��)+c(H��)��10-15,��25��ʱc(OH��)+c(H��)��10-14���ʸ��¶�Ӧ����25�档
B��a���Ӧ��c(H��)��10��15mol/L��c(OH��)��0mol/L����Ϊ���ԡ�
C��0.01 mol��L��1��HCl��Һ��c(H��)��10-2������pH=-�S10��H��)����PH=2��
���������⿼������ҺPH�������ӡ����������ӵĹ�ϵ����Ϥ����PH�ļ���ʽ���ѶȲ���
�����Ѷȣ�һ��
3��ѡ���� 250Cʱ����ˮ(D2O)�����ӻ�Ϊ1��6��10-15Ҳ����pHֵһ���Ķ������涨�����ȣ�pD==-lgCD+������������ȷ����(? )
������D2O��pD=7
����1LD2O�У��ܽ�0��01molDCl����pDֵΪ1
��1L0.1mol��L��NaOD����ˮ��Һ��pD=12
����100mL0 .25rnoL��LDCl����ˮ��Һ�У�����50mL0. 2mo1����L NaOD����ˮ��Һ����Ӧ����Һ��pD=1
���¶����ߣ�CD+��COD-��ֵ������
A���ڢ�
B���ۢ�
C���٢�
D���ܢ�
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4��ѡ���� �����Ȼ�ѧ����ʽ�� ��H����ֵ�ܱ�ʾ��ȼ���ȵ���
A��H2(g) + Cl2(g) =" 2HCl(g)" ��H =��184.6kJ/mol
B��CH4(g) + 2O2(g) = CO2(g) + 2H2O(g)��H =��802.3kJ/mol
C��2H2(g) + O2(g) = 2H2O(l)��H =��571.6kJ/mol
D��CO(g) + 1/2O2(g) = CO2(g)��H =��283kJ/mol