微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将相等物质的量的CO和H2O(g)混合,在一定条件下反应:CO(g)+H2O(g)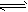 CO2(g)+H2(g),达到平衡后CO的转化率为25%,平衡混合气体的密度是相同条件下氢气的倍数是
CO2(g)+H2(g),达到平衡后CO的转化率为25%,平衡混合气体的密度是相同条件下氢气的倍数是
[? ]
A.46
B.23
C.11.5
D.5.75
参考答案:C
本题解析:
本题难度:一般
2、填空题 甲、乙、丙、丁四种物质转化关系如右图。已知甲是地壳中含量最高的元素组成的单质,化合物乙、丙、丁均含有第三周期一种相同元素。
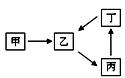
(1)若乙是难溶于水的酸性氧化物。
①乙的一种重要用途是? ?;
?;
②丙溶液中通入少量CO2生成丁的离子方程式是?。
(2)若2乙(g) + 甲(g)  ?2丙(g),是工业生产中重要反应之一。
?2丙(g),是工业生产中重要反应之一。
恒容条件下,一定量的乙和甲发生反应,不同温度下乙的转化率如下表所示:
温度/℃
| 400
| 450
| 500
| 550
| 600
| 650
|
转化率/%
| 99.2
| 97.5
| 93.5
| 85.6
| 73.7
| 58.5
|
①该反应的△H?0(填“>”、“<”或“=”,下同);
②若400℃和500℃的化学平衡常数分别为K1、K2,则K1?K2。
(3)若丙是离子化合物,且阴离子含金属元素R。
①R的原子结构示意图是?;
②已知:R(s) + 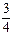 O2(g) =
O2(g) = 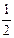 R2O3(s)? △H=-834.8 kJ・mol-1
R2O3(s)? △H=-834.8 kJ・mol-1
Mn(s) + O2(g) = MnO2(s)? △H=-520.9 kJ・mol-1
写出R的单质与MnO2反应的热化学方程式?。
参考答案:(1)①制造光导纤维或生产玻璃等(其他合理答案均给分)?(2分)
②SiO32-+CO2+H2O=H2SiO3↓+CO32-(其他合理答案均给分)?(3分)
(2)①<?(2分)
②>?(2分)
(3)①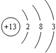 ?(2分)
?(2分)
②Al(s)+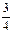 MnO2(s)=
MnO2(s)= Al2O3(s) +
Al2O3(s) +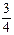 Mn(s) ?△H=-444.1 kJ・mol-1
Mn(s) ?△H=-444.1 kJ・mol-1
(其他合理答案均给分)?(3分)
本题解析:略
本题难度:简单
3、选择题 对于平衡体系mA(g)+nB(g) ?pC (g)+q(g);△H<0。下列结论中不正确的是(?)?
?pC (g)+q(g);△H<0。下列结论中不正确的是(?)?
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol
D.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
参考答案:D
本题解析:容器的体积缩小到原来的一半的瞬间,A的浓度是原来的2倍,但最终平衡后A的浓度为原来的2.1倍,说明反应向逆反应方向移动,因此m+n<p+q,A正确。只有按照相应的化学计量数之比充入,其转化率从能相等,B正确。体积不变,则物质的量也是不变的,C正确。增大压强,平衡不一定移动,所以选项D是错误的。答案选D。
本题难度:一般
4、填空题 高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO (g)  Fe(s)+ CO2(g)?△H>0
Fe(s)+ CO2(g)?△H>0
(1)此反应的平衡常数表达式为:K=??
(2)温度升高,达到新的平衡后,高炉内CO2与CO的体积比?(填“增大”、“减小”或“不变”)。
(3)已知1100℃时,K= 0.263。某时刻测得高炉中c(CO2)=" 0.025" mol・L-1,c(CO)=" 0.1" mol・L-1,在这种情况下,该反应?(填“向正反应方向进行”或“向逆反应方向进行”或“处于化学平衡状态”)。
(4)由氢气和氧气反应生成1mol水蒸气放热241.8KJ,已知氢气中H-H键能为436 kJ/mol,氧气分子中 O=O键能为498 kJ/mol,则水分子中O-H键的键能为??kJ/mol?。若1 g水蒸气转化成液态水时放热2.5 kJ,则反应H2(g) + 1/2O2(g) ==?H2O(l)的
△H=?kJ/mol
参考答案:(1)? c(CO2)/c(CO)?(2)增大?(3)?向正反应方向进行?(4))463.4?-286.8
本题解析:(1)FeO(s)+ CO (g)  Fe(s)+ CO2(g)?的反应的平衡常数表达式为:K=c(CO2)/c(CO)?,(固体物质不必写进平衡常数表达式);(2)△H>0,所以温度升高,平衡向右移动,即平衡常数K增大,所以CO2与CO的体积比增大;(3)温度不变,K不变,所以 c(CO2)/c(CO)?=0.025/0.1=0.25<0.263,所以该反应向正反应方向进行;
Fe(s)+ CO2(g)?的反应的平衡常数表达式为:K=c(CO2)/c(CO)?,(固体物质不必写进平衡常数表达式);(2)△H>0,所以温度升高,平衡向右移动,即平衡常数K增大,所以CO2与CO的体积比增大;(3)温度不变,K不变,所以 c(CO2)/c(CO)?=0.025/0.1=0.25<0.263,所以该反应向正反应方向进行;
(4)241.8=2×O-H键的键能-(436+0.5×498 ),所以O-H键的键能为463.4?kJ/mol,1 g水蒸气转化成液态水时放热2.5 kJ,即1mol水蒸气转化成液态水时放热45 kJ,所以
H2(g) + 1/2O2(g) ==?H2O(l)的△H=-(241.8+45)kJ/mol=-286.8kJ/mol。
点评:本题综合考查了化学平衡,热化学方程式的相关知识,考查比较全面,是高考考查的热点,该题难度适中。
本题难度:一般
5、填空题 二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上利用煤的汽化产物(水煤气)合成二甲醚。
请回答下列问题:
(1)煤的汽化的主要化学方程式为?。
(2)利用水煤气合成二甲醚的总反应式可表示为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H< 0。一定条件下得密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是?(填字母代号)。
CH3OCH3(g)+CO2(g) △H< 0。一定条件下得密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是?(填字母代号)。
A.高温高压
B.加入催化剂
C.减少CO2的浓度
D.增加CO的浓度 E.分离出二甲醚
 CH3OCH3(g)+H2O(g),某温度下得平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g),某温度下得平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下: